La química de los elementos y sus enlaces es fascinante... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
357
•
Actualizado May 6, 2026
•
Paula Solorzano
@paulasolo_vztxf
La química de los elementos y sus enlaces es fascinante... Mostrar más












La química es la ciencia que estudia la composición, estructura y propiedades de la materia. Esta asignatura es fundamental para entender los procesos que ocurren en nuestro entorno cotidiano.
Las notas que estás a punto de estudiar cubren conceptos esenciales como la tabla periódica y los enlaces químicos, herramientas fundamentales para cualquier estudiante de química.
💡 ¡Recuerda! La química no solo se trata de fórmulas y ecuaciones, sino de entender cómo funciona el mundo a nivel molecular.

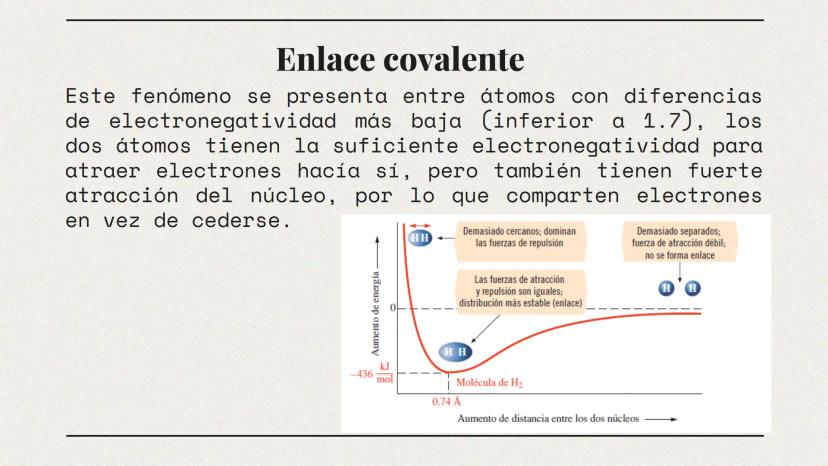
El enlace químico es el fenómeno que mantiene unidos a los átomos para formar moléculas o compuestos. Es uno de los conceptos más importantes en química porque explica cómo se forman las sustancias que nos rodean.
Entender los enlaces químicos nos permite comprender por qué algunas sustancias son resistentes mientras otras son frágiles, por qué algunas conducen electricidad y otras no, y cómo ocurren las reacciones químicas.
En las próximas páginas estudiaremos cómo se organizan los elementos y los diferentes tipos de enlaces que pueden formar entre sí.

¿Te has preguntado cómo se organizan los más de 100 elementos conocidos? En 1869, el químico ruso Dimitri Mendeleev revolucionó la química cuando publicó un ordenamiento de los elementos conocidos en su época.
Mendeleev descubrió que las propiedades de los elementos se repetían periódicamente cuando se ordenaban según su masa atómica. Esta observación fue clave para organizar todos los elementos de manera lógica y predecible.
Su trabajo fue tan brillante que incluso dejó espacios vacíos para elementos aún no descubiertos, prediciendo correctamente sus propiedades. ¡Imagina predecir la existencia de algo que nadie ha visto nunca!
💡 Dato interesante: Mendeleev jugaba "solitario" con tarjetas que tenían información de cada elemento para encontrar patrones en sus propiedades.

La tabla de Mendeleev no era perfecta. Algunos elementos no encajaban bien en su organización basada en la masa atómica. ¿Por qué? Porque faltaba un concepto clave que se descubriría casi 50 años después.
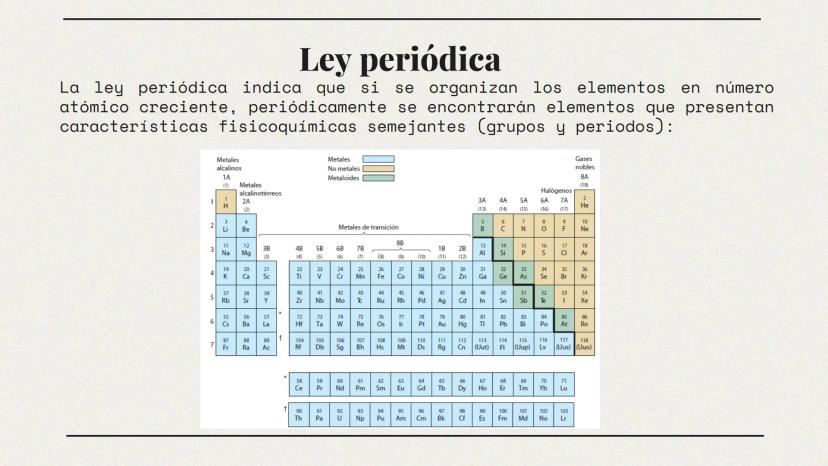
Fue el número atómico (la cantidad de protones en el núcleo), y no la masa atómica, lo que realmente determinaba las propiedades periódicas de los elementos. Este descubrimiento llevó a establecer la ley periódica:
"Las propiedades de los elementos son funciones periódicas de sus números atómicos"
Este principio fundamental permite predecir el comportamiento químico de los elementos con solo conocer su posición en la tabla periódica, lo que la convierte en una herramienta esencial para cualquier químico.

La tabla periódica está organizada en filas horizontales (periodos) y columnas verticales (grupos). Esta estructura no es casual: refleja cómo están organizados los electrones en los átomos.
Los elementos que pertenecen al mismo grupo (columna) tienen propiedades químicas similares porque tienen la misma configuración de electrones en su capa más externa. Por ejemplo, los metales alcalinos (Grupo 1A) son todos altamente reactivos y forman compuestos similares.
Los periodos (filas) muestran una variación gradual en las propiedades. Al movernos de izquierda a derecha en un periodo, los elementos pasan de ser metales típicos a no metales, terminando con gases nobles estables.
💡 Consejo para estudiar: Cuando aprendas sobre un elemento nuevo, ubícalo en la tabla periódica. Su posición te dirá mucho sobre su comportamiento químico.
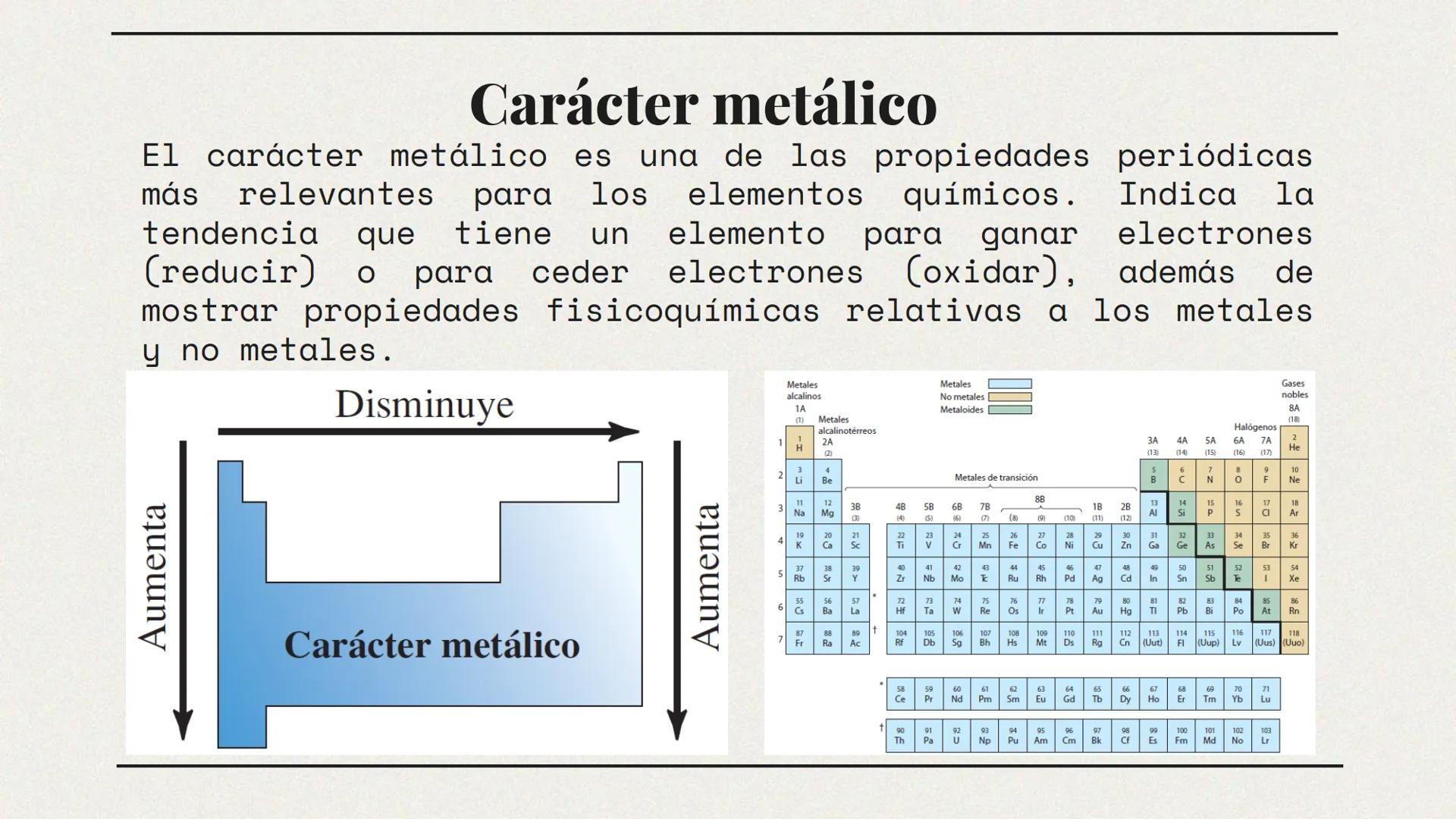
¿Has notado que algunos elementos brillan mientras otros son opacos? Esto se relaciona con su carácter metálico, una propiedad crucial que varía sistemáticamente en la tabla periódica.
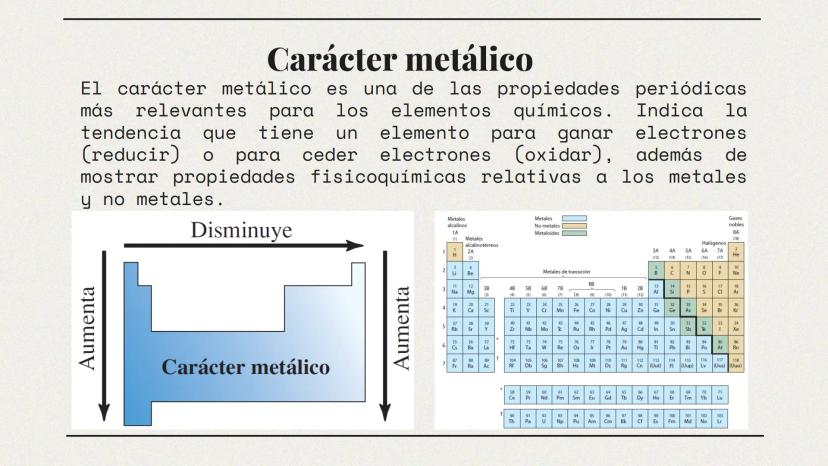
El carácter metálico indica la tendencia de un elemento a ceder electrones (oxidarse) o ganarlos (reducirse). Los elementos con alto carácter metálico, como el sodio y el potasio, ceden electrones fácilmente y exhiben propiedades típicas de los metales: conducen electricidad, tienen brillo y son maleables.
Este carácter disminuye al movernos hacia la derecha en un periodo y aumenta al descender en un grupo. Esto explica por qué el cesio (Cs) es más reactivo que el litio (Li), aunque ambos son metales alcalinos.
La comprensión del carácter metálico es fundamental para predecir cómo reaccionarán los elementos y qué tipo de compuestos formarán.
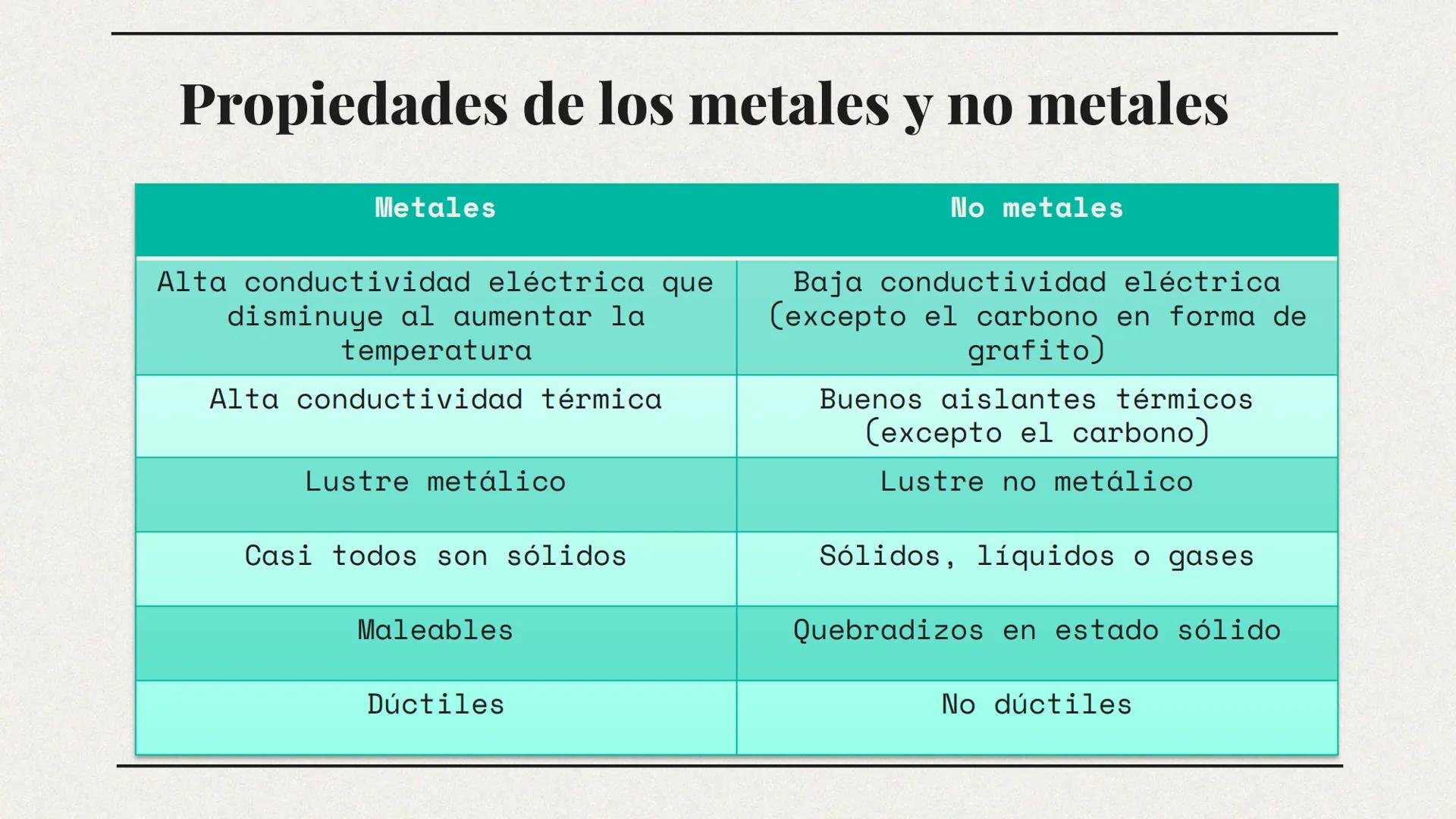
Los metales y no metales son como dos familias con características opuestas. Estas diferencias son clave para entender su comportamiento químico y sus aplicaciones.
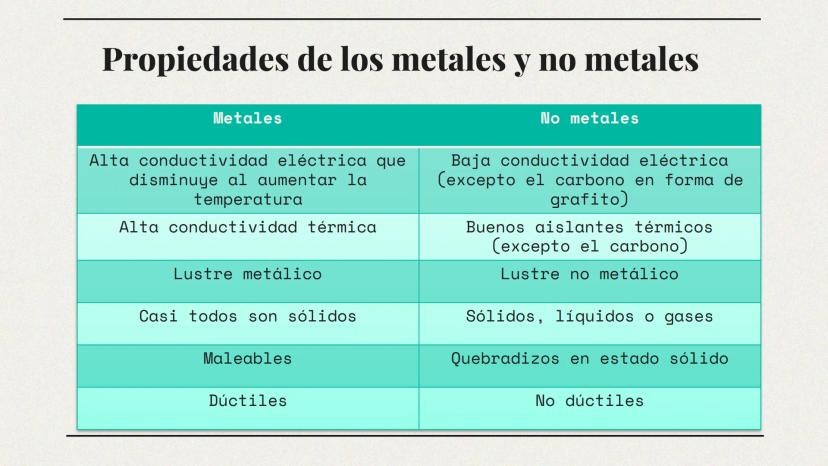
Los metales conducen muy bien la electricidad y el calor, presentan un brillo característico y son maleables (se pueden moldear en láminas). Casi todos son sólidos a temperatura ambiente, con excepciones como el mercurio. Estas propiedades explican por qué usamos cobre en cables eléctricos y aluminio en utensilios de cocina.
En contraste, los no metales generalmente son malos conductores (aislantes), no tienen brillo metálico y son quebradizos en estado sólido. Pueden encontrarse como sólidos, líquidos o gases a temperatura ambiente. El plástico, por ejemplo, es un buen aislante eléctrico por sus componentes no metálicos.
💡 Conexión con tu vida: Piensa en los objetos que te rodean. ¿Puedes identificar cuáles están hechos de metales y cuáles de no metales basándote en sus propiedades?

La estructura electrónica explica las diferencias fundamentales entre metales y no metales, determinando cómo reaccionan para formar compuestos.
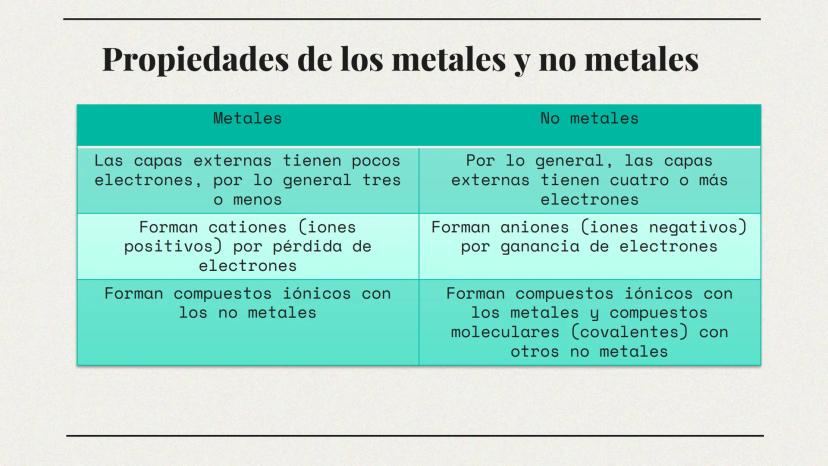
Los metales tienen pocos electrones en su capa externa (generalmente tres o menos), lo que los hace propensos a perderlos para formar cationes (iones con carga positiva). Esta tendencia explica por qué el sodio pierde fácilmente un electrón para formar Na⁺.
Los no metales, por otro lado, suelen tener cuatro o más electrones en su capa externa, por lo que prefieren ganar electrones para formar aniones (iones con carga negativa). El cloro, por ejemplo, gana un electrón para formar Cl⁻.
Estas diferencias explican por qué los metales y no metales se atraen tan fuertemente, formando compuestos iónicos como el NaCl (sal común), mientras que los no metales entre sí forman compuestos moleculares con enlaces covalentes, como el CO₂.
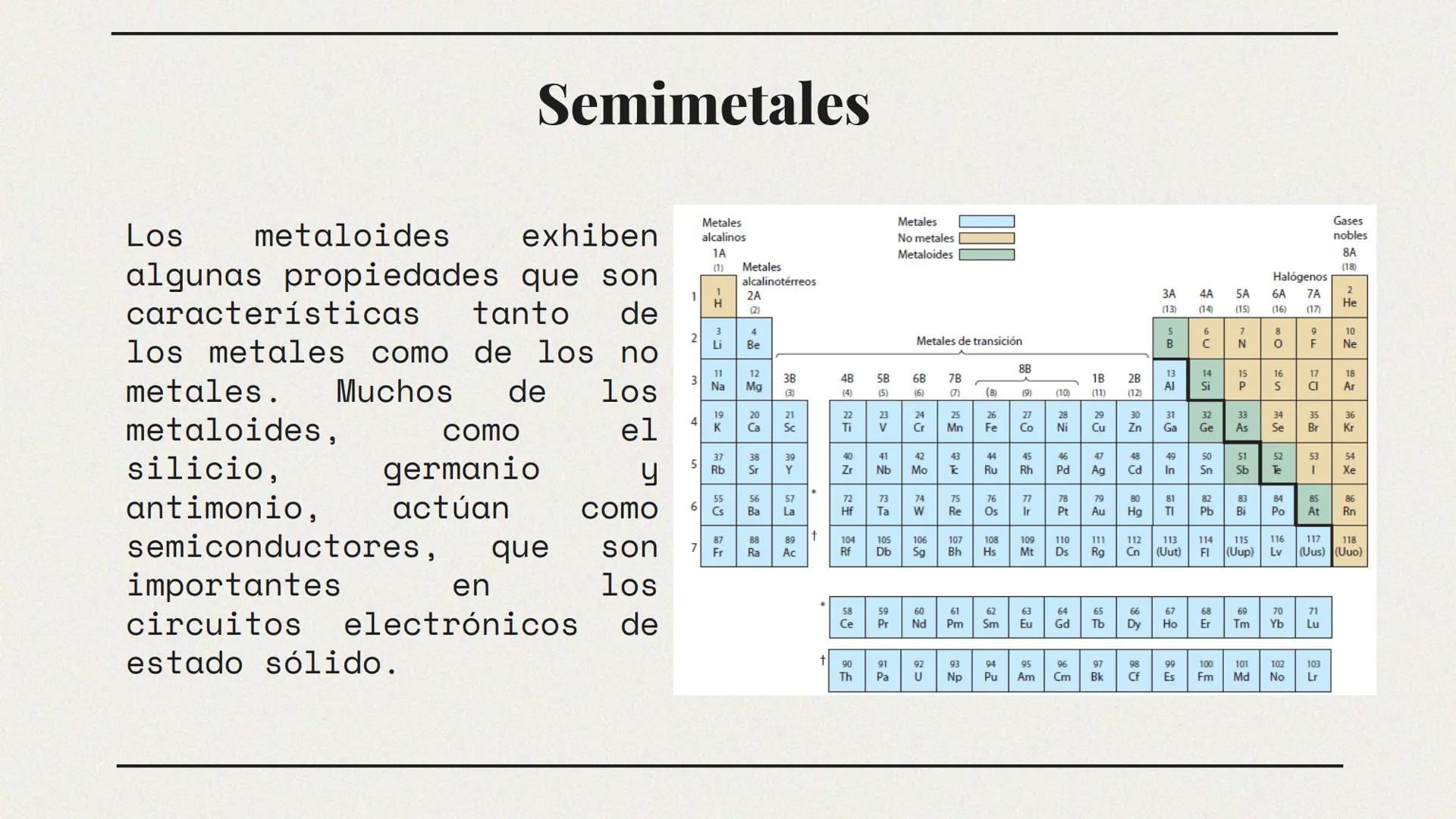
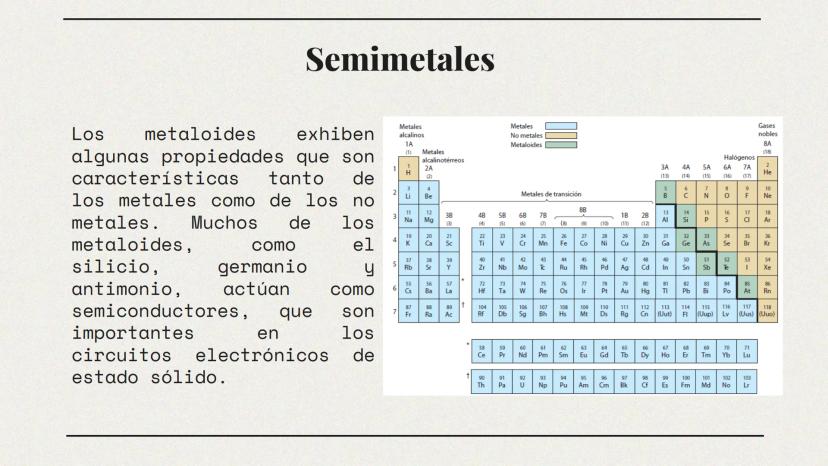
Entre los mundos de los metales y no metales existe una fascinante zona fronteriza: los semimetales o metaloides. Estos elementos híbridos son los camaleones de la tabla periódica.
Los semimetales exhiben características mixtas: algunas propiedades típicas de los metales y otras de los no metales. Se ubican en una diagonal que zigzaguea desde el boro (B) hasta el astato (At) en la tabla periódica, actuando como una línea divisoria entre metales y no metales.
Lo más interesante de estos elementos es su comportamiento como semiconductores. El silicio y el germanio, por ejemplo, tienen una conductividad eléctrica intermedia que puede ser manipulada. Esta propiedad los hace indispensables en la fabricación de chips de computadora, transistores y toda la tecnología electrónica moderna.
💡 Impacto tecnológico: Sin los semimetales como el silicio, no existirían los smartphones, computadoras ni la mayoría de dispositivos electrónicos que usamos diariamente.
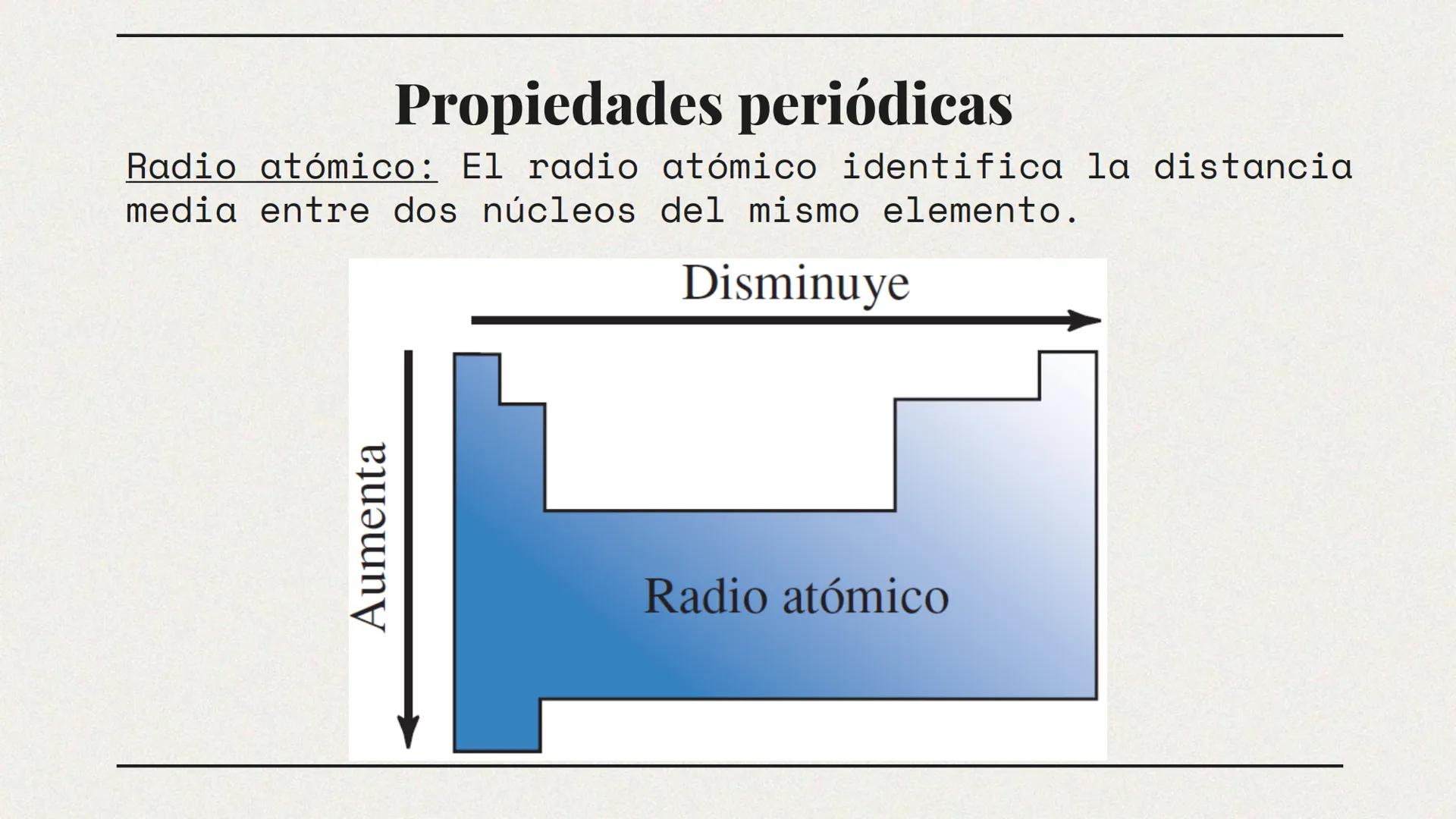
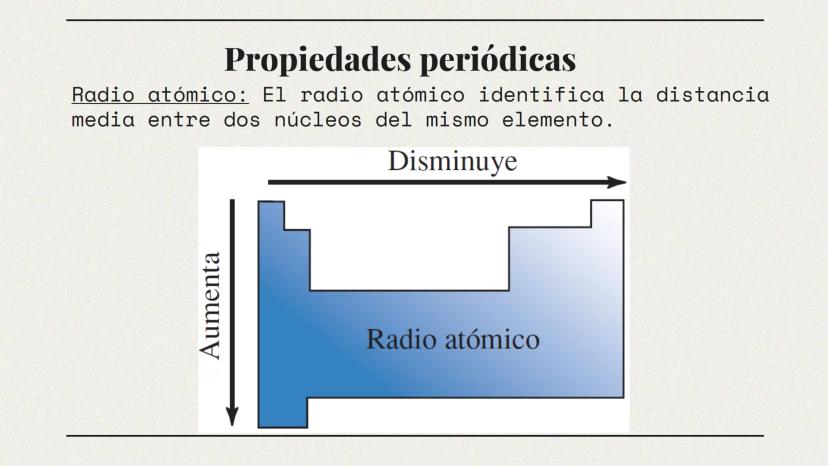
¿Has notado que los átomos de diferentes elementos tienen tamaños distintos? El radio atómico es una medida de este tamaño y varía de manera predecible en la tabla periódica.
El radio atómico se define como la distancia media entre dos núcleos del mismo elemento cuando están unidos. Esta propiedad es crucial porque afecta directamente cómo interactuarán los átomos entre sí.
En la tabla periódica, el radio atómico aumenta al descender en un grupo (columna). Esto ocurre porque se añaden nuevas capas de electrones que incrementan el tamaño. Por otro lado, disminuye al moverse de izquierda a derecha en un periodo (fila) debido a que la carga nuclear aumenta y atrae más fuertemente a los electrones.
Esta tendencia explica por qué el cesio (Cs) es uno de los átomos más grandes, mientras que el flúor (F) es uno de los más pequeños.
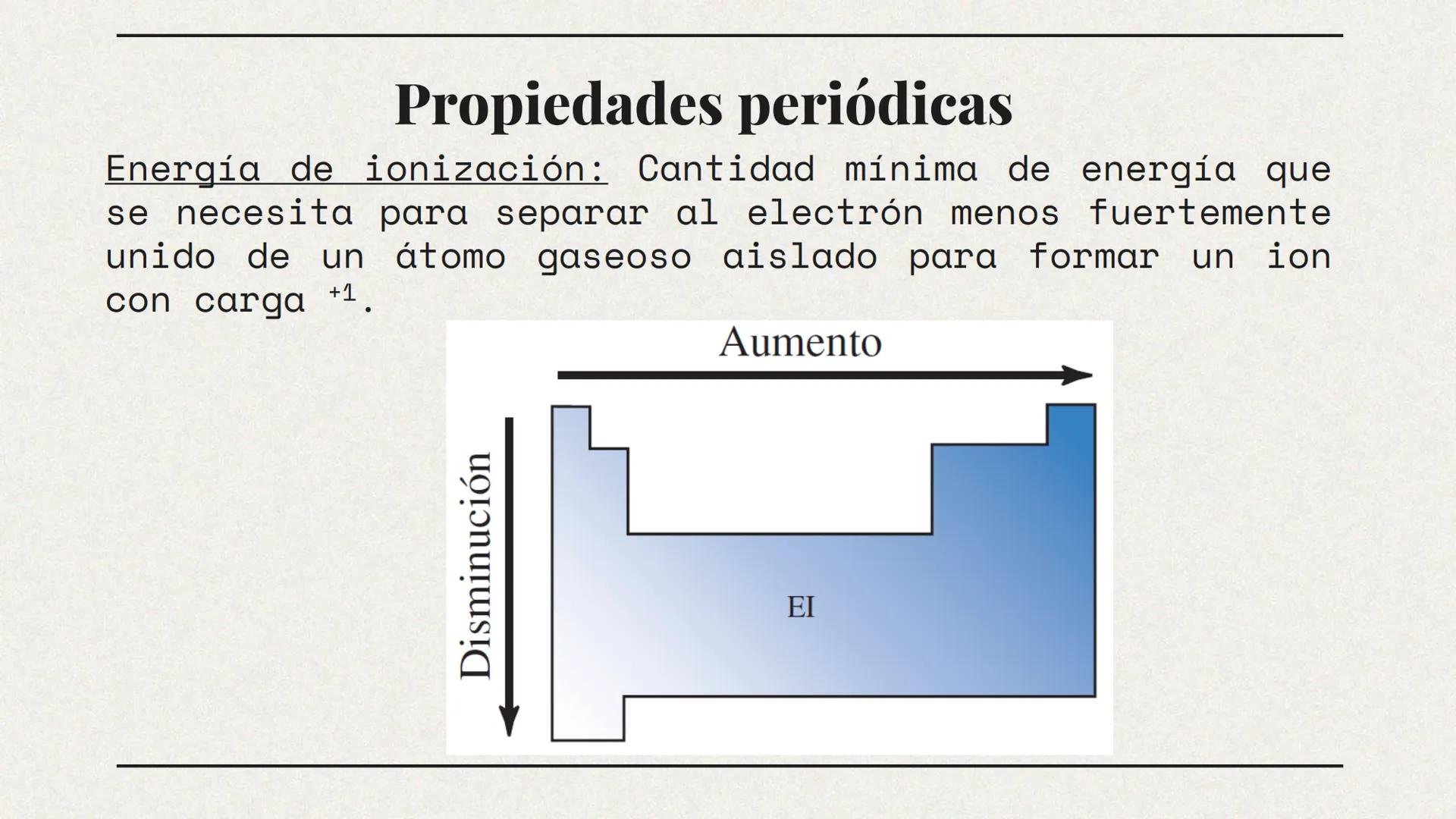
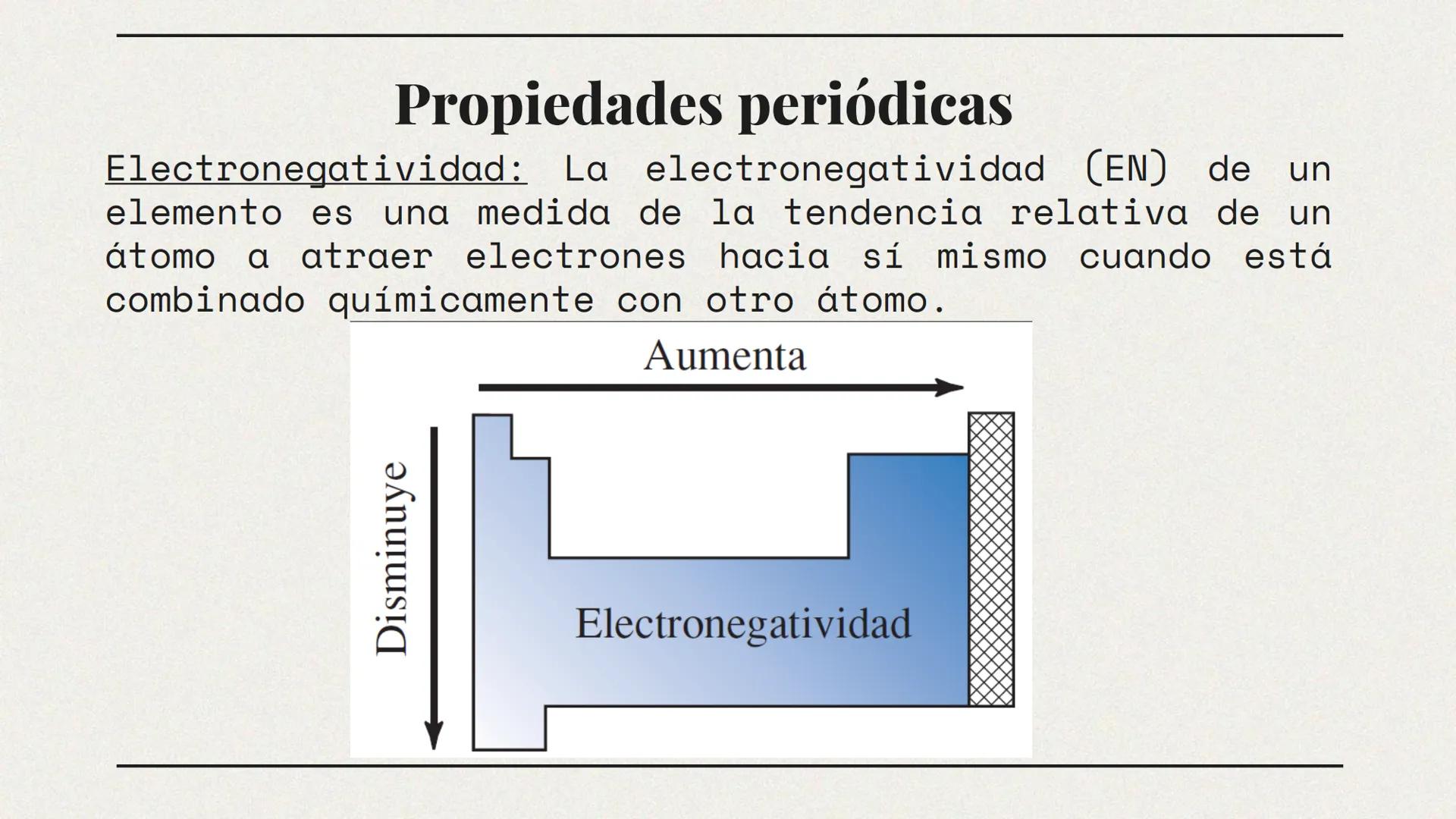








Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
Paula Solorzano
@paulasolo_vztxf
La química de los elementos y sus enlaces es fascinante porque explica cómo se forma todo lo que nos rodea. En estas notas, descubrirás cómo se organizan los elementos en la tabla periódica y comprenderás las diferentes maneras en que... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La química es la ciencia que estudia la composición, estructura y propiedades de la materia. Esta asignatura es fundamental para entender los procesos que ocurren en nuestro entorno cotidiano.
Las notas que estás a punto de estudiar cubren conceptos esenciales como la tabla periódica y los enlaces químicos, herramientas fundamentales para cualquier estudiante de química.
💡 ¡Recuerda! La química no solo se trata de fórmulas y ecuaciones, sino de entender cómo funciona el mundo a nivel molecular.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El enlace químico es el fenómeno que mantiene unidos a los átomos para formar moléculas o compuestos. Es uno de los conceptos más importantes en química porque explica cómo se forman las sustancias que nos rodean.
Entender los enlaces químicos nos permite comprender por qué algunas sustancias son resistentes mientras otras son frágiles, por qué algunas conducen electricidad y otras no, y cómo ocurren las reacciones químicas.
En las próximas páginas estudiaremos cómo se organizan los elementos y los diferentes tipos de enlaces que pueden formar entre sí.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
¿Te has preguntado cómo se organizan los más de 100 elementos conocidos? En 1869, el químico ruso Dimitri Mendeleev revolucionó la química cuando publicó un ordenamiento de los elementos conocidos en su época.
Mendeleev descubrió que las propiedades de los elementos se repetían periódicamente cuando se ordenaban según su masa atómica. Esta observación fue clave para organizar todos los elementos de manera lógica y predecible.
Su trabajo fue tan brillante que incluso dejó espacios vacíos para elementos aún no descubiertos, prediciendo correctamente sus propiedades. ¡Imagina predecir la existencia de algo que nadie ha visto nunca!
💡 Dato interesante: Mendeleev jugaba "solitario" con tarjetas que tenían información de cada elemento para encontrar patrones en sus propiedades.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La tabla de Mendeleev no era perfecta. Algunos elementos no encajaban bien en su organización basada en la masa atómica. ¿Por qué? Porque faltaba un concepto clave que se descubriría casi 50 años después.
Fue el número atómico (la cantidad de protones en el núcleo), y no la masa atómica, lo que realmente determinaba las propiedades periódicas de los elementos. Este descubrimiento llevó a establecer la ley periódica:
"Las propiedades de los elementos son funciones periódicas de sus números atómicos"
Este principio fundamental permite predecir el comportamiento químico de los elementos con solo conocer su posición en la tabla periódica, lo que la convierte en una herramienta esencial para cualquier químico.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La tabla periódica está organizada en filas horizontales (periodos) y columnas verticales (grupos). Esta estructura no es casual: refleja cómo están organizados los electrones en los átomos.
Los elementos que pertenecen al mismo grupo (columna) tienen propiedades químicas similares porque tienen la misma configuración de electrones en su capa más externa. Por ejemplo, los metales alcalinos (Grupo 1A) son todos altamente reactivos y forman compuestos similares.
Los periodos (filas) muestran una variación gradual en las propiedades. Al movernos de izquierda a derecha en un periodo, los elementos pasan de ser metales típicos a no metales, terminando con gases nobles estables.
💡 Consejo para estudiar: Cuando aprendas sobre un elemento nuevo, ubícalo en la tabla periódica. Su posición te dirá mucho sobre su comportamiento químico.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
¿Has notado que algunos elementos brillan mientras otros son opacos? Esto se relaciona con su carácter metálico, una propiedad crucial que varía sistemáticamente en la tabla periódica.
El carácter metálico indica la tendencia de un elemento a ceder electrones (oxidarse) o ganarlos (reducirse). Los elementos con alto carácter metálico, como el sodio y el potasio, ceden electrones fácilmente y exhiben propiedades típicas de los metales: conducen electricidad, tienen brillo y son maleables.
Este carácter disminuye al movernos hacia la derecha en un periodo y aumenta al descender en un grupo. Esto explica por qué el cesio (Cs) es más reactivo que el litio (Li), aunque ambos son metales alcalinos.
La comprensión del carácter metálico es fundamental para predecir cómo reaccionarán los elementos y qué tipo de compuestos formarán.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los metales y no metales son como dos familias con características opuestas. Estas diferencias son clave para entender su comportamiento químico y sus aplicaciones.
Los metales conducen muy bien la electricidad y el calor, presentan un brillo característico y son maleables (se pueden moldear en láminas). Casi todos son sólidos a temperatura ambiente, con excepciones como el mercurio. Estas propiedades explican por qué usamos cobre en cables eléctricos y aluminio en utensilios de cocina.
En contraste, los no metales generalmente son malos conductores (aislantes), no tienen brillo metálico y son quebradizos en estado sólido. Pueden encontrarse como sólidos, líquidos o gases a temperatura ambiente. El plástico, por ejemplo, es un buen aislante eléctrico por sus componentes no metálicos.
💡 Conexión con tu vida: Piensa en los objetos que te rodean. ¿Puedes identificar cuáles están hechos de metales y cuáles de no metales basándote en sus propiedades?

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La estructura electrónica explica las diferencias fundamentales entre metales y no metales, determinando cómo reaccionan para formar compuestos.
Los metales tienen pocos electrones en su capa externa (generalmente tres o menos), lo que los hace propensos a perderlos para formar cationes (iones con carga positiva). Esta tendencia explica por qué el sodio pierde fácilmente un electrón para formar Na⁺.
Los no metales, por otro lado, suelen tener cuatro o más electrones en su capa externa, por lo que prefieren ganar electrones para formar aniones (iones con carga negativa). El cloro, por ejemplo, gana un electrón para formar Cl⁻.
Estas diferencias explican por qué los metales y no metales se atraen tan fuertemente, formando compuestos iónicos como el NaCl (sal común), mientras que los no metales entre sí forman compuestos moleculares con enlaces covalentes, como el CO₂.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Entre los mundos de los metales y no metales existe una fascinante zona fronteriza: los semimetales o metaloides. Estos elementos híbridos son los camaleones de la tabla periódica.
Los semimetales exhiben características mixtas: algunas propiedades típicas de los metales y otras de los no metales. Se ubican en una diagonal que zigzaguea desde el boro (B) hasta el astato (At) en la tabla periódica, actuando como una línea divisoria entre metales y no metales.
Lo más interesante de estos elementos es su comportamiento como semiconductores. El silicio y el germanio, por ejemplo, tienen una conductividad eléctrica intermedia que puede ser manipulada. Esta propiedad los hace indispensables en la fabricación de chips de computadora, transistores y toda la tecnología electrónica moderna.
💡 Impacto tecnológico: Sin los semimetales como el silicio, no existirían los smartphones, computadoras ni la mayoría de dispositivos electrónicos que usamos diariamente.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
¿Has notado que los átomos de diferentes elementos tienen tamaños distintos? El radio atómico es una medida de este tamaño y varía de manera predecible en la tabla periódica.
El radio atómico se define como la distancia media entre dos núcleos del mismo elemento cuando están unidos. Esta propiedad es crucial porque afecta directamente cómo interactuarán los átomos entre sí.
En la tabla periódica, el radio atómico aumenta al descender en un grupo (columna). Esto ocurre porque se añaden nuevas capas de electrones que incrementan el tamaño. Por otro lado, disminuye al moverse de izquierda a derecha en un periodo (fila) debido a que la carga nuclear aumenta y atrae más fuertemente a los electrones.
Esta tendencia explica por qué el cesio (Cs) es uno de los átomos más grandes, mientras que el flúor (F) es uno de los más pequeños.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
9
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Fichas Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS