¡Hola! Vamos a explorar el fascinante mundo de los modelos... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
152
•
Actualizado Mar 24, 2026
•
maria sierra
@mariasier_l76tm
¡Hola! Vamos a explorar el fascinante mundo de los modelos... Mostrar más














Los modelos atómicos son representaciones que los científicos han creado para entender cómo están formados los átomos. Estas ideas han ido cambiando con el tiempo mientras la ciencia avanzaba con nuevos descubrimientos.
Estos modelos nos ayudan a visualizar algo tan pequeño que no podemos ver directamente, ¡incluso con los mejores microscopios!

Un modelo atómico es simplemente una explicación de cómo está estructurada la parte más pequeña de la materia. Durante mucho tiempo, se pensaba que el átomo era la porción más pequeña en que se podía dividir la materia.
Estos modelos son como mapas que nos ayudan a entender cómo funcionan los átomos, aunque nunca podamos verlos directamente con nuestros ojos.
💡 La palabra "átomo" viene del griego y significa "indivisible", aunque hoy sabemos que sí se puede dividir en partículas más pequeñas.

Todo comenzó con los griegos. Cinco siglos antes de Cristo, Demócrito propuso que la materia estaba formada por partículas indivisibles que llamó átomos. ¡Una idea revolucionaria para su época!
En 1803, John Dalton retomó esta idea y propuso que la materia se dividía en elementos y compuestos. Según él, los elementos estaban formados por átomos, mientras que los compuestos se formaban cuando estos átomos se unían en proporciones definidas.
Esta teoría fue el primer modelo atómico moderno y aunque hoy sabemos que tiene limitaciones, sentó las bases para entender la estructura de la materia.

A finales del siglo XIX, todo cambió cuando se descubrió que los átomos no eran indivisibles. En 1897, Sir Joseph Thomson descubrió el electrón, la primera partícula subatómica conocida.
Después, Hantaro Nagaoka propuso que los electrones giraban alrededor de un centro cargado positivamente, similar a como los planetas giran alrededor del Sol. Fue una idea brillante que se acercaba a la realidad.
Los experimentos en la Universidad de Manchester fueron cruciales para descubrir el núcleo del átomo. Dispararon partículas contra láminas metálicas y, según cómo se desviaban, pudieron deducir cómo se distribuía la carga eléctrica dentro del átomo.

J.J. Thomson, tras descubrir el electrón, propuso un modelo conocido como el "modelo del puding". ¿Te imaginas un pudin con pasas? ¡Así era su idea del átomo!
En este modelo, el átomo era una esfera de carga positiva (el pudin) donde los electrones de carga negativa (las pasas) estaban distribuidos uniformemente. Thomson pensaba que los electrones estaban incrustados en esta masa positiva.
Este modelo también explicaba que los electrones no estaban quietos, sino que vibraban dentro de la estructura atómica debido a la energía interna del átomo. Por eso se considera un modelo dinámico, aunque muy diferente a lo que conocemos hoy.
🔍 ¡Curiosidad! El modelo de Thomson fue revolucionario porque fue el primero en reconocer que el átomo tenía partes más pequeñas con cargas eléctricas diferentes.

Jean Baptiste Perrin modificó el modelo de Thomson al sugerir que las cargas negativas (los electrones) se encontraban fuera del "pudin" positivo, no incrustadas en él como pensaba Thomson.
En 1895, Perrin confirmó que los rayos catódicos (que luego se identificaron como electrones) depositaban carga en un electroscopio. Este experimento fue crucial para entender que estábamos tratando con partículas cargadas.
Por esta misma época, Thomson se interesó en medir la velocidad de estas partículas, lo que eventualmente lo llevaría a identificar el electrón como una partícula subatómica.

En 1911, Ernest Rutherford propuso un nuevo modelo basado en su famoso "experimento de la lámina de oro". Disparó partículas alfa (con carga positiva) contra una finísima lámina de oro y observó cómo se desviaban.
Según el modelo de Rutherford, el átomo tiene dos partes principales: el núcleo y la corteza. El núcleo es muy pequeño pero concentra toda la carga positiva y casi toda la masa del átomo.
La carga positiva del núcleo es lo que hacía que algunas partículas alfa se desviaran al acercarse, ya que cargas iguales se repelen entre sí.
💥 ¡Imagínate la sorpresa de Rutherford! Esperaba que todas las partículas atravesaran la lámina sin desviarse, pero algunas rebotaban como si hubieran chocado contra algo muy denso.
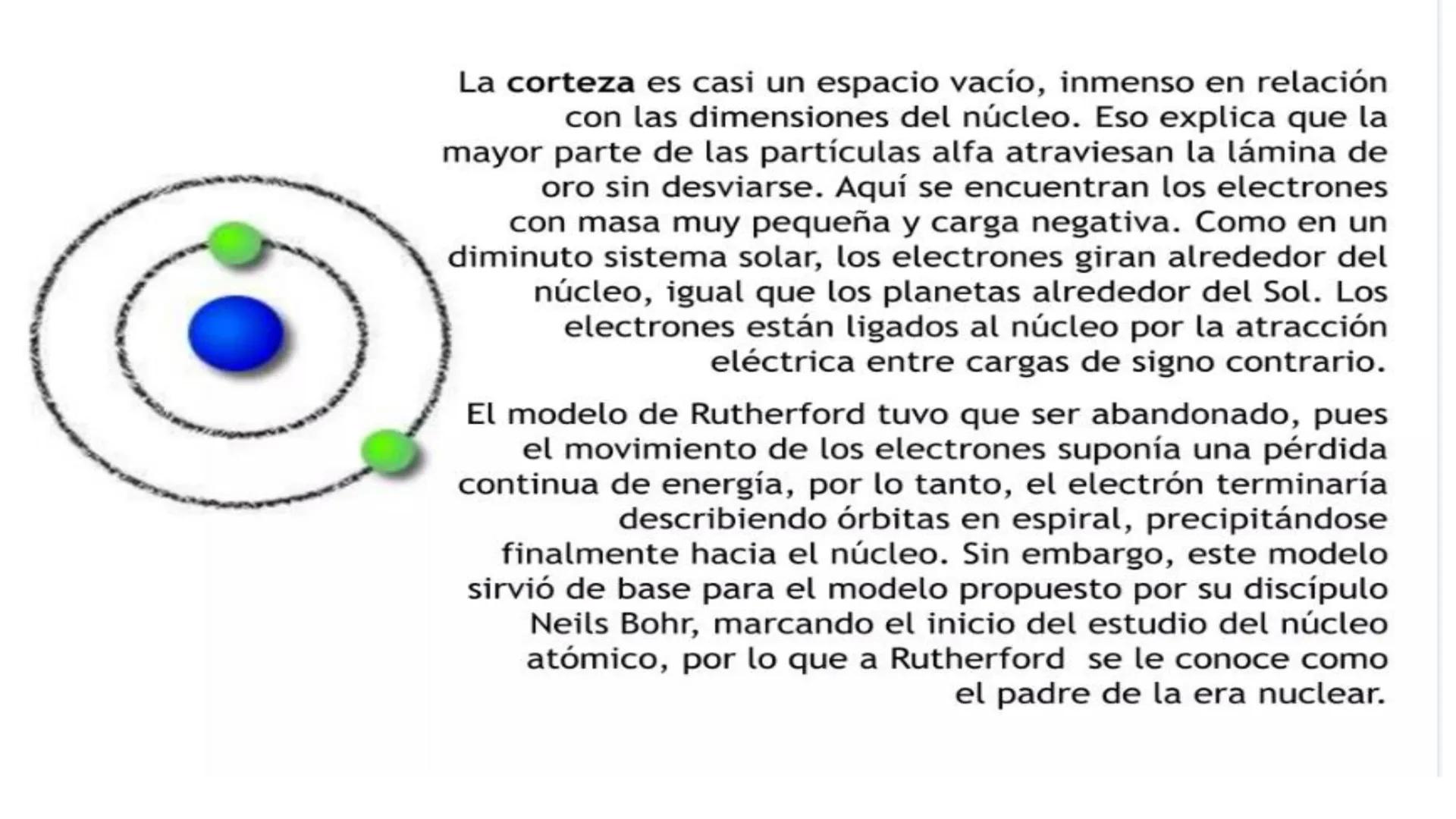
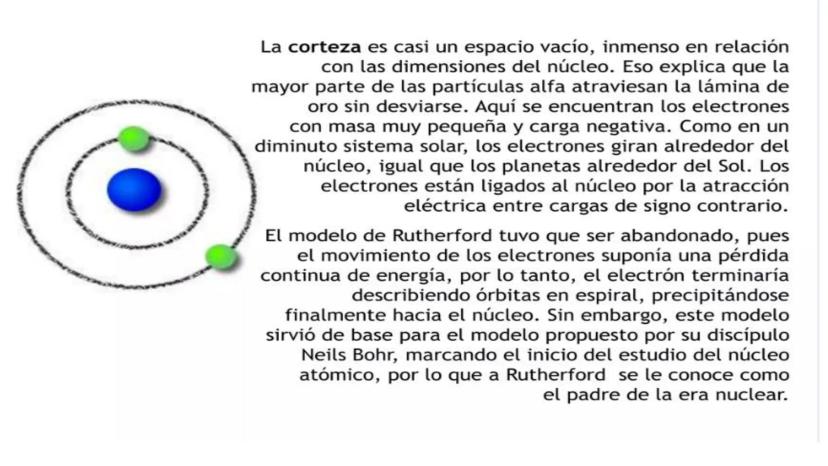
La corteza, según Rutherford, es casi un espacio vacío donde se encuentran los electrones girando alrededor del núcleo, similar a los planetas alrededor del Sol. Esto explicaba por qué la mayoría de las partículas alfa atravesaban la lámina sin desviarse.
Los electrones, con su carga negativa, se mantenían en órbita alrededor del núcleo debido a la atracción eléctrica entre cargas opuestas.
Sin embargo, este modelo tenía un problema grave: según las leyes de la física clásica, los electrones en movimiento deberían perder energía continuamente y caer en espiral hacia el núcleo. ¡Pero esto no ocurre en la realidad!
A pesar de este problema, el modelo de Rutherford fue fundamental para el desarrollo de la física nuclear, tanto que se le conoce como el "padre de la era nuclear".

El físico danés Niels Bohr mejoró el modelo de Rutherford para resolver sus problemas. Propuso que los electrones giran a grandes velocidades alrededor del núcleo, pero solo en ciertas órbitas permitidas con niveles de energía específicos.
Según Bohr, un electrón no puede estar en cualquier parte: solo puede ocupar ciertas órbitas circulares con energías fijas. Para cambiar de órbita, el electrón necesita absorber o emitir energía exactamente igual a la diferencia entre los niveles.
Este modelo explicaba perfectamente el espectro de líneas del hidrógeno (los colores específicos que emite cuando se calienta). Aunque el modelo se ha refinado con el tiempo, sentó las bases de la física nuclear moderna.
🌟 ¡Dato interesante! El modelo de Bohr explica por qué los materiales emiten colores específicos cuando se calientan: son los electrones saltando entre niveles de energía.

Bohr se centró específicamente en el átomo de hidrógeno, el más simple con un protón en el núcleo y un electrón girando a su alrededor. Su objetivo era explicar dos cosas que nadie había podido explicar antes: la estabilidad de la materia y los espectros de emisión.
Su modelo combinaba ideas del modelo de Rutherford con los conceptos revolucionarios de la física cuántica que habían propuesto Max Planck y Albert Einstein años antes.
A pesar de sus limitaciones (funciona muy bien para el hidrógeno pero no tan bien para otros elementos), el modelo de Bohr sigue siendo útil hoy en día como una manera simplificada de entender la estructura atómica.
Muchas de las imágenes de átomos que ves en tus libros escolares están basadas en este modelo, con los electrones girando en órbitas definidas alrededor del núcleo.



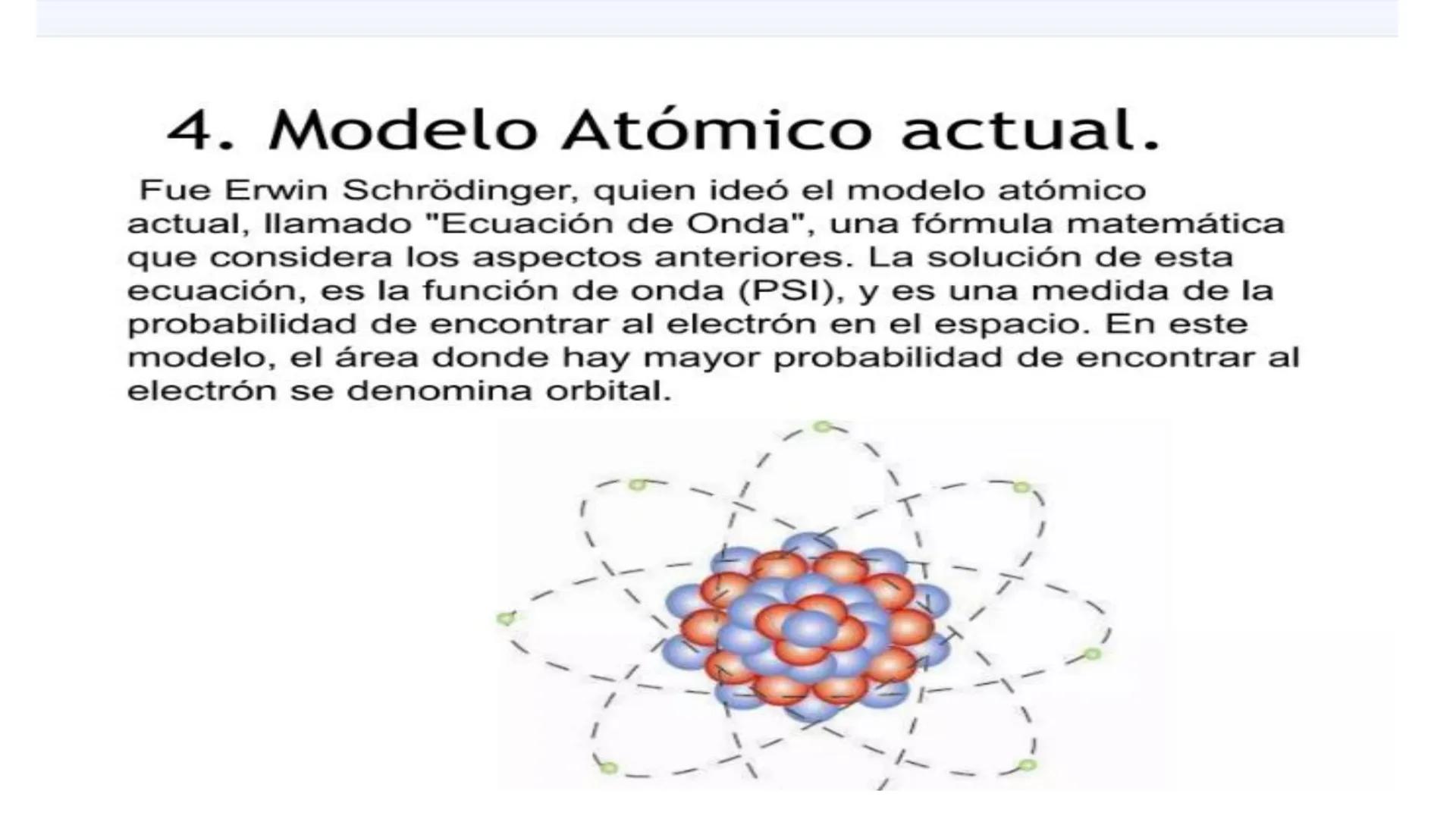

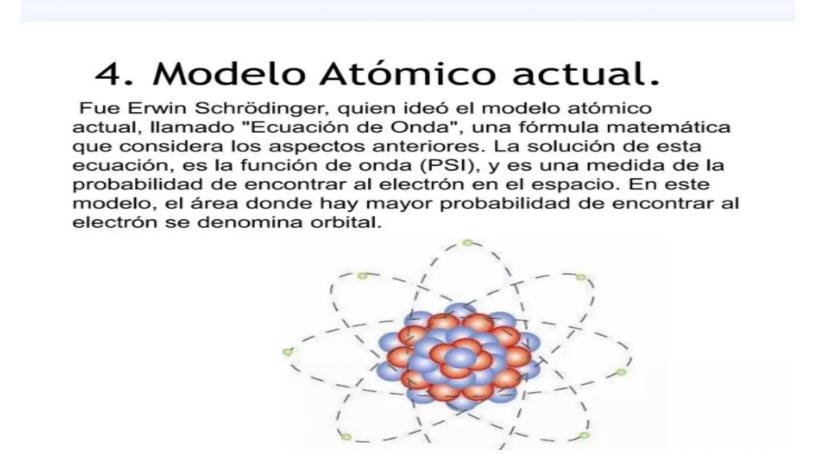
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
maria sierra
@mariasier_l76tm
¡Hola! Vamos a explorar el fascinante mundo de los modelos atómicos. Estos modelos nos ayudan a entender cómo está formada la materia que nos rodea y cómo ha evolucionado nuestra comprensión del átomo a través del tiempo.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los modelos atómicos son representaciones que los científicos han creado para entender cómo están formados los átomos. Estas ideas han ido cambiando con el tiempo mientras la ciencia avanzaba con nuevos descubrimientos.
Estos modelos nos ayudan a visualizar algo tan pequeño que no podemos ver directamente, ¡incluso con los mejores microscopios!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Un modelo atómico es simplemente una explicación de cómo está estructurada la parte más pequeña de la materia. Durante mucho tiempo, se pensaba que el átomo era la porción más pequeña en que se podía dividir la materia.
Estos modelos son como mapas que nos ayudan a entender cómo funcionan los átomos, aunque nunca podamos verlos directamente con nuestros ojos.
💡 La palabra "átomo" viene del griego y significa "indivisible", aunque hoy sabemos que sí se puede dividir en partículas más pequeñas.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Todo comenzó con los griegos. Cinco siglos antes de Cristo, Demócrito propuso que la materia estaba formada por partículas indivisibles que llamó átomos. ¡Una idea revolucionaria para su época!
En 1803, John Dalton retomó esta idea y propuso que la materia se dividía en elementos y compuestos. Según él, los elementos estaban formados por átomos, mientras que los compuestos se formaban cuando estos átomos se unían en proporciones definidas.
Esta teoría fue el primer modelo atómico moderno y aunque hoy sabemos que tiene limitaciones, sentó las bases para entender la estructura de la materia.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
A finales del siglo XIX, todo cambió cuando se descubrió que los átomos no eran indivisibles. En 1897, Sir Joseph Thomson descubrió el electrón, la primera partícula subatómica conocida.
Después, Hantaro Nagaoka propuso que los electrones giraban alrededor de un centro cargado positivamente, similar a como los planetas giran alrededor del Sol. Fue una idea brillante que se acercaba a la realidad.
Los experimentos en la Universidad de Manchester fueron cruciales para descubrir el núcleo del átomo. Dispararon partículas contra láminas metálicas y, según cómo se desviaban, pudieron deducir cómo se distribuía la carga eléctrica dentro del átomo.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
J.J. Thomson, tras descubrir el electrón, propuso un modelo conocido como el "modelo del puding". ¿Te imaginas un pudin con pasas? ¡Así era su idea del átomo!
En este modelo, el átomo era una esfera de carga positiva (el pudin) donde los electrones de carga negativa (las pasas) estaban distribuidos uniformemente. Thomson pensaba que los electrones estaban incrustados en esta masa positiva.
Este modelo también explicaba que los electrones no estaban quietos, sino que vibraban dentro de la estructura atómica debido a la energía interna del átomo. Por eso se considera un modelo dinámico, aunque muy diferente a lo que conocemos hoy.
🔍 ¡Curiosidad! El modelo de Thomson fue revolucionario porque fue el primero en reconocer que el átomo tenía partes más pequeñas con cargas eléctricas diferentes.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Jean Baptiste Perrin modificó el modelo de Thomson al sugerir que las cargas negativas (los electrones) se encontraban fuera del "pudin" positivo, no incrustadas en él como pensaba Thomson.
En 1895, Perrin confirmó que los rayos catódicos (que luego se identificaron como electrones) depositaban carga en un electroscopio. Este experimento fue crucial para entender que estábamos tratando con partículas cargadas.
Por esta misma época, Thomson se interesó en medir la velocidad de estas partículas, lo que eventualmente lo llevaría a identificar el electrón como una partícula subatómica.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
En 1911, Ernest Rutherford propuso un nuevo modelo basado en su famoso "experimento de la lámina de oro". Disparó partículas alfa (con carga positiva) contra una finísima lámina de oro y observó cómo se desviaban.
Según el modelo de Rutherford, el átomo tiene dos partes principales: el núcleo y la corteza. El núcleo es muy pequeño pero concentra toda la carga positiva y casi toda la masa del átomo.
La carga positiva del núcleo es lo que hacía que algunas partículas alfa se desviaran al acercarse, ya que cargas iguales se repelen entre sí.
💥 ¡Imagínate la sorpresa de Rutherford! Esperaba que todas las partículas atravesaran la lámina sin desviarse, pero algunas rebotaban como si hubieran chocado contra algo muy denso.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La corteza, según Rutherford, es casi un espacio vacío donde se encuentran los electrones girando alrededor del núcleo, similar a los planetas alrededor del Sol. Esto explicaba por qué la mayoría de las partículas alfa atravesaban la lámina sin desviarse.
Los electrones, con su carga negativa, se mantenían en órbita alrededor del núcleo debido a la atracción eléctrica entre cargas opuestas.
Sin embargo, este modelo tenía un problema grave: según las leyes de la física clásica, los electrones en movimiento deberían perder energía continuamente y caer en espiral hacia el núcleo. ¡Pero esto no ocurre en la realidad!
A pesar de este problema, el modelo de Rutherford fue fundamental para el desarrollo de la física nuclear, tanto que se le conoce como el "padre de la era nuclear".

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El físico danés Niels Bohr mejoró el modelo de Rutherford para resolver sus problemas. Propuso que los electrones giran a grandes velocidades alrededor del núcleo, pero solo en ciertas órbitas permitidas con niveles de energía específicos.
Según Bohr, un electrón no puede estar en cualquier parte: solo puede ocupar ciertas órbitas circulares con energías fijas. Para cambiar de órbita, el electrón necesita absorber o emitir energía exactamente igual a la diferencia entre los niveles.
Este modelo explicaba perfectamente el espectro de líneas del hidrógeno (los colores específicos que emite cuando se calienta). Aunque el modelo se ha refinado con el tiempo, sentó las bases de la física nuclear moderna.
🌟 ¡Dato interesante! El modelo de Bohr explica por qué los materiales emiten colores específicos cuando se calientan: son los electrones saltando entre niveles de energía.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Bohr se centró específicamente en el átomo de hidrógeno, el más simple con un protón en el núcleo y un electrón girando a su alrededor. Su objetivo era explicar dos cosas que nadie había podido explicar antes: la estabilidad de la materia y los espectros de emisión.
Su modelo combinaba ideas del modelo de Rutherford con los conceptos revolucionarios de la física cuántica que habían propuesto Max Planck y Albert Einstein años antes.
A pesar de sus limitaciones (funciona muy bien para el hidrógeno pero no tan bien para otros elementos), el modelo de Bohr sigue siendo útil hoy en día como una manera simplificada de entender la estructura atómica.
Muchas de las imágenes de átomos que ves en tus libros escolares están basadas en este modelo, con los electrones girando en órbitas definidas alrededor del núcleo.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
1
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Fichas Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS