¡Las proteínas son literalmente la maquinaria de la vida! Son... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
58
•
Actualizado May 15, 2026
•
Daya
@daya_d6k31
¡Las proteínas son literalmente la maquinaria de la vida! Son... Mostrar más

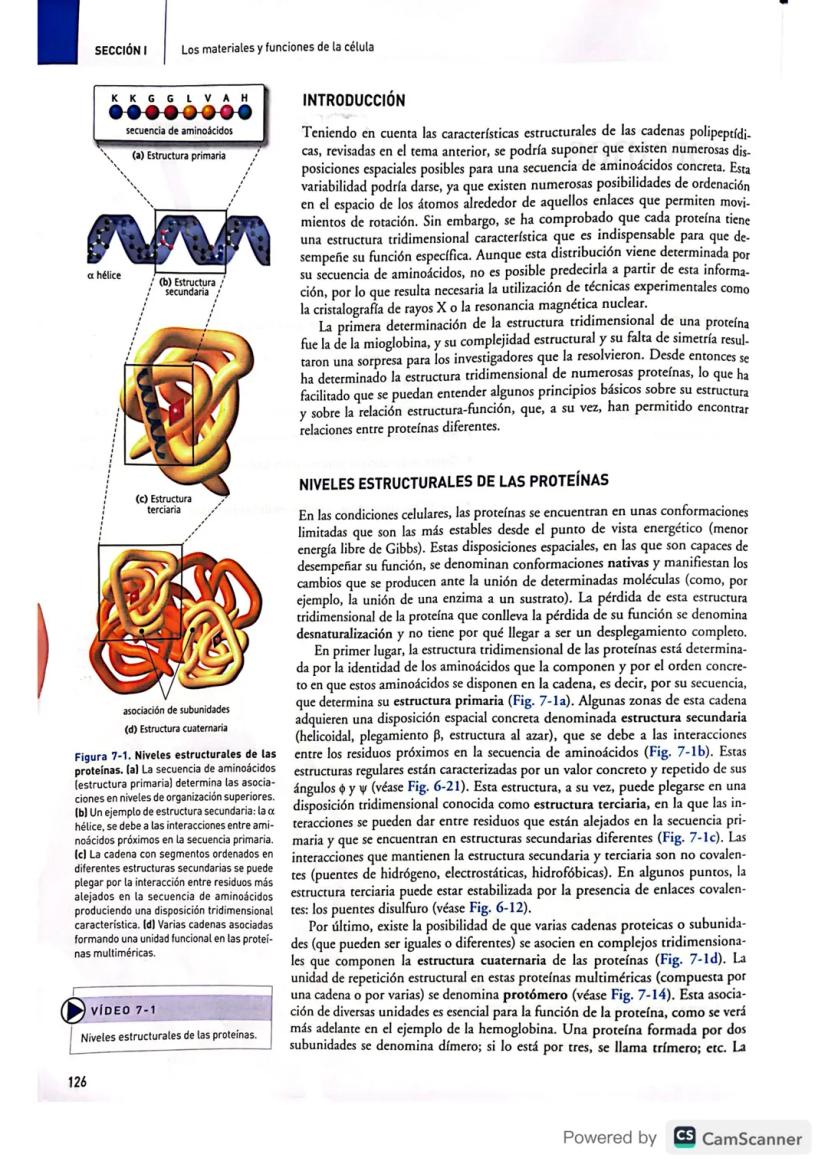
















Las proteínas son moléculas fascinantes que necesitan una forma específica para trabajar bien. Piénsalo así: cada proteína es como una llave única que solo encaja en su cerradura correspondiente.
Lo más increíble es que aunque una secuencia de aminoácidos podría formar millones de formas diferentes, cada proteína siempre adopta una estructura tridimensional característica. Esta forma específica es absolutamente necesaria para que pueda hacer su trabajo.
Para descubrir cómo se ve realmente una proteína, los científicos usan técnicas súper avanzadas como la cristalografía de rayos X. La primera proteína que lograron "fotografiar" así fue la mioglobina, y los investigadores quedaron sorprendidos por su complejidad.
💡 Dato curioso: Aunque la secuencia de aminoácidos determina la forma de la proteína, ¡todavía no podemos predecir la estructura solo mirando la secuencia!
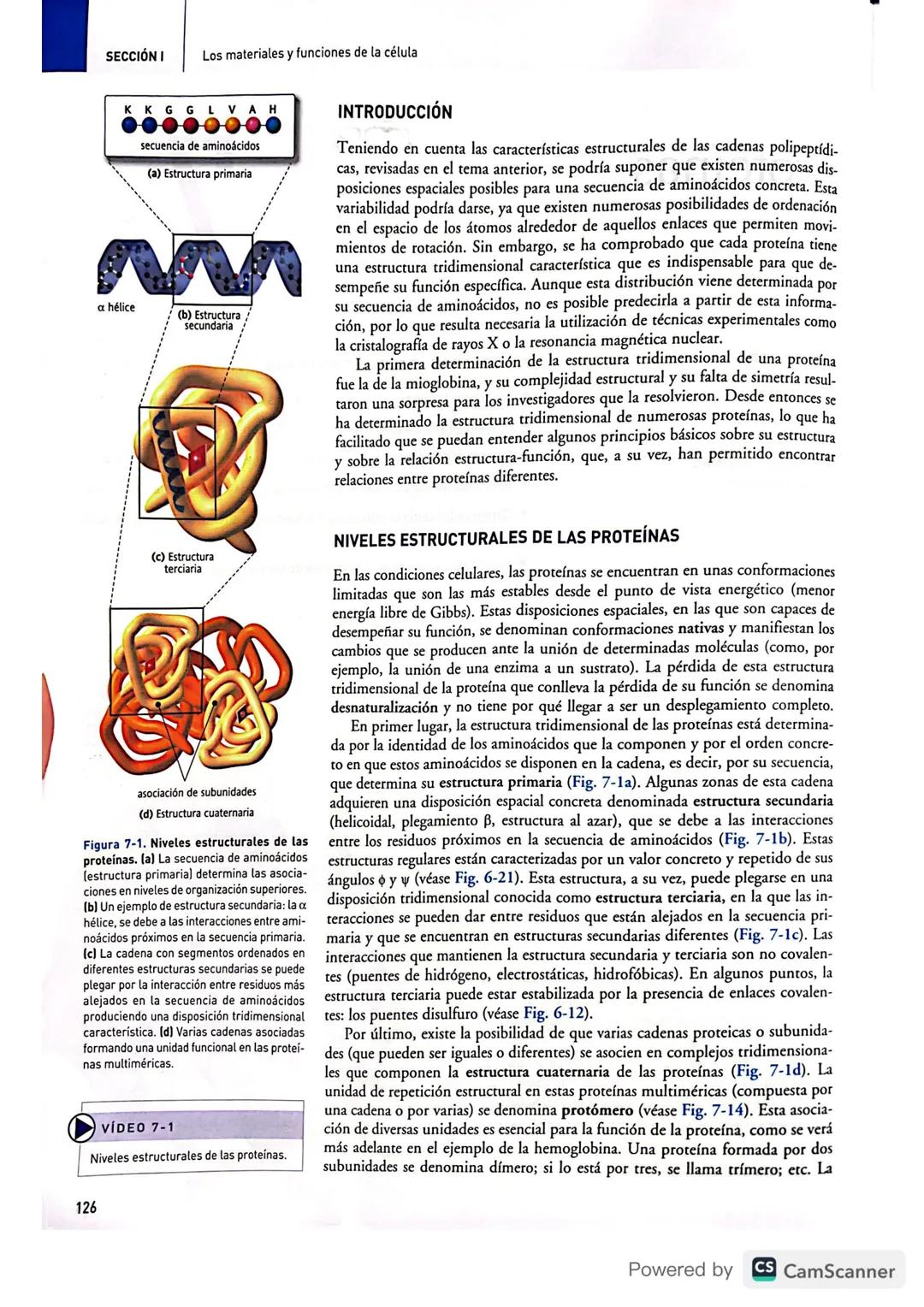
Las proteínas se organizan como edificios de cuatro pisos. La estructura primaria es la secuencia de aminoácidos, como las letras de una frase. Es la base de todo lo demás.
La estructura secundaria aparece cuando partes de la cadena forman patrones regulares como hélices o láminas plegadas (lámina β). Estas formas se mantienen gracias a puentes de hidrógeno entre aminoácidos cercanos.
Luego viene la estructura terciaria: toda la proteína se pliega en una forma tridimensional específica. Aquí, aminoácidos que estaban separados en la secuencia se acercan y forman interacciones.
Finalmente, algunas proteínas tienen estructura cuaternaria: varias cadenas se juntan para formar un complejo funcional. Por ejemplo, la hemoglobina necesita cuatro subunidades para transportar oxígeno eficientemente.
💡 Recuerda: Las proteínas globulares son como pelotas solubles en agua, mientras que las fibrosas son como cables largos e insolubles.
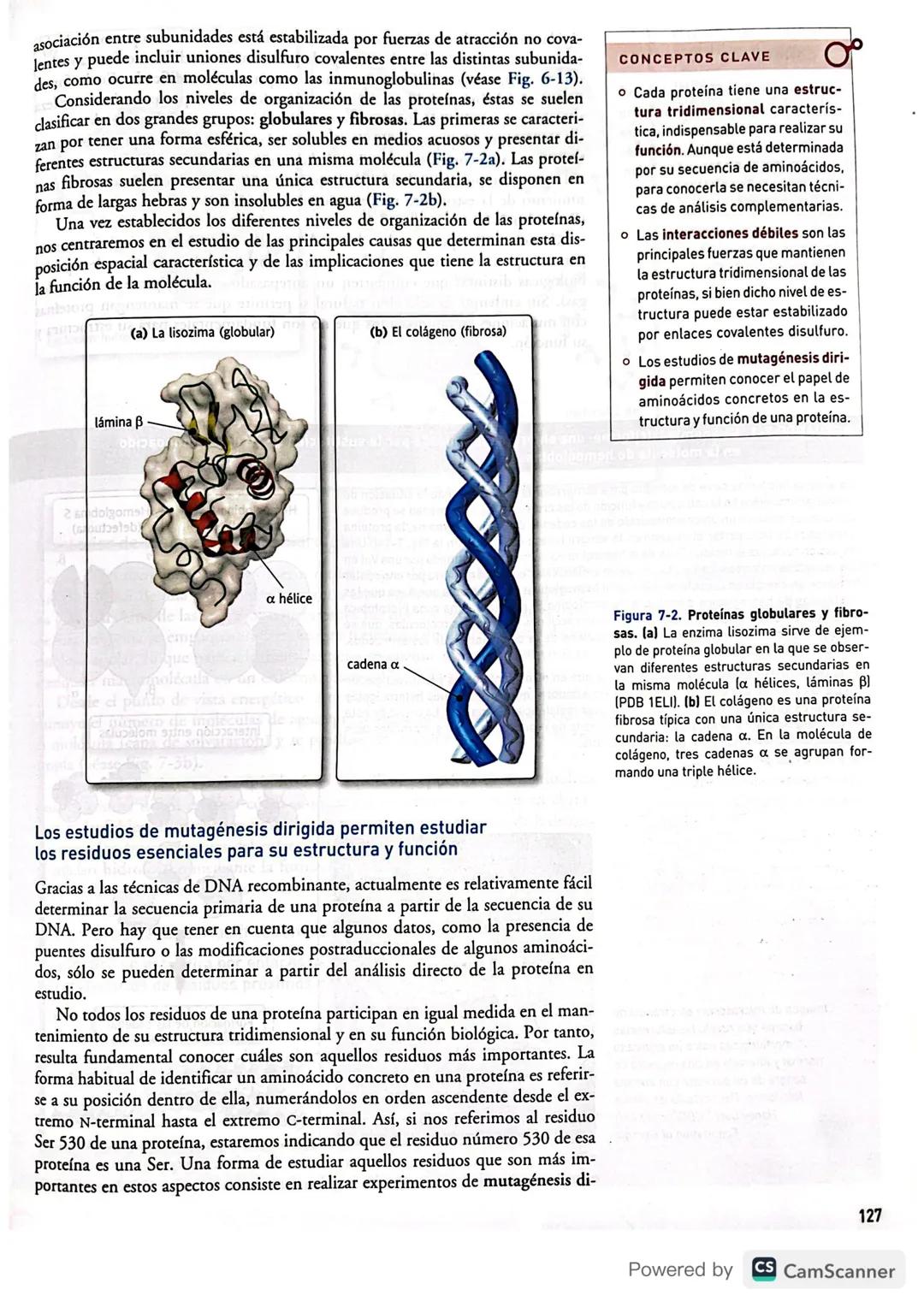
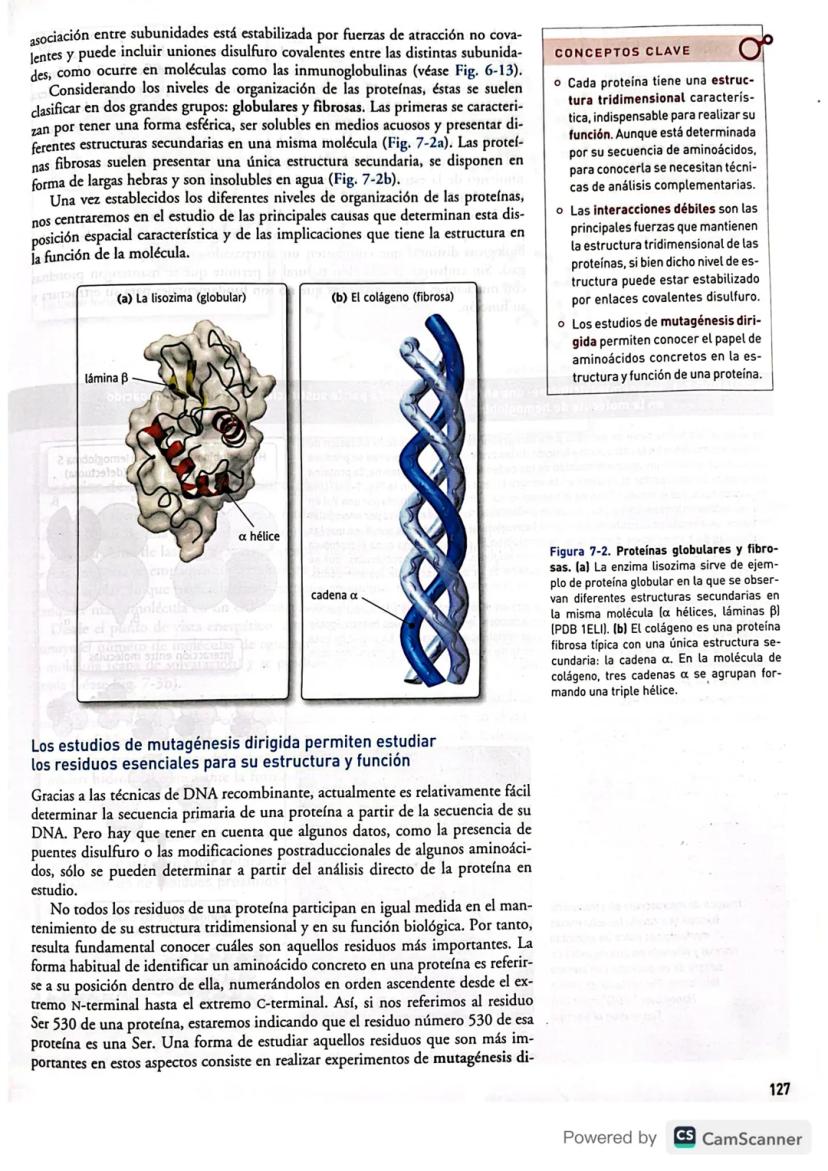
Las proteínas se clasifican en dos grandes familias. Las proteínas globulares son esféricas, solubles en agua y tienen diferentes estructuras secundarias mezcladas (como la lisozima). Las proteínas fibrosas son largas, insolubles y generalmente tienen una sola estructura secundaria dominante (como el colágeno).
La mutagénesis dirigida es una herramienta genial para entender cómo funcionan las proteínas. Los científicos cambian un aminoácido específico y observan qué pasa. Si la proteína deja de funcionar, ese aminoácido era súper importante.
Los aminoácidos más cruciales se mantienen iguales entre especies diferentes. Esto tiene sentido evolutivo: si un cambio arruina la función, esos organismos no sobreviven.
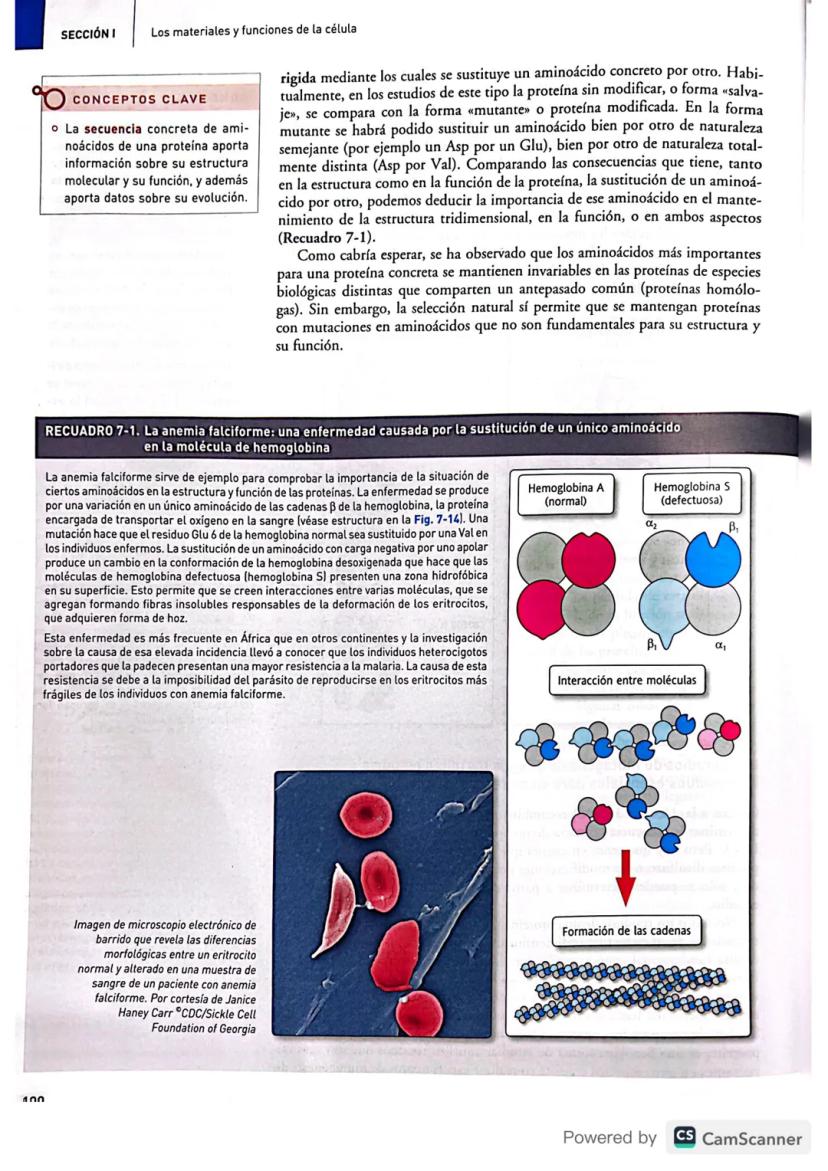
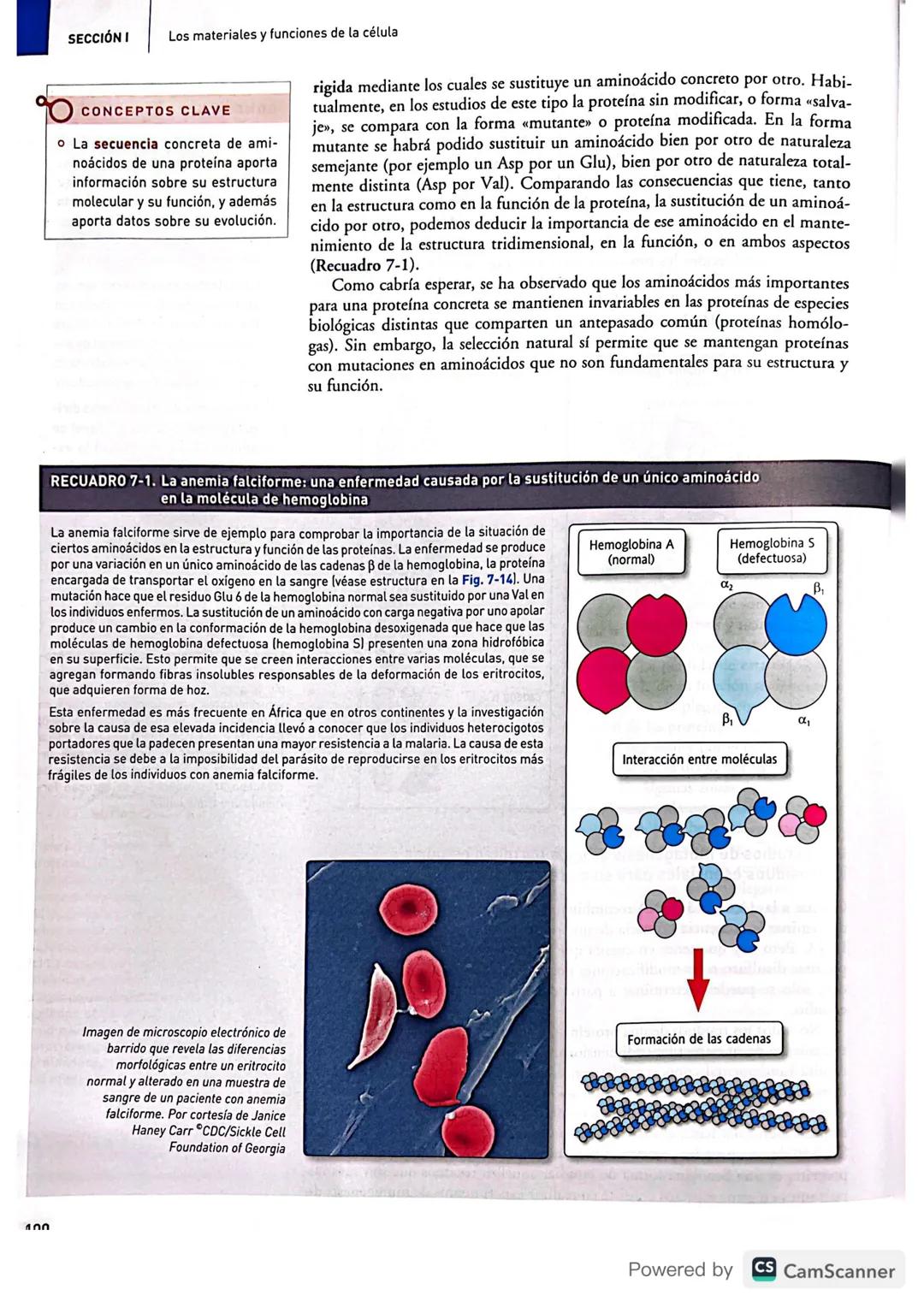
La anemia falciforme es el ejemplo perfecto de esto. Solo cambia un aminoácido (glutámico por valina) en la hemoglobina, ¡pero causa una enfermedad grave! Los glóbulos rojos se deforman como hoces y no transportan oxígeno correctamente.
💡 Conexión real: La anemia falciforme es más común en África porque paradójicamente protege contra la malaria. ¡Un efecto evolutivo inesperado!
Aquí viene algo súper inteligente de la naturaleza: las proteínas globulares esconden sus partes hidrofóbicas en el centro, como si fueran tímidas al agua. Esto forma un núcleo hidrofóbico rodeado de partes polares que sí interactúan con el agua.
¿Por qué pasa esto? Es pura termodinámica. Cuando las cadenas apolares se agrupan, liberan moléculas de agua que estaban "atrapadas" alrededor de ellas. Esto aumenta la entropía y hace que el sistema sea más estable energéticamente.
Pero aquí hay un problema: el esqueleto peptídico es polar. ¿Cómo puede estar en un núcleo hidrofóbico? La solución es brillante: estas partes polares forman puentes de hidrógeno entre ellas creando estructuras secundarias regulares .
Es como si la proteína resolviera un rompecabezas químico complejo: mantener las partes hidrofóbicas juntas mientras satisface las necesidades de unión de las partes polares.
💡 Piénsalo así: Una proteína es como una persona con chaqueta impermeable (exterior polar) y ropa interior (núcleo hidrofóbico) - cada parte está donde debe estar.

La α-hélice es como un resorte molecular súper organizado. Fue descubierta por Linus Pauling y Robert Corey, quienes calcularon la forma más estable posible para una cadena de aminoácidos.
Esta estructura es dextrógira (gira hacia la derecha) y tiene exactamente 3.6 aminoácidos por vuelta. Esto significa que los aminoácidos separados por tres o cuatro posiciones quedan muy cerca espacialmente, mientras que los separados por dos quedan en lados opuestos.
Los puentes de hidrógeno intracatenarios son clave: conectan el grupo C=O de un aminoácido con el grupo -NH del aminoácido que está cuatro posiciones después. Así, casi todos los grupos polares del esqueleto quedan "satisfechos" y no necesitan interactuar con agua.
Algo genial es que estos puentes de hidrógeno crean un dipolo eléctrico a lo largo de toda la hélice. El extremo amino queda con carga parcial positiva y el extremo carboxilo con carga negativa. ¡Esto permite interacciones específicas con otras moléculas!
💡 Datos importantes: La prolina "rompe" las α-hélices porque su estructura cíclica no permite la flexibilidad necesaria, y carece del grupo -NH para formar puentes de hidrógeno.

No todos los aminoácidos son "amigos" de la α-hélice. Los favoritos son alanina, glutámico, leucina y metionina. La glicina es problemática porque es tan pequeña que tiene demasiada flexibilidad. La prolina es la peor porque su estructura rígida introduce una "rodilla" que rompe la hélice.
Las interacciones entre cadenas laterales también importan mucho. Si dos aminoácidos con carga positiva quedan cerca , se repelen y desestabilizan la hélice. Lo mismo pasa si hay cadenas laterales muy voluminosas juntas.
En las proteínas globulares, las α-hélices suelen ubicarse en la superficie externa. Para esto necesitan una cara hidrofílica (que mire hacia el agua) y una cara hidrofóbica (que mire hacia el núcleo de la proteína).
La queratina es el ejemplo perfecto de proteína fibrosa basada en α-hélices. Forma nuestro cabello, uñas y piel. Algunos defectos en queratina causan enfermedades como epidermiólisis ampollar, donde la piel forma ampollas fácilmente.
💡 Aplicación práctica: Los tratamientos de alisado del cabello rompen temporalmente las α-hélices de la queratina para cambiar su forma.

Las láminas β son totalmente diferentes a las α-hélices. Imagínate varias tiras de papel puestas lado a lado y conectadas por puentes de hidrógeno. Eso son las hebras β formando una lámina.
Estas hebras pueden correr en la misma dirección (paralelas) o en direcciones opuestas (antiparalelas). Las antiparalelas son más estables porque los puentes de hidrógeno se forman de manera más directa.
Los giros β son súper importantes aunque parezcan simples. Con solo cuatro aminoácidos, logran cambiar la dirección de la cadena en 180°. Son como las esquinas de un edificio: pequeñas pero esenciales para la estructura total.
Estos giros suelen estar en la superficie de la proteína, donde pueden interactuar con agua. Es común encontrar prolina en estas zonas, y en el giro tipo II, el tercer aminoácido siempre es glicina.
💡 Función clave: Los giros β no solo conectan estructuras; también forman parte de sitios activos de enzimas y lugares de unión para anticuerpos.

Los motivos proteicos son como módulos prefabricados que se repiten en diferentes proteínas. Son combinaciones específicas de estructuras secundarias que tienen funciones particulares.
Un motivo súper útil es el de unión a calcio: dos α-hélices conectadas por un loop rico en ácido aspártico y glutámico. Estas cargas negativas atrapan perfectamente el Ca²⁺. Lo encuentras en proteínas como calmodulina y troponina C, que regulan la contracción muscular.
La horquilla β es el motivo más simple: dos hebras β antiparalelas conectadas por un giro β. Puede existir sola o formar parte de estructuras más complejas.
Los dominios son unidades más grandes que pueden plegarse independientemente. Muchas proteínas tienen varios dominios, cada uno con su función específica. Las proteínas de membrana típicamente tienen tres dominios: extracelular (recibe señales), transmembrana (ancla la proteína) e intracelular (transmite la señal).
💡 Piénsalo así: Los motivos son como palabras en un idioma molecular, y los dominios son como párrafos con significados completos.

La estructura terciaria es el "gran finale" del plegamiento proteico. Aquí, aminoácidos que estaban separadísimos en la secuencia se encuentran y forman interacciones específicas. Esto crea sitios de unión perfectos para otras moléculas.
El plegamiento ocurre durante la síntesis en los ribosomas, a veces con ayuda de proteínas chaperonas. Estas son como "entrenadores personales" moleculares que ayudan a las proteínas nuevas a plegarse correctamente.
La desnaturalización es cuando una proteína pierde su forma tridimensional y, por tanto, su función. Es como un origami que se desarma: la información sigue ahí, pero la forma se perdió.
Las principales causas de desnaturalización son el calor (rompe puentes de hidrógeno), cambios de pH (altera cargas), sales concentradas, disolventes apolares y detergentes. Algunos procesos son reversibles, otros no.
💡 Ejemplo cotidiano: Cuando cocinas un huevo, las proteínas de la clara se desnaturalizan por el calor. ¡Por eso cambia de transparente a blanco y no puedes "descocinarlo"!

Las encefalopatías espongiformes (como la enfermedad de las vacas locas) demuestran dramáticamente la importancia de la estructura proteica. Una proteína normal cambia de forma y se vuelve tóxica, causando daño cerebral irreversible.
En el citosol celular no se forman puentes disulfuro porque es un ambiente reductor. Los grupos -SH se mantienen libres. En contraste, en el retículo endoplasmático y fuera de la célula, el ambiente oxidante permite formar estos enlaces covalentes estabilizadores.
Los dominios transmembrana suelen tener estructura de α-hélice porque esta forma es perfecta para atravesar la bicapa lipídica. Las cadenas laterales hidrofóbicas interactúan favorablemente con las colas de los fosfolípidos.
La comprensión de la estructura proteica es fundamental para el diseño de medicamentos. Muchos fármacos funcionan encajando específicamente en sitios de unión de proteínas, como llaves en cerraduras moleculares.
💡 Perspectiva futura: La inteligencia artificial está revolucionando la predicción de estructuras proteicas, lo que acelerará enormemente el descubrimiento de nuevos medicamentos.









Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
Daya
@daya_d6k31
¡Las proteínas son literalmente la maquinaria de la vida! Son moléculas súper complejas que necesitan una estructura específica para funcionar correctamente. Imagínate: si cambias un solo aminoácido, puedes causar una enfermedad grave como la anemia falciforme.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las proteínas son moléculas fascinantes que necesitan una forma específica para trabajar bien. Piénsalo así: cada proteína es como una llave única que solo encaja en su cerradura correspondiente.
Lo más increíble es que aunque una secuencia de aminoácidos podría formar millones de formas diferentes, cada proteína siempre adopta una estructura tridimensional característica. Esta forma específica es absolutamente necesaria para que pueda hacer su trabajo.
Para descubrir cómo se ve realmente una proteína, los científicos usan técnicas súper avanzadas como la cristalografía de rayos X. La primera proteína que lograron "fotografiar" así fue la mioglobina, y los investigadores quedaron sorprendidos por su complejidad.
💡 Dato curioso: Aunque la secuencia de aminoácidos determina la forma de la proteína, ¡todavía no podemos predecir la estructura solo mirando la secuencia!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las proteínas se organizan como edificios de cuatro pisos. La estructura primaria es la secuencia de aminoácidos, como las letras de una frase. Es la base de todo lo demás.
La estructura secundaria aparece cuando partes de la cadena forman patrones regulares como hélices o láminas plegadas (lámina β). Estas formas se mantienen gracias a puentes de hidrógeno entre aminoácidos cercanos.
Luego viene la estructura terciaria: toda la proteína se pliega en una forma tridimensional específica. Aquí, aminoácidos que estaban separados en la secuencia se acercan y forman interacciones.
Finalmente, algunas proteínas tienen estructura cuaternaria: varias cadenas se juntan para formar un complejo funcional. Por ejemplo, la hemoglobina necesita cuatro subunidades para transportar oxígeno eficientemente.
💡 Recuerda: Las proteínas globulares son como pelotas solubles en agua, mientras que las fibrosas son como cables largos e insolubles.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las proteínas se clasifican en dos grandes familias. Las proteínas globulares son esféricas, solubles en agua y tienen diferentes estructuras secundarias mezcladas (como la lisozima). Las proteínas fibrosas son largas, insolubles y generalmente tienen una sola estructura secundaria dominante (como el colágeno).
La mutagénesis dirigida es una herramienta genial para entender cómo funcionan las proteínas. Los científicos cambian un aminoácido específico y observan qué pasa. Si la proteína deja de funcionar, ese aminoácido era súper importante.
Los aminoácidos más cruciales se mantienen iguales entre especies diferentes. Esto tiene sentido evolutivo: si un cambio arruina la función, esos organismos no sobreviven.
La anemia falciforme es el ejemplo perfecto de esto. Solo cambia un aminoácido (glutámico por valina) en la hemoglobina, ¡pero causa una enfermedad grave! Los glóbulos rojos se deforman como hoces y no transportan oxígeno correctamente.
💡 Conexión real: La anemia falciforme es más común en África porque paradójicamente protege contra la malaria. ¡Un efecto evolutivo inesperado!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Aquí viene algo súper inteligente de la naturaleza: las proteínas globulares esconden sus partes hidrofóbicas en el centro, como si fueran tímidas al agua. Esto forma un núcleo hidrofóbico rodeado de partes polares que sí interactúan con el agua.
¿Por qué pasa esto? Es pura termodinámica. Cuando las cadenas apolares se agrupan, liberan moléculas de agua que estaban "atrapadas" alrededor de ellas. Esto aumenta la entropía y hace que el sistema sea más estable energéticamente.
Pero aquí hay un problema: el esqueleto peptídico es polar. ¿Cómo puede estar en un núcleo hidrofóbico? La solución es brillante: estas partes polares forman puentes de hidrógeno entre ellas creando estructuras secundarias regulares .
Es como si la proteína resolviera un rompecabezas químico complejo: mantener las partes hidrofóbicas juntas mientras satisface las necesidades de unión de las partes polares.
💡 Piénsalo así: Una proteína es como una persona con chaqueta impermeable (exterior polar) y ropa interior (núcleo hidrofóbico) - cada parte está donde debe estar.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La α-hélice es como un resorte molecular súper organizado. Fue descubierta por Linus Pauling y Robert Corey, quienes calcularon la forma más estable posible para una cadena de aminoácidos.
Esta estructura es dextrógira (gira hacia la derecha) y tiene exactamente 3.6 aminoácidos por vuelta. Esto significa que los aminoácidos separados por tres o cuatro posiciones quedan muy cerca espacialmente, mientras que los separados por dos quedan en lados opuestos.
Los puentes de hidrógeno intracatenarios son clave: conectan el grupo C=O de un aminoácido con el grupo -NH del aminoácido que está cuatro posiciones después. Así, casi todos los grupos polares del esqueleto quedan "satisfechos" y no necesitan interactuar con agua.
Algo genial es que estos puentes de hidrógeno crean un dipolo eléctrico a lo largo de toda la hélice. El extremo amino queda con carga parcial positiva y el extremo carboxilo con carga negativa. ¡Esto permite interacciones específicas con otras moléculas!
💡 Datos importantes: La prolina "rompe" las α-hélices porque su estructura cíclica no permite la flexibilidad necesaria, y carece del grupo -NH para formar puentes de hidrógeno.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
No todos los aminoácidos son "amigos" de la α-hélice. Los favoritos son alanina, glutámico, leucina y metionina. La glicina es problemática porque es tan pequeña que tiene demasiada flexibilidad. La prolina es la peor porque su estructura rígida introduce una "rodilla" que rompe la hélice.
Las interacciones entre cadenas laterales también importan mucho. Si dos aminoácidos con carga positiva quedan cerca , se repelen y desestabilizan la hélice. Lo mismo pasa si hay cadenas laterales muy voluminosas juntas.
En las proteínas globulares, las α-hélices suelen ubicarse en la superficie externa. Para esto necesitan una cara hidrofílica (que mire hacia el agua) y una cara hidrofóbica (que mire hacia el núcleo de la proteína).
La queratina es el ejemplo perfecto de proteína fibrosa basada en α-hélices. Forma nuestro cabello, uñas y piel. Algunos defectos en queratina causan enfermedades como epidermiólisis ampollar, donde la piel forma ampollas fácilmente.
💡 Aplicación práctica: Los tratamientos de alisado del cabello rompen temporalmente las α-hélices de la queratina para cambiar su forma.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las láminas β son totalmente diferentes a las α-hélices. Imagínate varias tiras de papel puestas lado a lado y conectadas por puentes de hidrógeno. Eso son las hebras β formando una lámina.
Estas hebras pueden correr en la misma dirección (paralelas) o en direcciones opuestas (antiparalelas). Las antiparalelas son más estables porque los puentes de hidrógeno se forman de manera más directa.
Los giros β son súper importantes aunque parezcan simples. Con solo cuatro aminoácidos, logran cambiar la dirección de la cadena en 180°. Son como las esquinas de un edificio: pequeñas pero esenciales para la estructura total.
Estos giros suelen estar en la superficie de la proteína, donde pueden interactuar con agua. Es común encontrar prolina en estas zonas, y en el giro tipo II, el tercer aminoácido siempre es glicina.
💡 Función clave: Los giros β no solo conectan estructuras; también forman parte de sitios activos de enzimas y lugares de unión para anticuerpos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los motivos proteicos son como módulos prefabricados que se repiten en diferentes proteínas. Son combinaciones específicas de estructuras secundarias que tienen funciones particulares.
Un motivo súper útil es el de unión a calcio: dos α-hélices conectadas por un loop rico en ácido aspártico y glutámico. Estas cargas negativas atrapan perfectamente el Ca²⁺. Lo encuentras en proteínas como calmodulina y troponina C, que regulan la contracción muscular.
La horquilla β es el motivo más simple: dos hebras β antiparalelas conectadas por un giro β. Puede existir sola o formar parte de estructuras más complejas.
Los dominios son unidades más grandes que pueden plegarse independientemente. Muchas proteínas tienen varios dominios, cada uno con su función específica. Las proteínas de membrana típicamente tienen tres dominios: extracelular (recibe señales), transmembrana (ancla la proteína) e intracelular (transmite la señal).
💡 Piénsalo así: Los motivos son como palabras en un idioma molecular, y los dominios son como párrafos con significados completos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La estructura terciaria es el "gran finale" del plegamiento proteico. Aquí, aminoácidos que estaban separadísimos en la secuencia se encuentran y forman interacciones específicas. Esto crea sitios de unión perfectos para otras moléculas.
El plegamiento ocurre durante la síntesis en los ribosomas, a veces con ayuda de proteínas chaperonas. Estas son como "entrenadores personales" moleculares que ayudan a las proteínas nuevas a plegarse correctamente.
La desnaturalización es cuando una proteína pierde su forma tridimensional y, por tanto, su función. Es como un origami que se desarma: la información sigue ahí, pero la forma se perdió.
Las principales causas de desnaturalización son el calor (rompe puentes de hidrógeno), cambios de pH (altera cargas), sales concentradas, disolventes apolares y detergentes. Algunos procesos son reversibles, otros no.
💡 Ejemplo cotidiano: Cuando cocinas un huevo, las proteínas de la clara se desnaturalizan por el calor. ¡Por eso cambia de transparente a blanco y no puedes "descocinarlo"!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las encefalopatías espongiformes (como la enfermedad de las vacas locas) demuestran dramáticamente la importancia de la estructura proteica. Una proteína normal cambia de forma y se vuelve tóxica, causando daño cerebral irreversible.
En el citosol celular no se forman puentes disulfuro porque es un ambiente reductor. Los grupos -SH se mantienen libres. En contraste, en el retículo endoplasmático y fuera de la célula, el ambiente oxidante permite formar estos enlaces covalentes estabilizadores.
Los dominios transmembrana suelen tener estructura de α-hélice porque esta forma es perfecta para atravesar la bicapa lipídica. Las cadenas laterales hidrofóbicas interactúan favorablemente con las colas de los fosfolípidos.
La comprensión de la estructura proteica es fundamental para el diseño de medicamentos. Muchos fármacos funcionan encajando específicamente en sitios de unión de proteínas, como llaves en cerraduras moleculares.
💡 Perspectiva futura: La inteligencia artificial está revolucionando la predicción de estructuras proteicas, lo que acelerará enormemente el descubrimiento de nuevos medicamentos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
0
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Fichas Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS