Las enzimas son proteínas súper importantes que aceleran las reacciones... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
192
•
Actualizado May 9, 2026
•
guzmanvaleria346
@guzmanvaleria346_u2hp
Las enzimas son proteínas súper importantes que aceleran las reacciones... Mostrar más











Las enzimas son proteínas que bajan la energía de activación necesaria para que ocurran las reacciones químicas. Piénsalo así: hacen que las reacciones sean más fáciles y rápidas, pero no cambian el resultado final.
La magia ocurre cuando el sustrato (la molécula que va a cambiar) se une al sitio activo de la enzima. Esta unión forma un complejo enzima-sustrato que facilita la transformación. Un ejemplo genial es la quimiotripsina, que se encarga de degradar las proteínas que comes.
Existen dos tipos principales: las proteínas simples (solo cadenas de aminoácidos) y las proteínas conjugadas (que necesitan ayuda extra de otras moléculas para funcionar).
Dato clave: Las enzimas no se gastan en las reacciones, por eso pueden trabajar una y otra vez como verdaderos catalizadores biológicos.

Una enzima completa tiene tres componentes principales. La apoenzima es la parte proteica, como el motor principal. El cofactor es la parte no proteica que algunas enzimas necesitan para funcionar (no todas la tienen). Cuando se juntan, forman la holoenzima activa.
Los cofactores se dividen en dos grupos. Los activadores son iones metálicos como Fe²⁺, Mg²⁺, Cu²⁺, K⁺, Na⁺ y Zn²⁺. Las coenzimas son compuestos orgánicos pequeños, como las vitaminas hidrosolubles, que se unen temporal o permanentemente.
El sitio activo es una hendidura especial donde ocurre toda la acción. Aquí se rompen los enlaces del sustrato y se forman los nuevos productos. Lo increíble es que este sitio puede cambiar su forma para adaptarse mejor al sustrato, como un guante que se ajusta a tu mano.
Recuerda: Sin cofactores, muchas enzimas son como un carro sin gasolina: no pueden funcionar.

La actividad enzimática mide qué tan rápido una enzima convierte el sustrato en productos. En el laboratorio usamos la fórmula: Actividad = -Δ[S]/Δt o +Δ[P]/Δt (disminución del sustrato o aumento del producto en el tiempo).
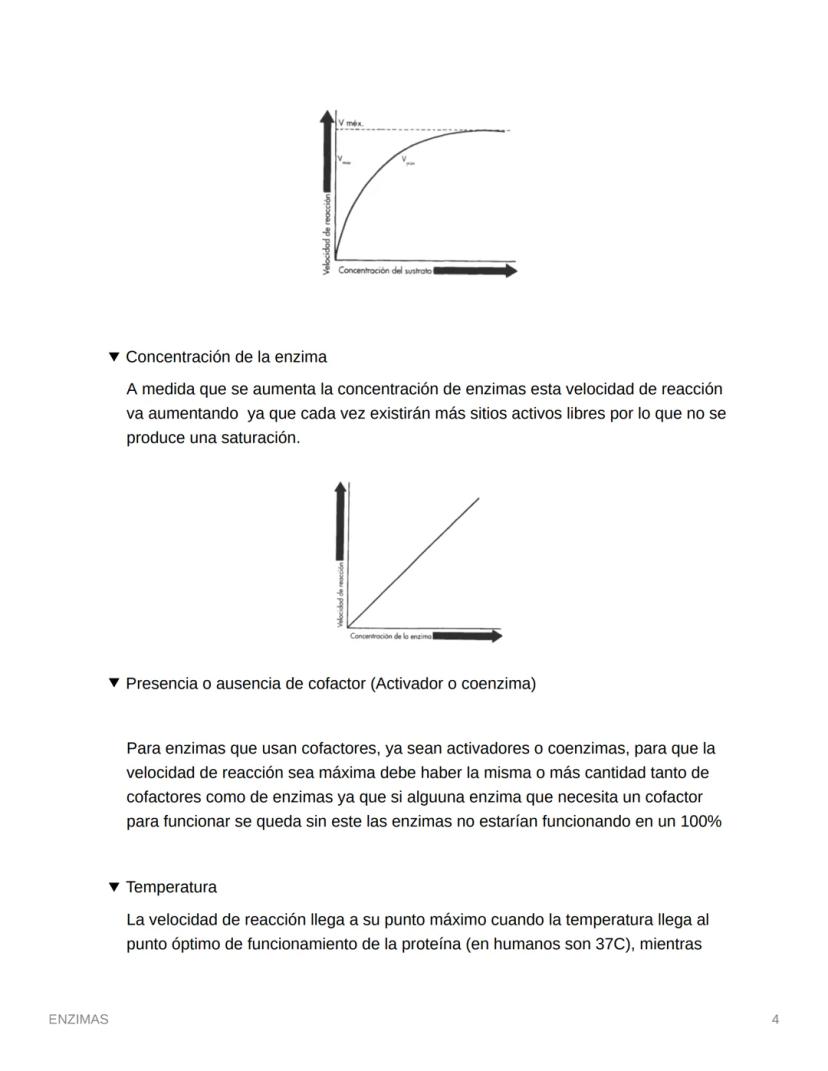
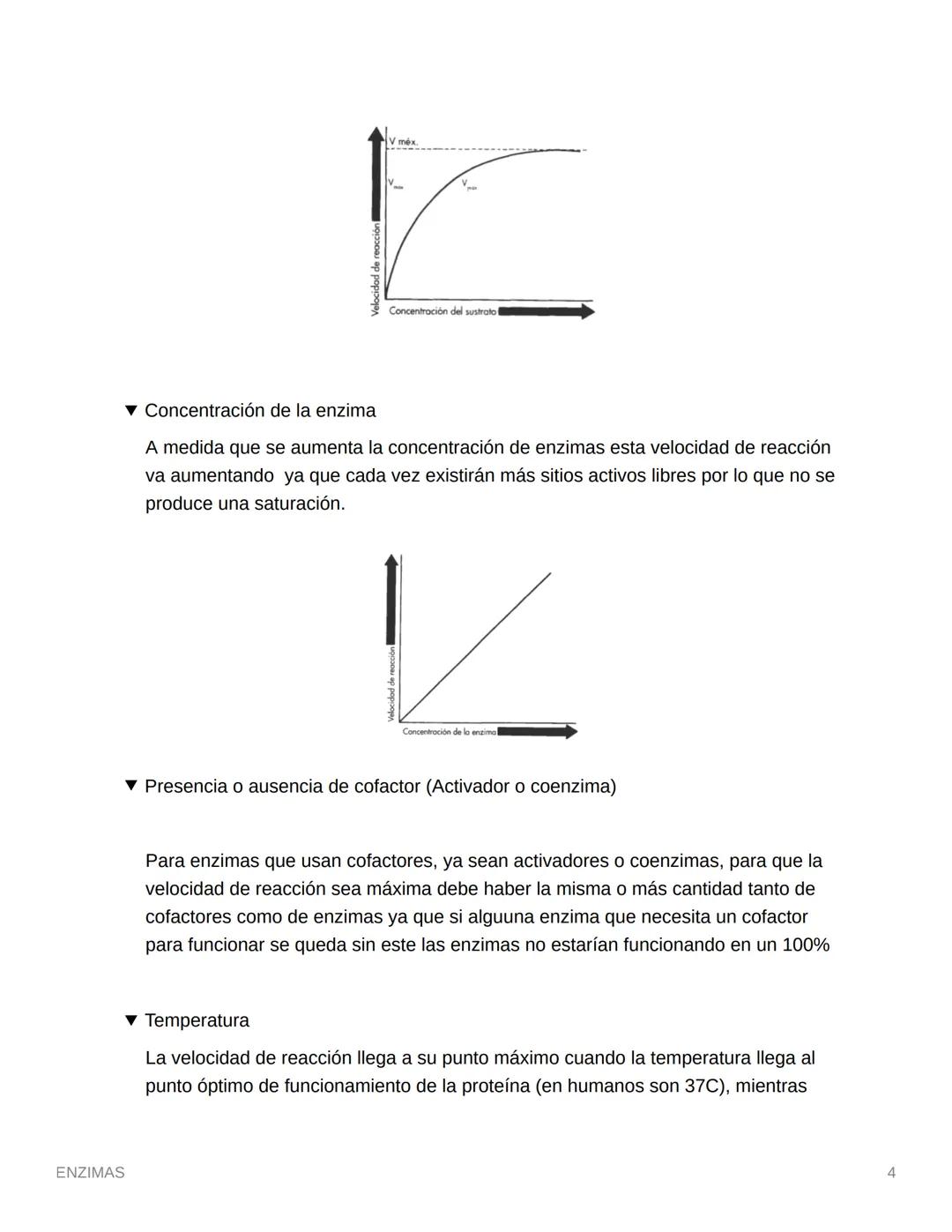
La concentración del sustrato es clave: si aumentas el sustrato con enzimas fijas, la velocidad sube hasta llegar a un máximo. ¿Por qué se detiene? Porque las enzimas se saturan y ya no pueden trabajar más rápido.
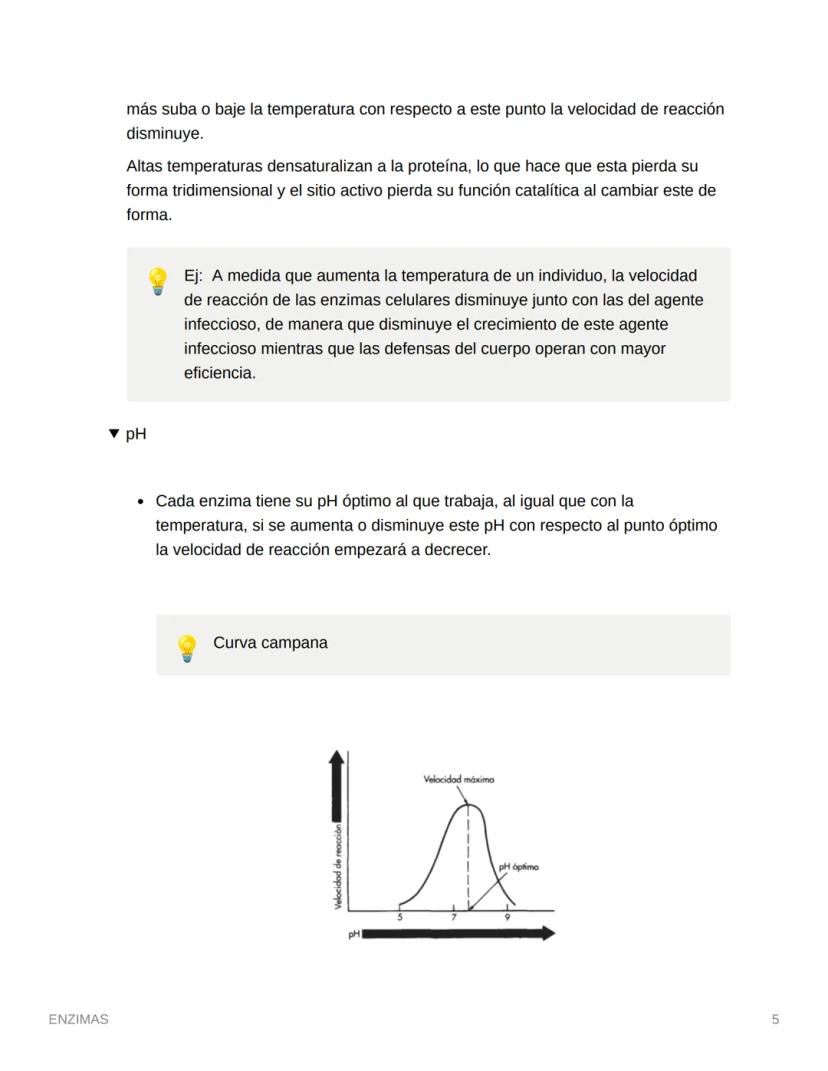
Con la concentración de enzimas pasa lo contrario: mientras más enzimas tengas, más sitios activos disponibles habrá, y la velocidad seguirá aumentando sin saturarse.
Tip de estudio: Imagina las enzimas como cajeros en un banco: pocos cajeros = colas largas, más cajeros = servicio más rápido.
La temperatura tiene un punto óptimo (37°C en humanos) donde las enzimas funcionan mejor. Si sube o baja mucho, la velocidad disminuye. Las temperaturas muy altas desnaturalizan la proteína, cambiando su forma y destruyendo el sitio activo.
Cuando tienes fiebre, es una estrategia genial de tu cuerpo: las enzimas de los microorganismos invasores se vuelven menos eficientes, mientras que tus defensas siguen funcionando mejor.
La presencia de cofactores es fundamental para enzimas que los necesitan. Debe haber igual o más cantidad de cofactores que de enzimas, porque si una enzima se queda sin su cofactor, simplemente no puede trabajar.
Dato curioso: La fiebre es como subir la temperatura del horno: cocina mejor tus defensas y "quema" a los invasores.
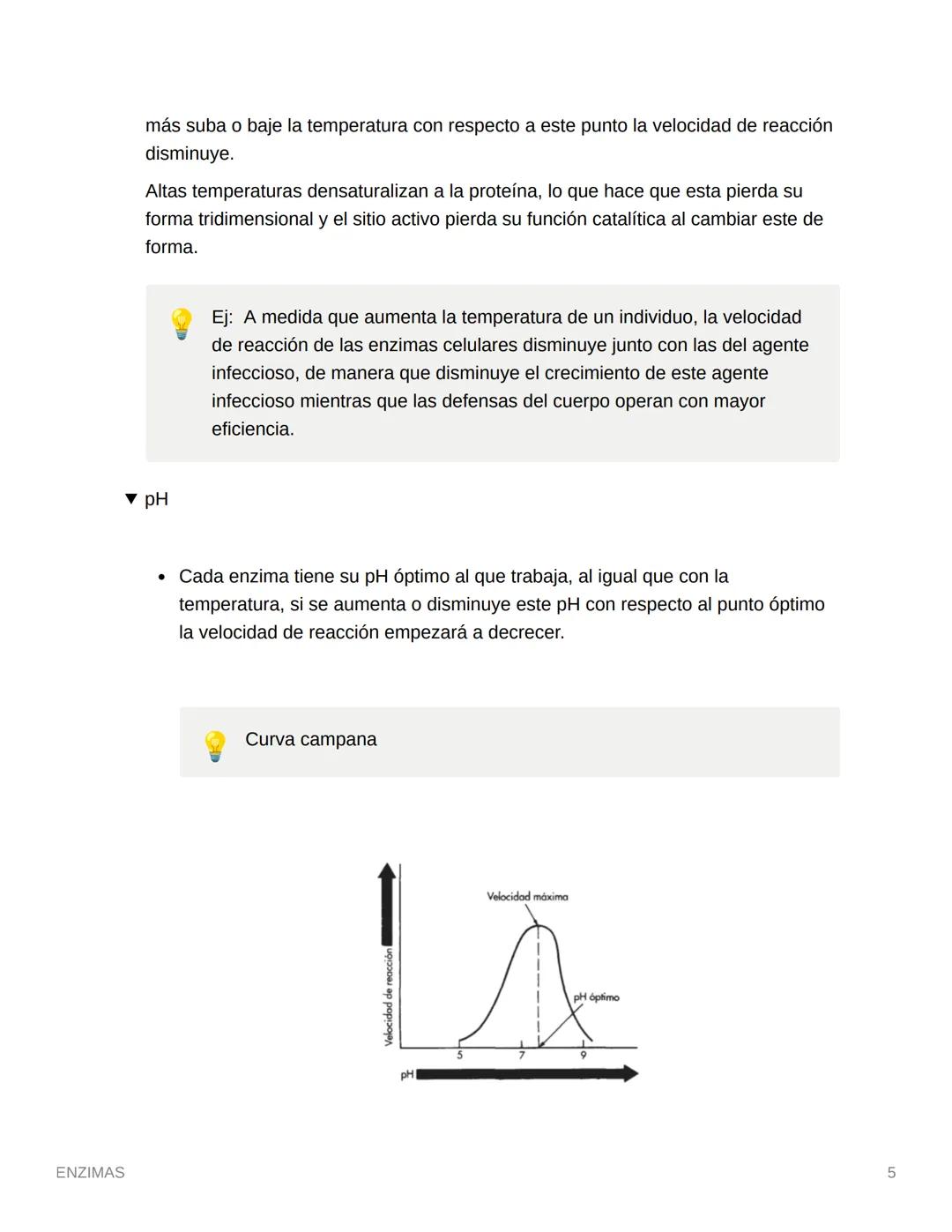
Cada enzima tiene su pH óptimo donde funciona perfectamente. Si el pH se aleja de este punto ideal, la velocidad de reacción disminuye siguiendo una curva en forma de campana.
La mayoría de enzimas celulares funcionan mejor a pH 7 (neutro), que es el pH normal de nuestras células. Pero hay excepciones fascinantes: la pepsina del estómago trabaja a pH 1.5 (súper ácido) y la tripsina del intestino a pH 7.8 (ligeramente alcalino).
Este sistema es perfecto: la comida llega ácida del estómago a los intestinos, donde las sales biliares neutralizan la acidez. Entonces la tripsina puede trabajar cómodamente, terminando de convertir las proteínas en aminoácidos y péptidos pequeños.
Conexión real: Por eso los antiácidos pueden interferir con la digestión si se toman en el momento equivocado.

Los inhibidores competitivos son moléculas que compiten directamente con el sustrato por el sitio activo. Son reversibles y muchas veces se parecen estructuralmente al sustrato real, como gemelos que confunden al sistema.
El truco está en que puedes disminuir su efecto aumentando la concentración del sustrato. Es como una competencia: si hay más sustrato "verdadero", tiene más probabilidades de ganar el sitio activo.
Un ejemplo genial son las drogas sulfas: se parecen tanto a los precursores del ácido fólico que las bacterias se confunden. Como el ácido fólico es esencial para su metabolismo, las bacterias mueren al no poder realizar respiración celular.
Aplicación médica: Este principio se usa en muchos antibióticos que engañan a las bacterias sin dañar nuestras células.

Los inhibidores no competitivos son generalmente irreversibles y más peligrosos. No importa cuánto sustrato agregues, el inhibidor seguirá siendo efectivo porque no compite por el sitio activo.
Estos inhibidores atacan de diferentes maneras: los iones metálicos pesados como Hg²⁺ o Ag⁺ crean enlaces con grupos -SH en las enzimas. Otros cambian la conformación de la enzima o se unen a los activadores.
El ión cianuro es letal porque se une al Fe³⁺ en la citocromo oxidasa, una enzima clave en la respiración celular. El gas Sarin inhibe la acetilcolinesterasa, necesaria para los impulsos nerviosos, causando pérdida muscular y muerte en 5-10 minutos.
Dato importante: Por eso estos compuestos son tan peligrosos: no hay forma fácil de revertir su efecto.

Las enzimas alostéricas tienen sitios especiales (diferentes al sitio activo) donde se unen otras moléculas llamadas efectores. Estas enzimas siempre tienen estructura cuaternaria y actúan como reguladores del metabolismo.
Los efectores positivos activan la enzima aumentando su actividad catalítica. Los efectores negativos la inhiben disminuyendo su función. Ambos cambian la forma del sitio activo para lograr su efecto.
La retroalimentación negativa es un sistema súper inteligente: cuando se produce mucho producto Z, este mismo inhibe a la enzima que lo produce. Si hay poco Z, la inhibición es mínima y se produce más. Es como un termostato que se autorregula.
Analogía útil: Es como el control de volumen de tu música: el producto final "le dice" a la enzima si debe subir o bajar la producción.

Las enzimas son herramientas increíbles para diagnosticar enfermedades. Alexander Fleming, el mismo del descubrimiento de la penicilina, también encontró la lisozima en las lágrimas, que nos protege de microorganismos dañinos.
Para detectar un infarto al miocardio se miden tres enzimas clave: la creatina quinasa (CK) se eleva rápidamente después del infarto, la SGOT sube rápido y baja en 4-5 días, y la lactato deshidrogenasa (LD) aumenta lentamente 1-2 días después.
Para hepatitis viral se mide la SGPT, para enfermedades pancreáticas se detectan amilasa y lipasa elevadas. La ureasa indica problemas renales, la lisozima alta sugiere leucemia monocítica, y la fosfatasa ácida se usa para detectar cáncer de próstata.
Conexión médica: Cada enzima "sale" de su lugar normal cuando hay daño, como una alarma biológica que los médicos pueden detectar.




Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
guzmanvaleria346
@guzmanvaleria346_u2hp
Las enzimas son proteínas súper importantes que aceleran las reacciones químicas en tu cuerpo. Imagínate que son como los "aceleradores" de todas las funciones vitales: desde digerir la comida hasta respirar. Entender cómo funcionan te ayudará a comprender mejor la... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las enzimas son proteínas que bajan la energía de activación necesaria para que ocurran las reacciones químicas. Piénsalo así: hacen que las reacciones sean más fáciles y rápidas, pero no cambian el resultado final.
La magia ocurre cuando el sustrato (la molécula que va a cambiar) se une al sitio activo de la enzima. Esta unión forma un complejo enzima-sustrato que facilita la transformación. Un ejemplo genial es la quimiotripsina, que se encarga de degradar las proteínas que comes.
Existen dos tipos principales: las proteínas simples (solo cadenas de aminoácidos) y las proteínas conjugadas (que necesitan ayuda extra de otras moléculas para funcionar).
Dato clave: Las enzimas no se gastan en las reacciones, por eso pueden trabajar una y otra vez como verdaderos catalizadores biológicos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Una enzima completa tiene tres componentes principales. La apoenzima es la parte proteica, como el motor principal. El cofactor es la parte no proteica que algunas enzimas necesitan para funcionar (no todas la tienen). Cuando se juntan, forman la holoenzima activa.
Los cofactores se dividen en dos grupos. Los activadores son iones metálicos como Fe²⁺, Mg²⁺, Cu²⁺, K⁺, Na⁺ y Zn²⁺. Las coenzimas son compuestos orgánicos pequeños, como las vitaminas hidrosolubles, que se unen temporal o permanentemente.
El sitio activo es una hendidura especial donde ocurre toda la acción. Aquí se rompen los enlaces del sustrato y se forman los nuevos productos. Lo increíble es que este sitio puede cambiar su forma para adaptarse mejor al sustrato, como un guante que se ajusta a tu mano.
Recuerda: Sin cofactores, muchas enzimas son como un carro sin gasolina: no pueden funcionar.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La actividad enzimática mide qué tan rápido una enzima convierte el sustrato en productos. En el laboratorio usamos la fórmula: Actividad = -Δ[S]/Δt o +Δ[P]/Δt (disminución del sustrato o aumento del producto en el tiempo).
La concentración del sustrato es clave: si aumentas el sustrato con enzimas fijas, la velocidad sube hasta llegar a un máximo. ¿Por qué se detiene? Porque las enzimas se saturan y ya no pueden trabajar más rápido.
Con la concentración de enzimas pasa lo contrario: mientras más enzimas tengas, más sitios activos disponibles habrá, y la velocidad seguirá aumentando sin saturarse.
Tip de estudio: Imagina las enzimas como cajeros en un banco: pocos cajeros = colas largas, más cajeros = servicio más rápido.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La temperatura tiene un punto óptimo (37°C en humanos) donde las enzimas funcionan mejor. Si sube o baja mucho, la velocidad disminuye. Las temperaturas muy altas desnaturalizan la proteína, cambiando su forma y destruyendo el sitio activo.
Cuando tienes fiebre, es una estrategia genial de tu cuerpo: las enzimas de los microorganismos invasores se vuelven menos eficientes, mientras que tus defensas siguen funcionando mejor.
La presencia de cofactores es fundamental para enzimas que los necesitan. Debe haber igual o más cantidad de cofactores que de enzimas, porque si una enzima se queda sin su cofactor, simplemente no puede trabajar.
Dato curioso: La fiebre es como subir la temperatura del horno: cocina mejor tus defensas y "quema" a los invasores.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Cada enzima tiene su pH óptimo donde funciona perfectamente. Si el pH se aleja de este punto ideal, la velocidad de reacción disminuye siguiendo una curva en forma de campana.
La mayoría de enzimas celulares funcionan mejor a pH 7 (neutro), que es el pH normal de nuestras células. Pero hay excepciones fascinantes: la pepsina del estómago trabaja a pH 1.5 (súper ácido) y la tripsina del intestino a pH 7.8 (ligeramente alcalino).
Este sistema es perfecto: la comida llega ácida del estómago a los intestinos, donde las sales biliares neutralizan la acidez. Entonces la tripsina puede trabajar cómodamente, terminando de convertir las proteínas en aminoácidos y péptidos pequeños.
Conexión real: Por eso los antiácidos pueden interferir con la digestión si se toman en el momento equivocado.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los inhibidores competitivos son moléculas que compiten directamente con el sustrato por el sitio activo. Son reversibles y muchas veces se parecen estructuralmente al sustrato real, como gemelos que confunden al sistema.
El truco está en que puedes disminuir su efecto aumentando la concentración del sustrato. Es como una competencia: si hay más sustrato "verdadero", tiene más probabilidades de ganar el sitio activo.
Un ejemplo genial son las drogas sulfas: se parecen tanto a los precursores del ácido fólico que las bacterias se confunden. Como el ácido fólico es esencial para su metabolismo, las bacterias mueren al no poder realizar respiración celular.
Aplicación médica: Este principio se usa en muchos antibióticos que engañan a las bacterias sin dañar nuestras células.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los inhibidores no competitivos son generalmente irreversibles y más peligrosos. No importa cuánto sustrato agregues, el inhibidor seguirá siendo efectivo porque no compite por el sitio activo.
Estos inhibidores atacan de diferentes maneras: los iones metálicos pesados como Hg²⁺ o Ag⁺ crean enlaces con grupos -SH en las enzimas. Otros cambian la conformación de la enzima o se unen a los activadores.
El ión cianuro es letal porque se une al Fe³⁺ en la citocromo oxidasa, una enzima clave en la respiración celular. El gas Sarin inhibe la acetilcolinesterasa, necesaria para los impulsos nerviosos, causando pérdida muscular y muerte en 5-10 minutos.
Dato importante: Por eso estos compuestos son tan peligrosos: no hay forma fácil de revertir su efecto.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las enzimas alostéricas tienen sitios especiales (diferentes al sitio activo) donde se unen otras moléculas llamadas efectores. Estas enzimas siempre tienen estructura cuaternaria y actúan como reguladores del metabolismo.
Los efectores positivos activan la enzima aumentando su actividad catalítica. Los efectores negativos la inhiben disminuyendo su función. Ambos cambian la forma del sitio activo para lograr su efecto.
La retroalimentación negativa es un sistema súper inteligente: cuando se produce mucho producto Z, este mismo inhibe a la enzima que lo produce. Si hay poco Z, la inhibición es mínima y se produce más. Es como un termostato que se autorregula.
Analogía útil: Es como el control de volumen de tu música: el producto final "le dice" a la enzima si debe subir o bajar la producción.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las enzimas son herramientas increíbles para diagnosticar enfermedades. Alexander Fleming, el mismo del descubrimiento de la penicilina, también encontró la lisozima en las lágrimas, que nos protege de microorganismos dañinos.
Para detectar un infarto al miocardio se miden tres enzimas clave: la creatina quinasa (CK) se eleva rápidamente después del infarto, la SGOT sube rápido y baja en 4-5 días, y la lactato deshidrogenasa (LD) aumenta lentamente 1-2 días después.
Para hepatitis viral se mide la SGPT, para enfermedades pancreáticas se detectan amilasa y lipasa elevadas. La ureasa indica problemas renales, la lisozima alta sugiere leucemia monocítica, y la fosfatasa ácida se usa para detectar cáncer de próstata.
Conexión médica: Cada enzima "sale" de su lugar normal cuando hay daño, como una alarma biológica que los médicos pueden detectar.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
3
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Fichas Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS