Las reacciones químicas son procesos fundamentales en química donde sustancias... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
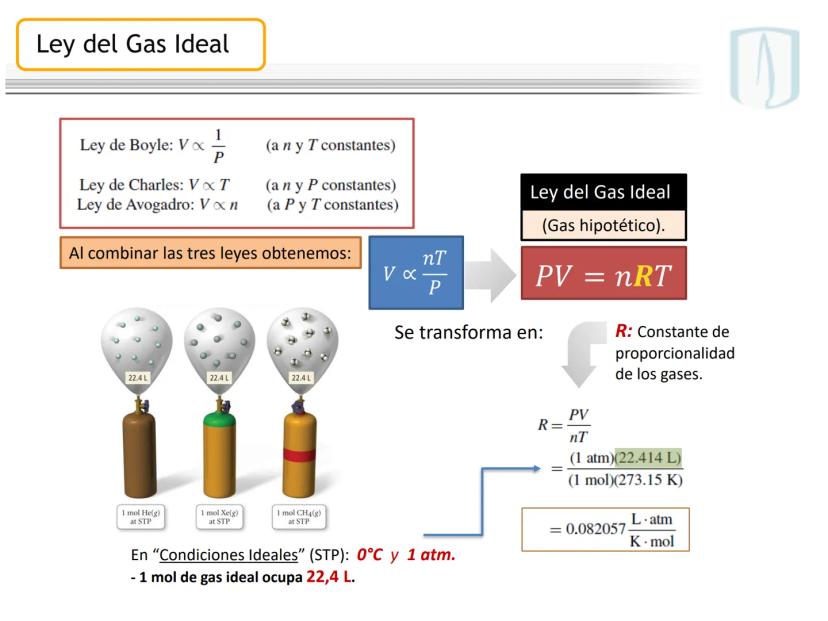
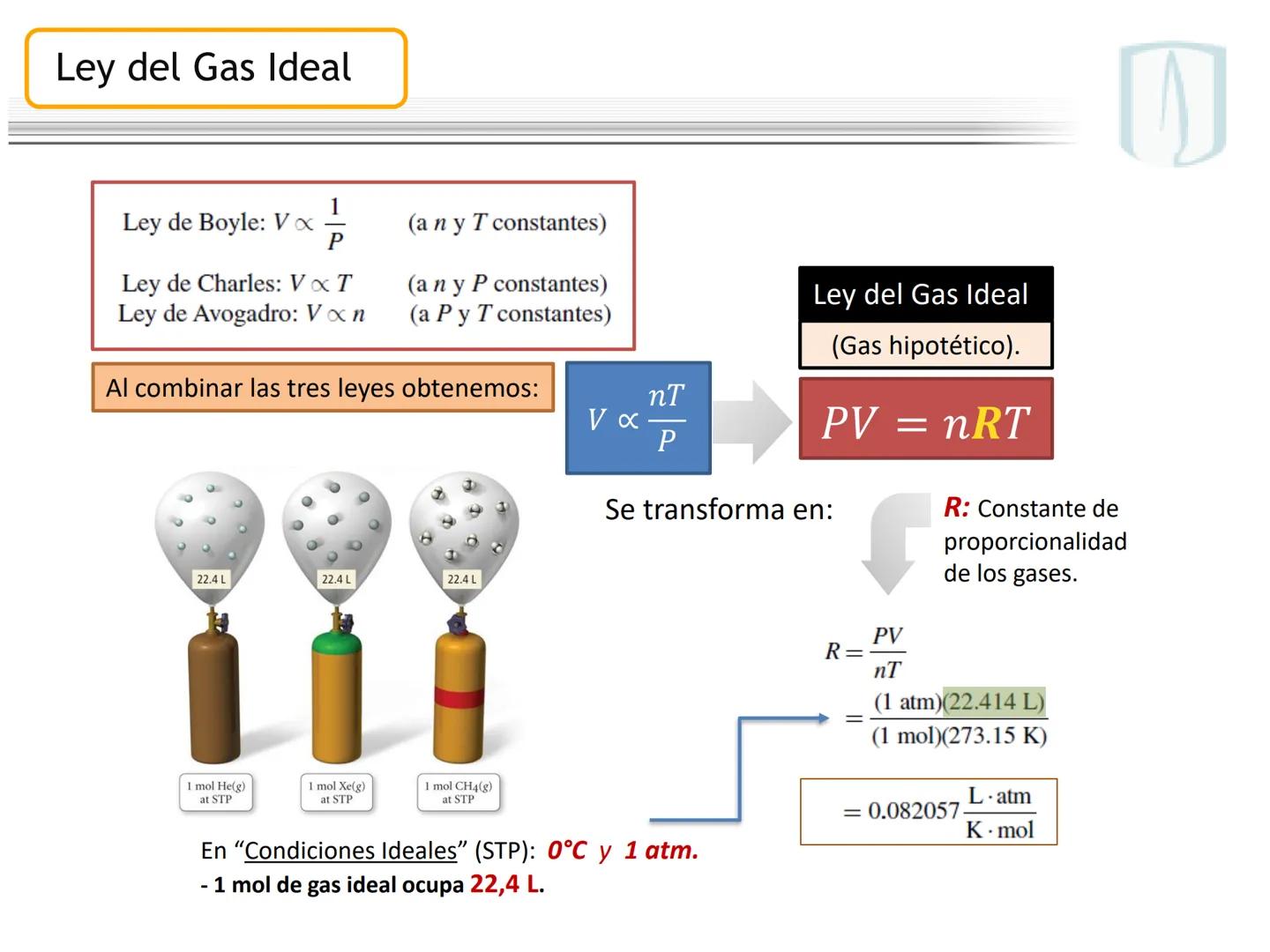
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
1,246
•
Actualizado Mar 23, 2026
•
María Juliana Falla Tovar
@marajulianafall
Las reacciones químicas son procesos fundamentales en química donde sustancias... Mostrar más






Este curso de Química (QUIM1103) del Departamento de Química de la Universidad de los Andes nos introduce a los conceptos fundamentales que rigen las transformaciones de la materia.
Aquí comenzaremos a comprender cómo las sustancias interactúan entre sí para formar nuevos compuestos, siguiendo leyes y principios que podemos predecir y calcular matemáticamente.
¡Dato clave! La química no solo explica cómo funciona el mundo a nivel molecular, sino que también nos permite crear y transformar materiales para aplicaciones prácticas.
Las reacciones químicas están presentes en todo lo que nos rodea, desde la combustión de un fósforo hasta la fotosíntesis de las plantas. Estas transformaciones siguen patrones predecibles que podemos representar.
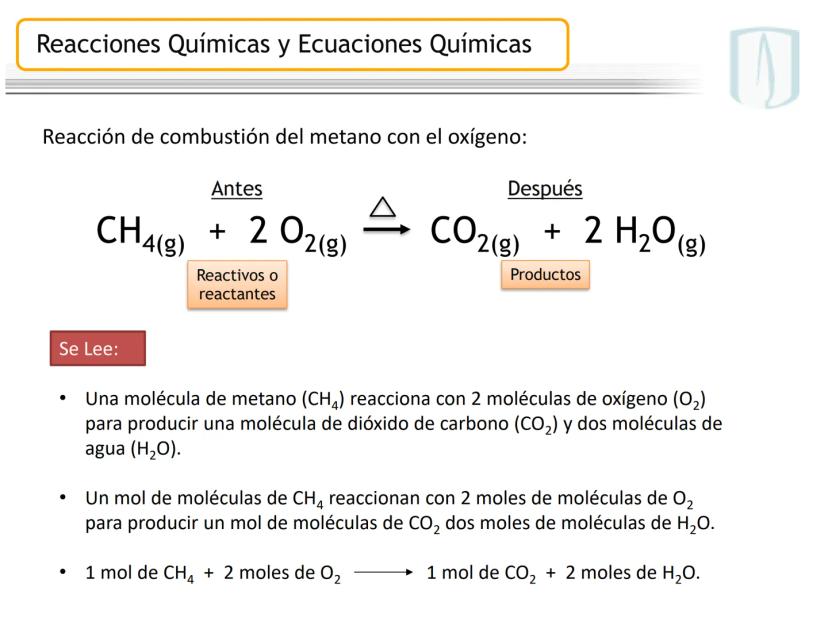
En química, expresamos estos cambios mediante ecuaciones químicas como , donde el metano reacciona con oxígeno para formar dióxido de carbono y agua.
Las ecuaciones nos muestran visualmente lo que sucede con los átomos durante una reacción: ninguno se crea ni se destruye, solo se reorganizan para formar nuevas sustancias.
¡Recuerda! Incluso cuando haces algo tan sencillo como quemar gas en la cocina, estás observando una reacción química que sigue exactamente las mismas leyes que estudiamos en clase.

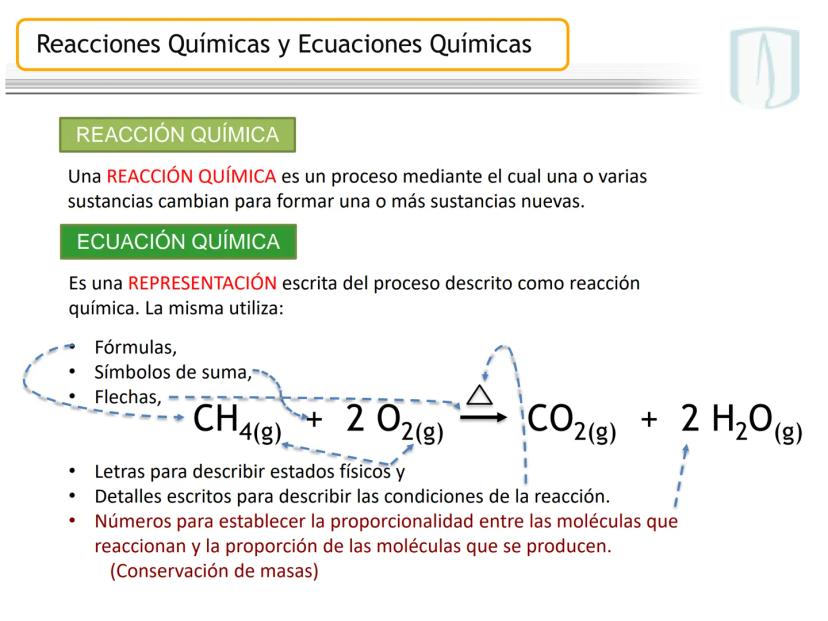
Una reacción química es un proceso donde una o varias sustancias cambian para formar nuevas sustancias con propiedades diferentes. Durante este proceso, los átomos se reorganizan pero no desaparecen.
La ecuación química es la representación escrita de este proceso mediante fórmulas y símbolos. Incluye los reactivos (izquierda), productos (derecha), estados físicos y las proporciones entre moléculas.
Por ejemplo, en , los números al frente de las moléculas son los coeficientes estequiométricos que indican la proporción exacta en que participan las moléculas.
¡Ojo con esto! Los coeficientes estequiométricos son fundamentales para calcular cantidades en una reacción química. Sin ellos, no podríamos saber cuánto producto obtendremos.
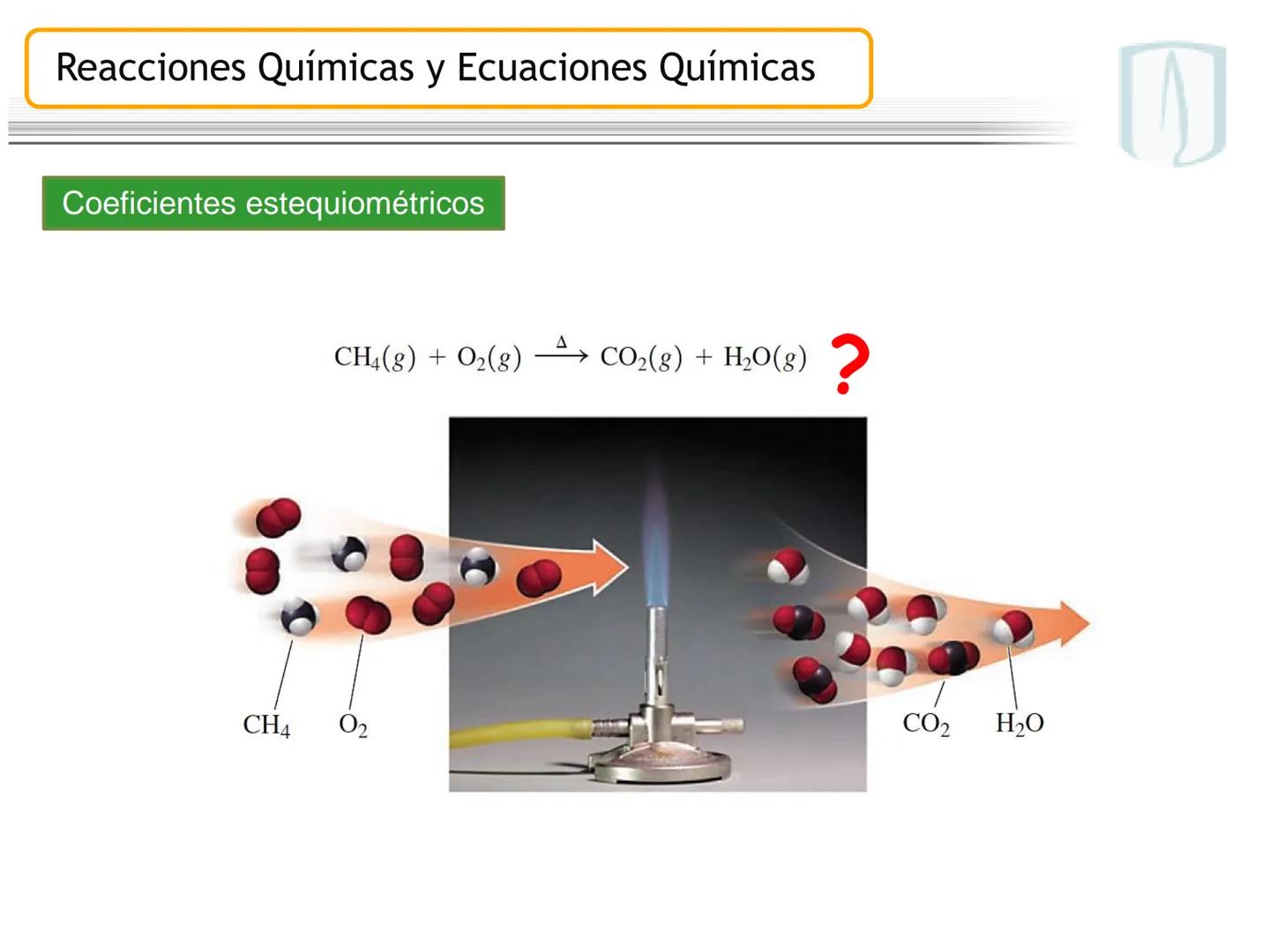
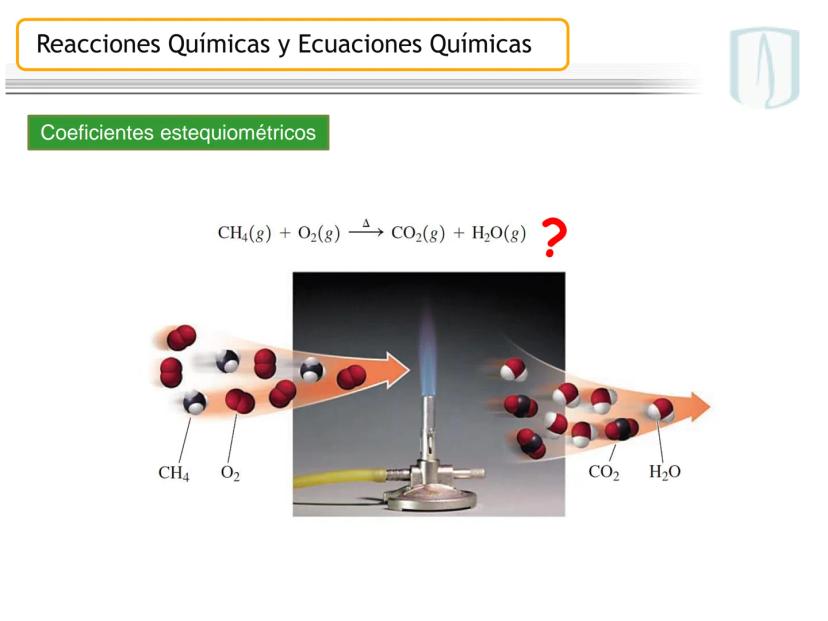
Los coeficientes estequiométricos son números que balancean una ecuación química para cumplir con la ley de conservación de la materia. Son esenciales para representar correctamente las proporciones de reactivos y productos.
Tomemos la ecuación . A simple vista notamos que no está balanceada, pues los átomos no se conservan de reactivos a productos.
Para balancearla, debemos asegurarnos que la cantidad de cada tipo de átomo sea igual en ambos lados. Debemos agregar coeficientes adecuados para que la ley de conservación de masa se cumpla.
¡Inténtalo! Cuando balancees una ecuación, comienza con los elementos que aparecen en menor cantidad de compuestos, luego sigue con los demás. Es como resolver un rompecabezas.
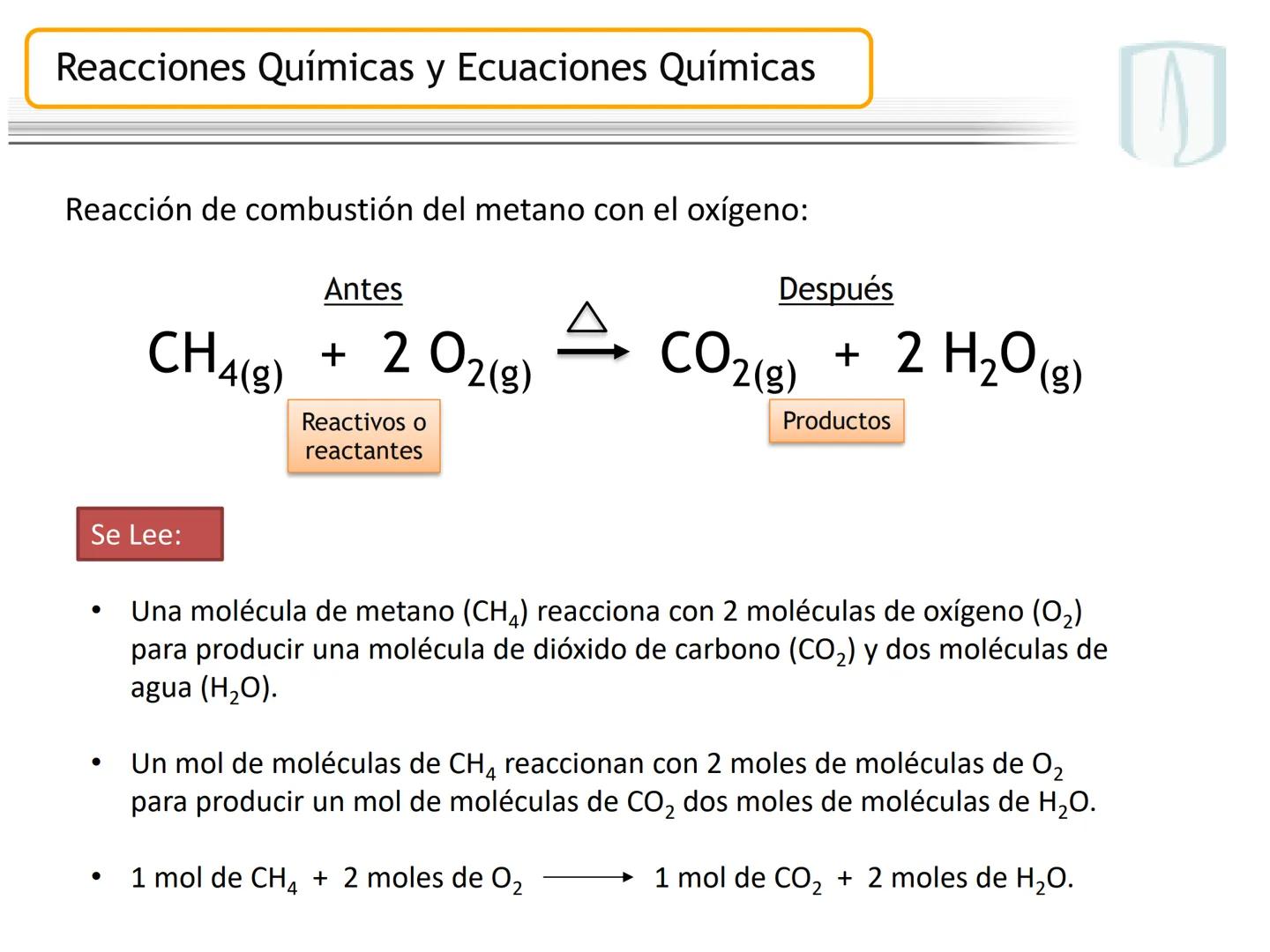
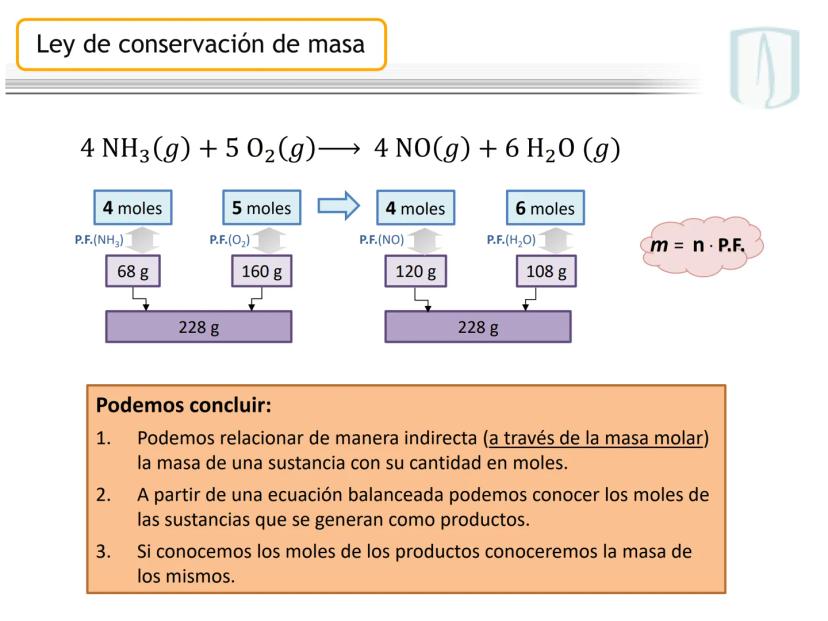
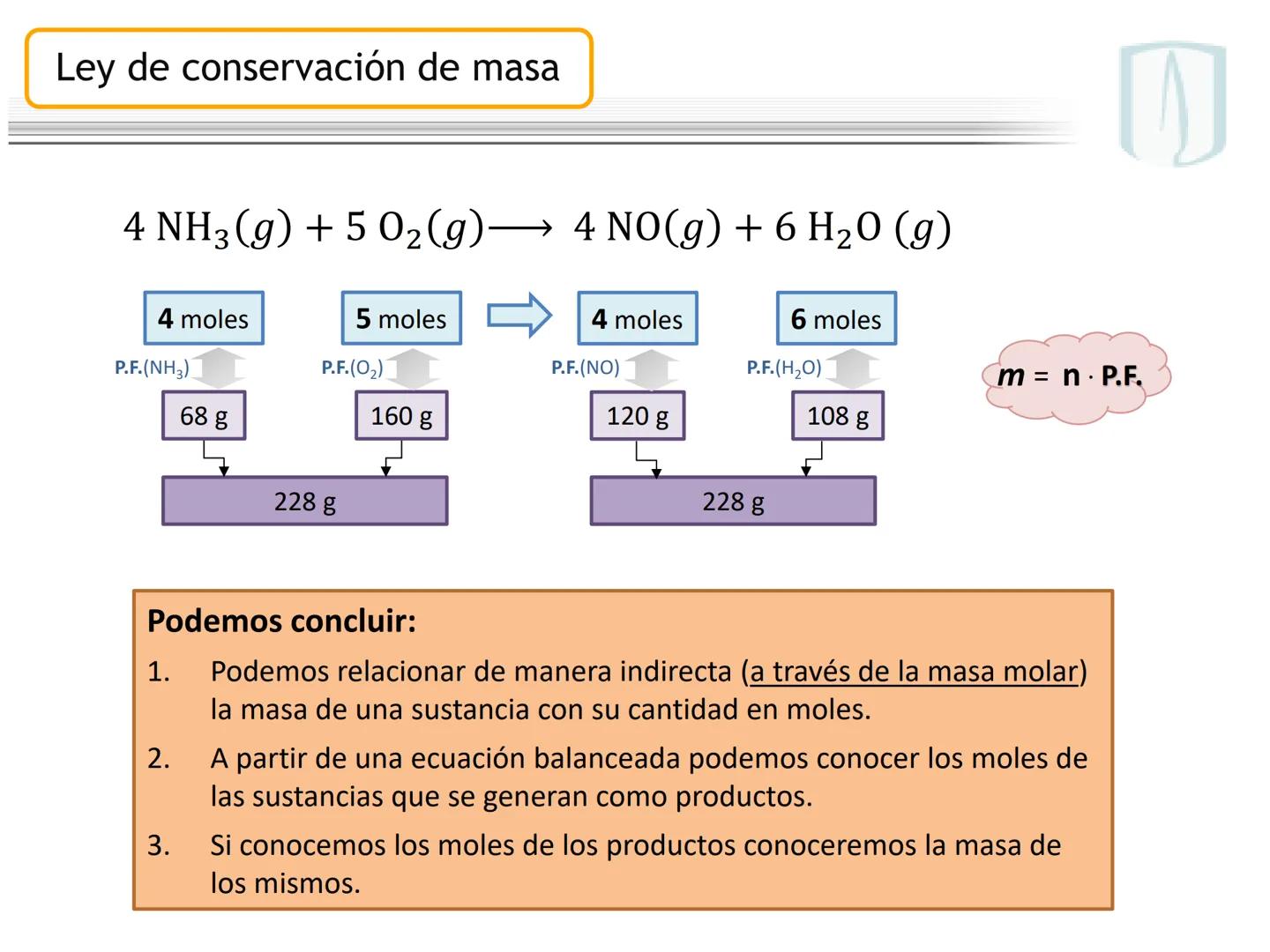
En la ecuación balanceada $4 NH_{3}(g) + 5 O_{2}(g) \longrightarrow 4 NO(g) + 6 H_{2}O (g)$, los coeficientes nos indican las proporciones molares exactas entre reactivos y productos.
Al verificar la conservación de la masa, vemos que los reactivos suman 228 g (68 g de NH₃ y 160 g de O₂) y los productos también suman 228 g (120 g de NO y 108 g de H₂O). La masa total se mantiene constante.
Esta relación se explica por la fórmula , que nos permite convertir entre masa y moles de una sustancia.
¡Concepto clave! La conservación de masa no solo es una ley fundamental de la química, sino que también nos permite predecir cuánto producto obtendremos en una reacción basándonos en los reactivos disponibles.

Al enfrentarnos a la ecuación , podemos calcular las relaciones entre los compuestos usando la estequiometría.
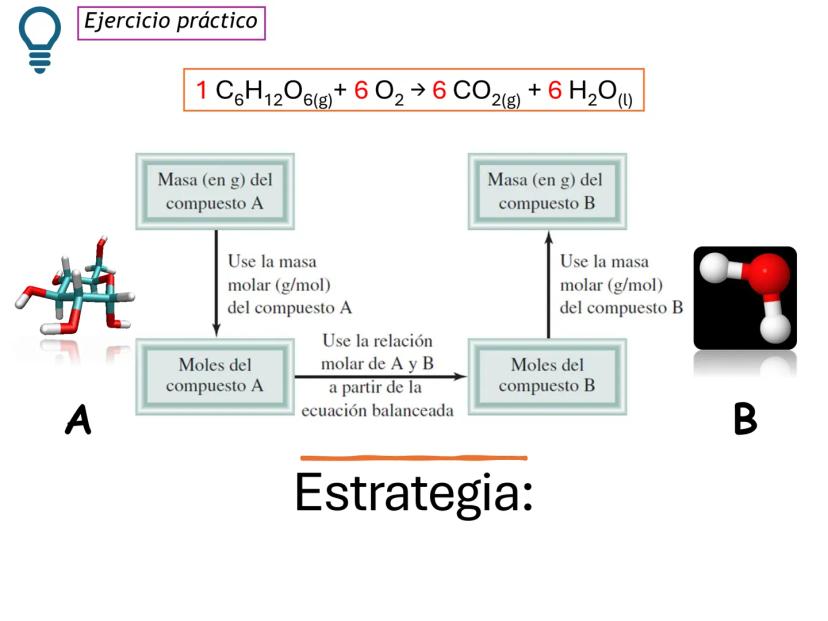
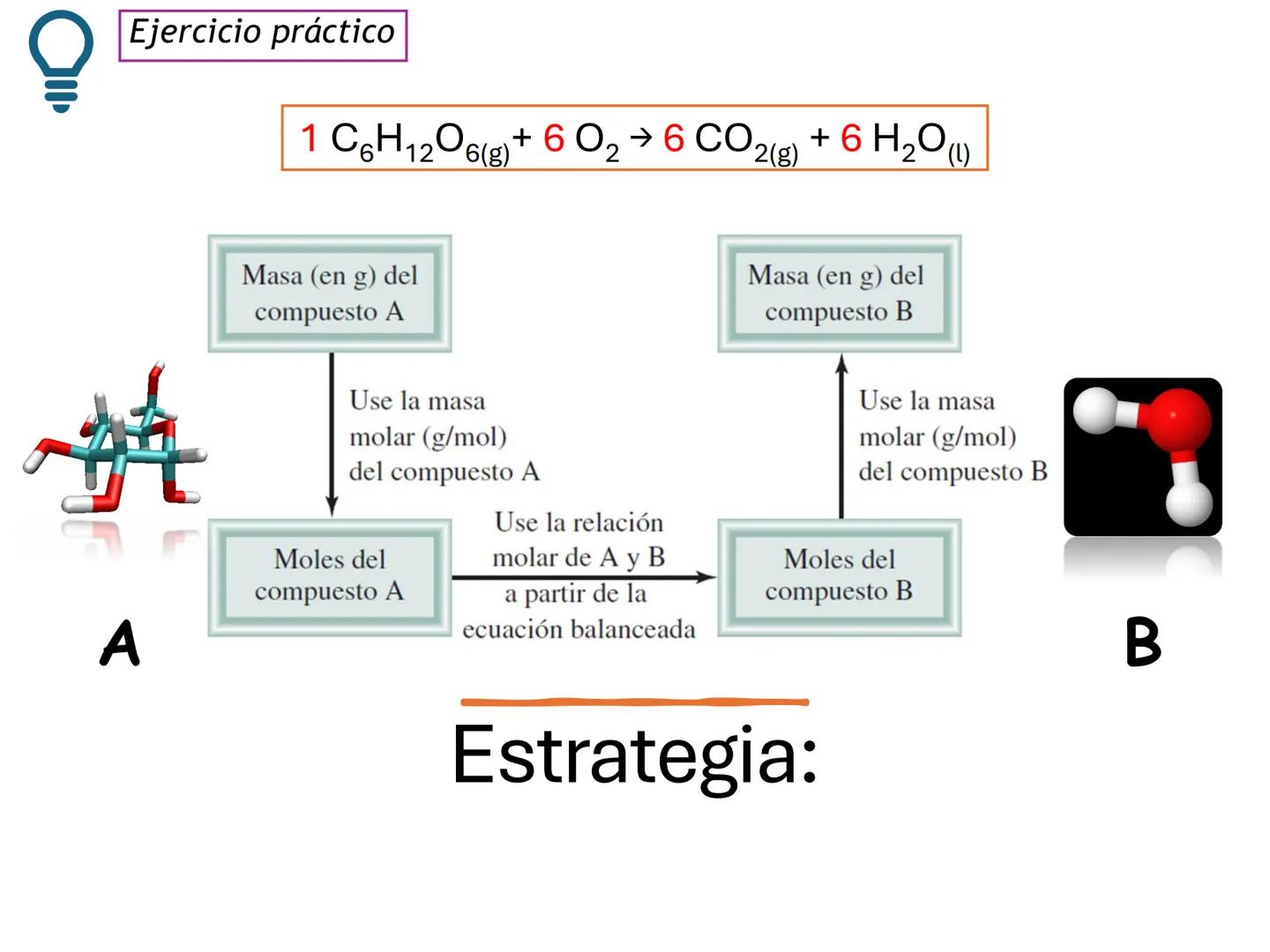
Para resolver problemas estequiométricos, necesitamos seguir una estrategia sistemática que conecte la masa del compuesto A con la masa del compuesto B que queremos encontrar.
Esta estrategia implica convertir masa a moles usando la masa molar, aplicar la relación molar de la ecuación balanceada, y luego convertir nuevamente a masa si es necesario.
¡Consejo útil! Dibuja un diagrama de flujo para tus conversiones: masa A → moles A → moles B → masa B. ¡Te ayudará a no perderte en los cálculos!
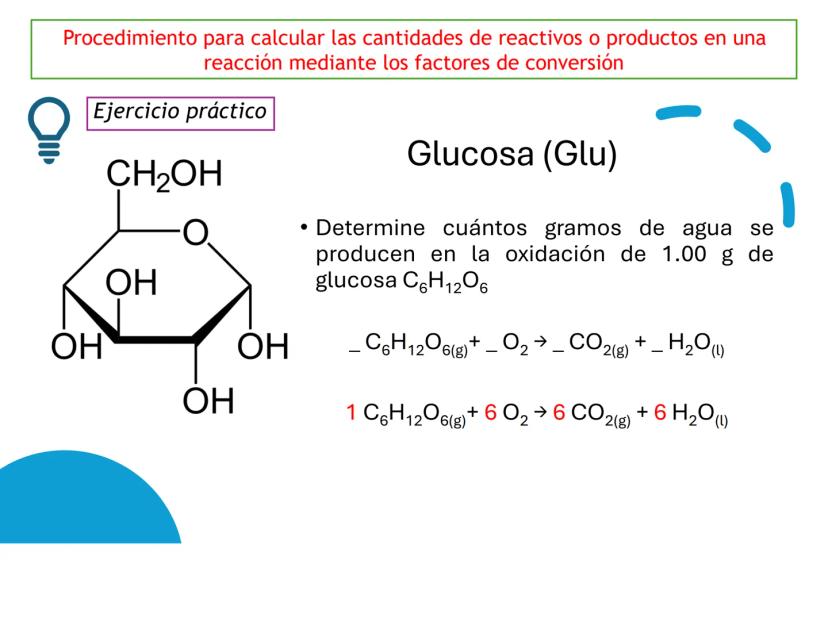
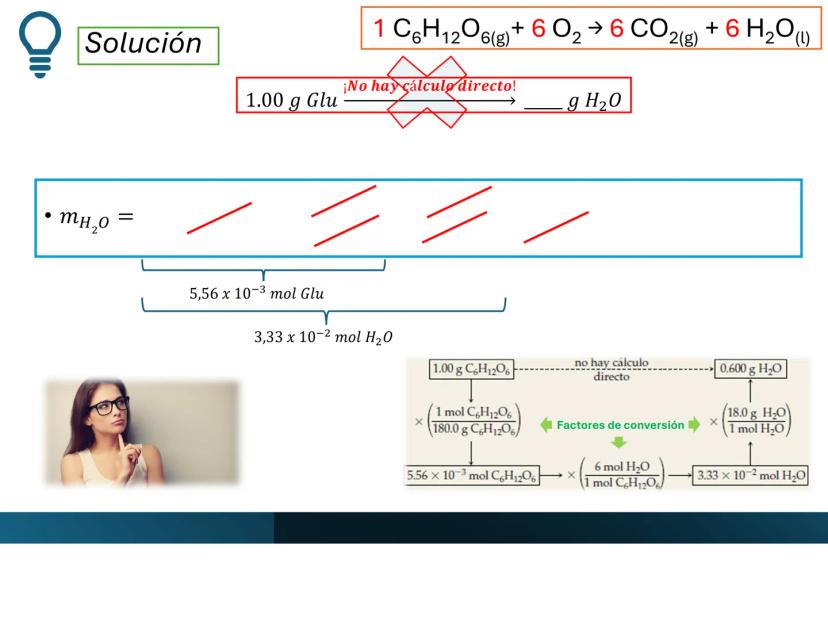
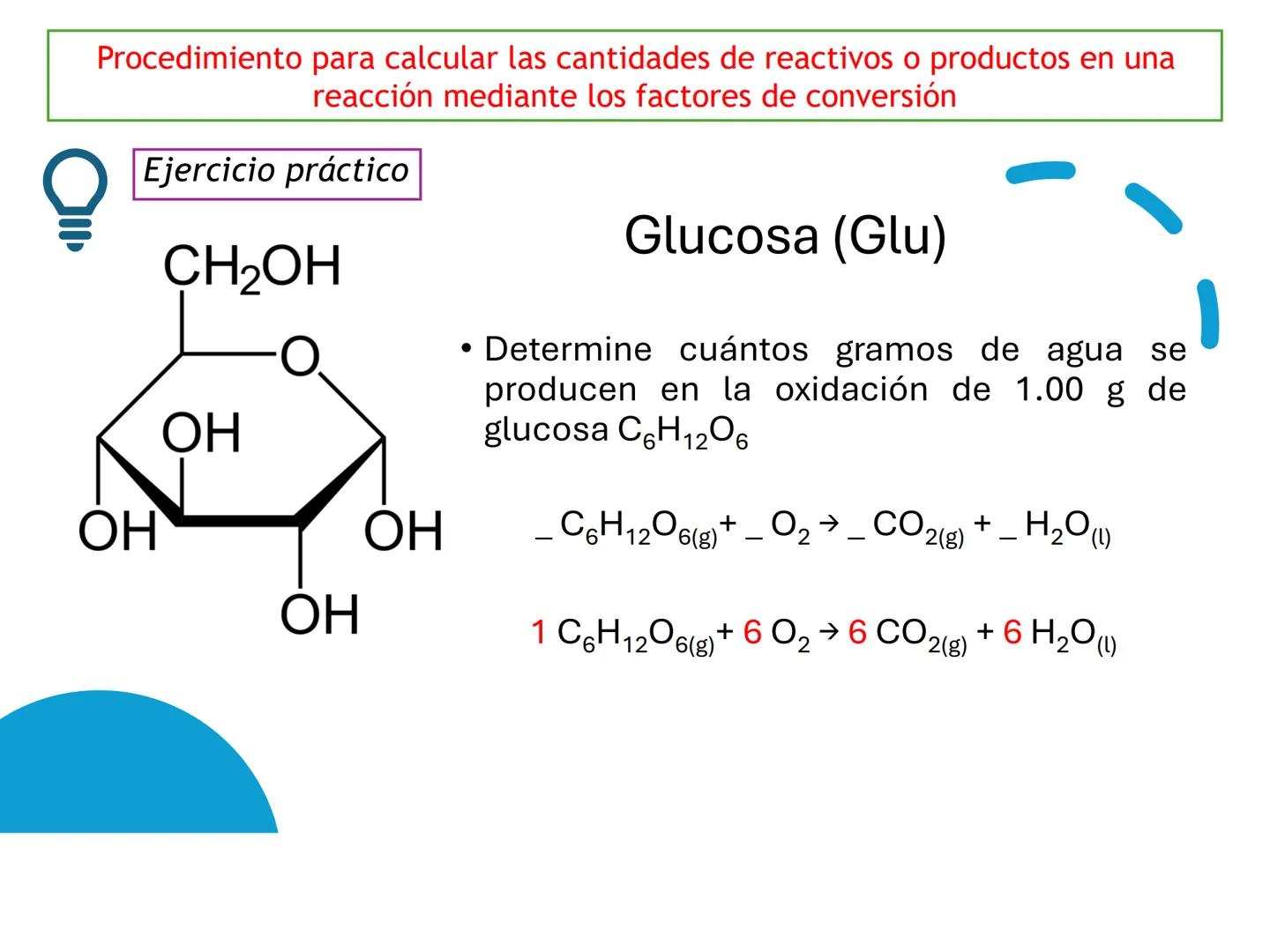
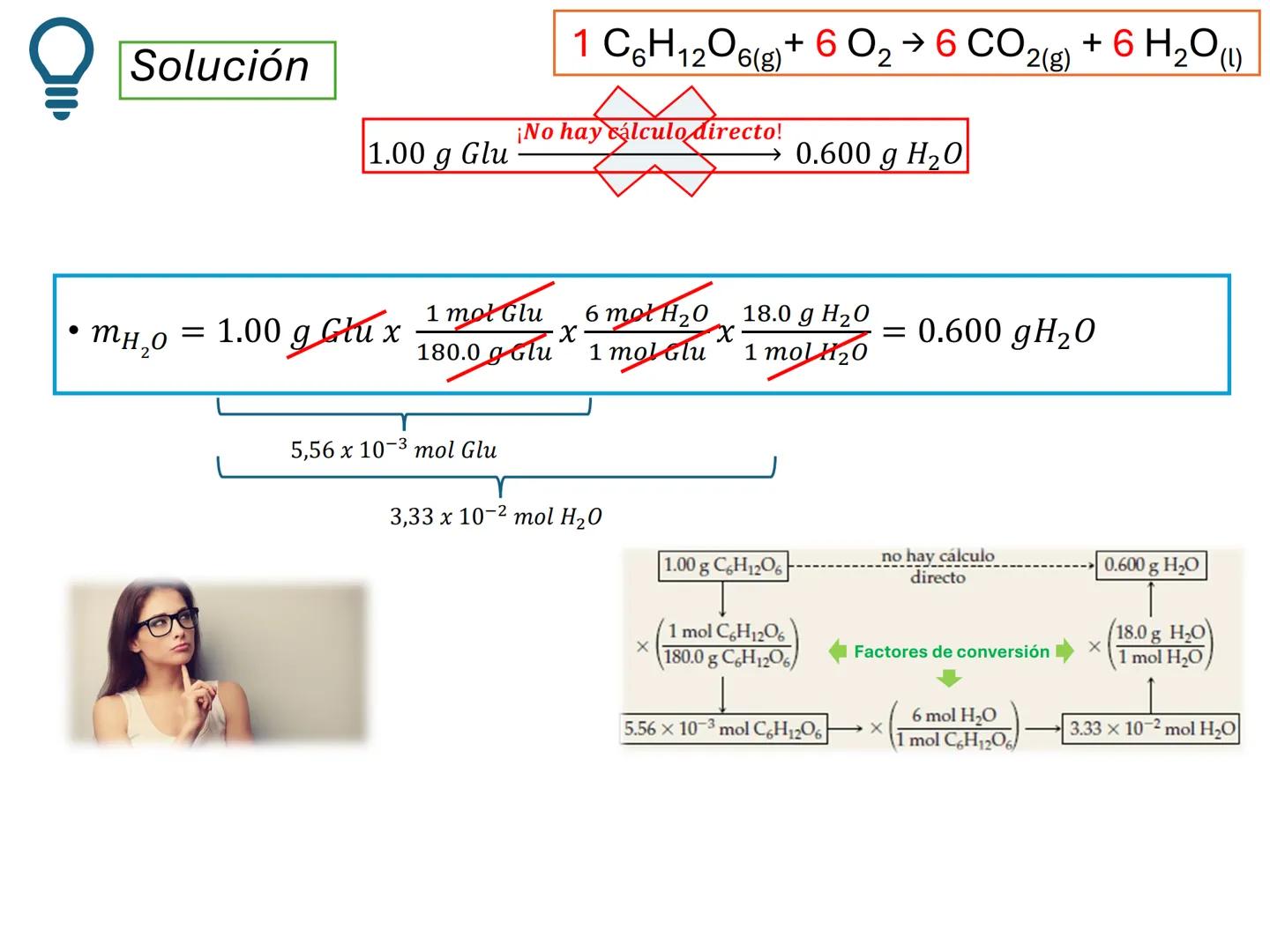
Para calcular la masa de agua que se produce a partir de 1.00 g de glucosa, utilizamos factores de conversión en secuencia para transformar unidades.
Primero convertimos gramos de glucosa a moles: $1.00g~C_{6}H_{12}O_{6} \times \frac{1~mol~C_{6}H_{12}O_{6}}{180.0~g~C_{6}H_{12}O_{6}} = 5.56 \times 10^{-3}~mol~C_{6}H_{12}O_{6}$
Luego, usamos la relación estequiométrica para calcular moles de agua: $5.56 \times 10^{-3}~mol~C_{6}H_{12}O_{6} \times \frac{6~mol~H_{2}O}{1~mol~C_{6}H_{12}O_{6}} = 3.33 \times 10^{-2}~mol~H_{2}O$
Finalmente, convertimos moles de agua a gramos: $3.33 \times 10^{-2}~mol~H_{2}O \times \frac{18.0~g~H_{2}O}{1~mol~H_{2}O} = 0.600~g~H_{2}O$
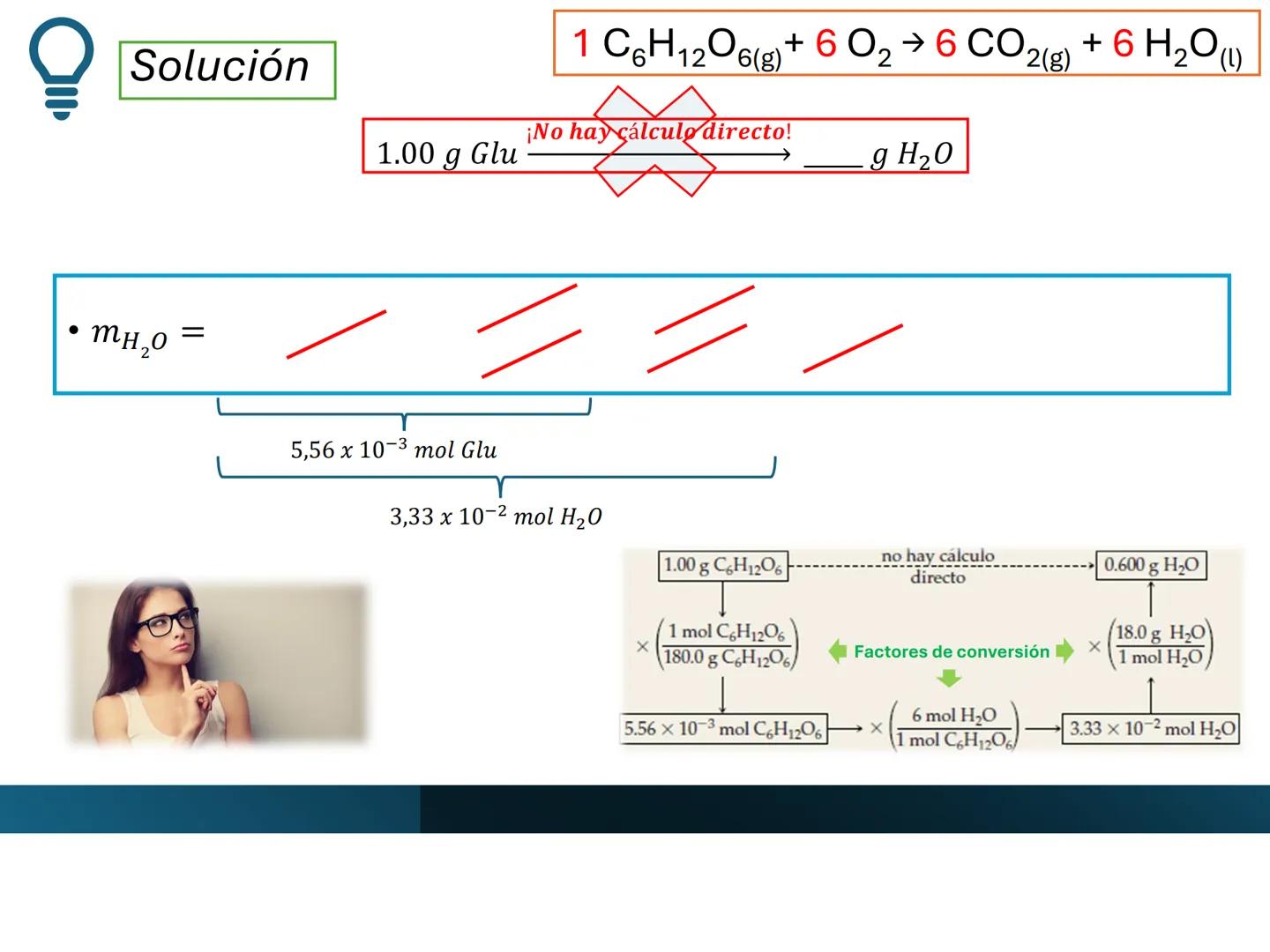
¡Fíjate bien! No existe una conversión directa de gramos de glucosa a gramos de agua. Siempre debes pasar por los moles y usar la relación estequiométrica.
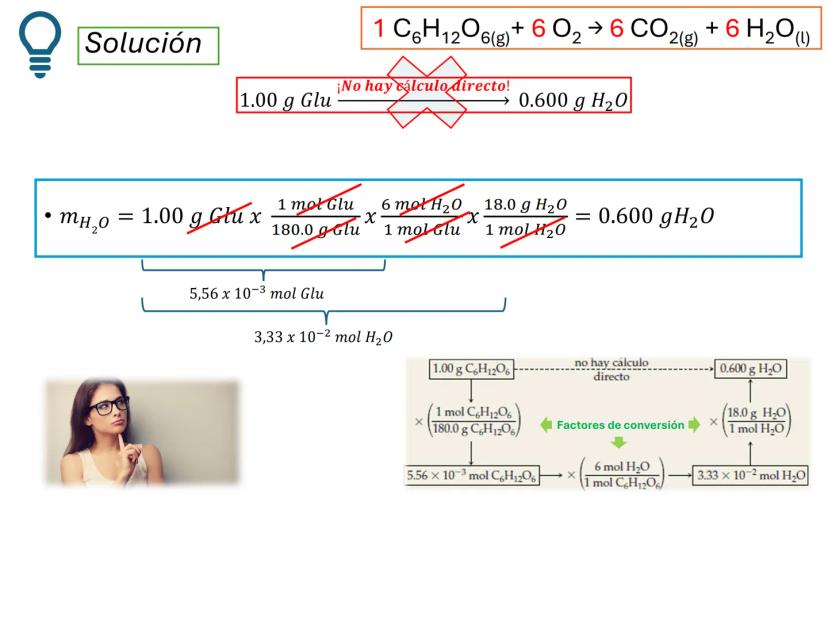
Para calcular cuánta agua se produce a partir de 1.00 g de glucosa en la reacción , usamos factores de conversión encadenados.
Este método nos permite hacer la conversión en un solo cálculo:
Cada factor de conversión tiene un propósito: el primero convierte a moles, el segundo aplica la relación estequiométrica, y el tercero convierte de vuelta a gramos.
¡Simplifica tu trabajo! Organiza todos los factores de conversión en una sola línea para reducir errores y ver claramente la conexión entre lo que tienes y lo que buscas.
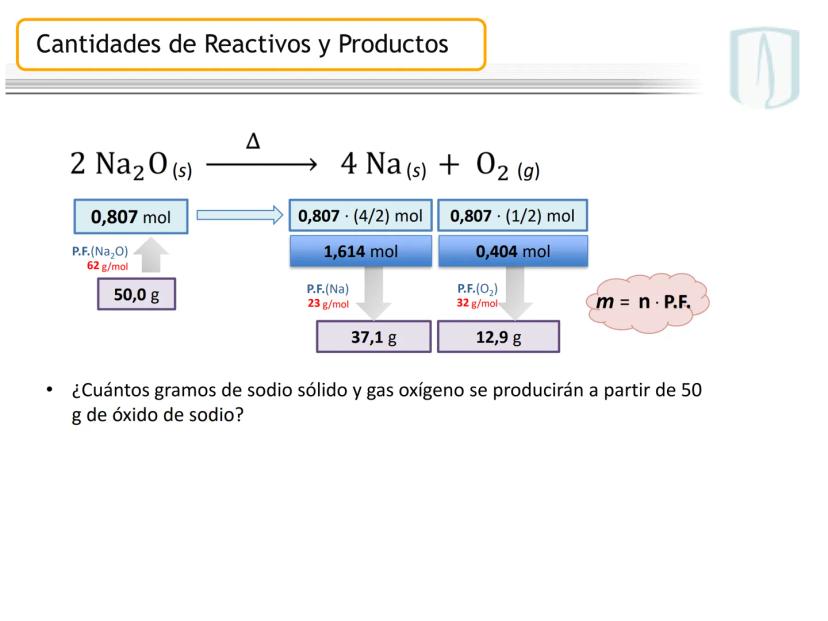
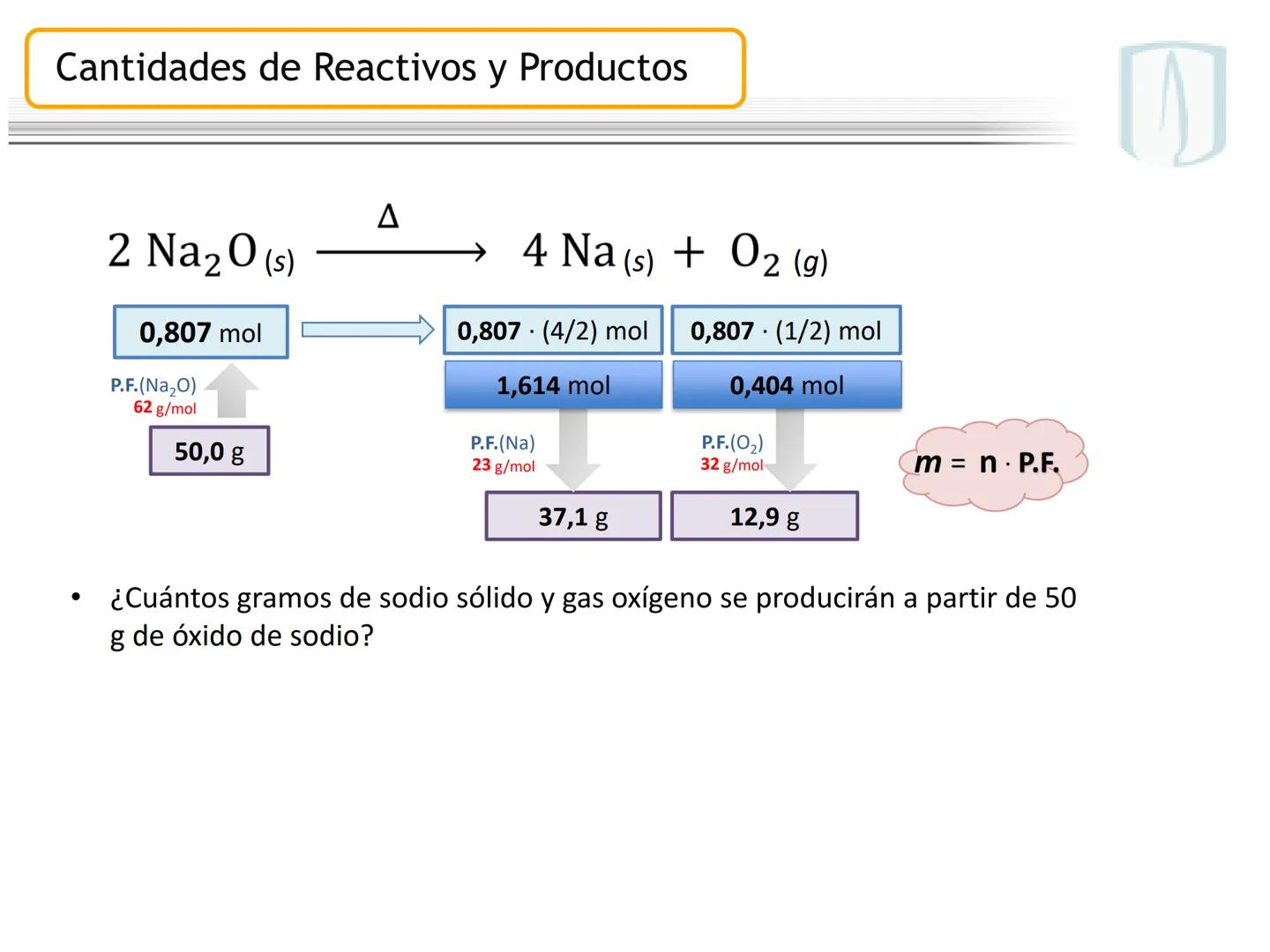
En la reacción , debemos determinar cuánta masa de óxido de hierro(III) se necesita para producir 10.0 g de hierro metálico.
Para resolver este problema, necesitamos convertir la masa de hierro a moles, usar la relación estequiométrica para calcular moles de óxido de hierro, y finalmente convertir a gramos.
También se nos pide calcular la masa de dióxido de carbono producida, lo que requiere un procedimiento similar usando la relación entre hierro y CO₂ según la ecuación balanceada.
¡Ponte a prueba! Este ejercicio te permitirá practicar las conversiones estequiométricas. Recuerda verificar tus unidades en cada paso para asegurar un resultado correcto.
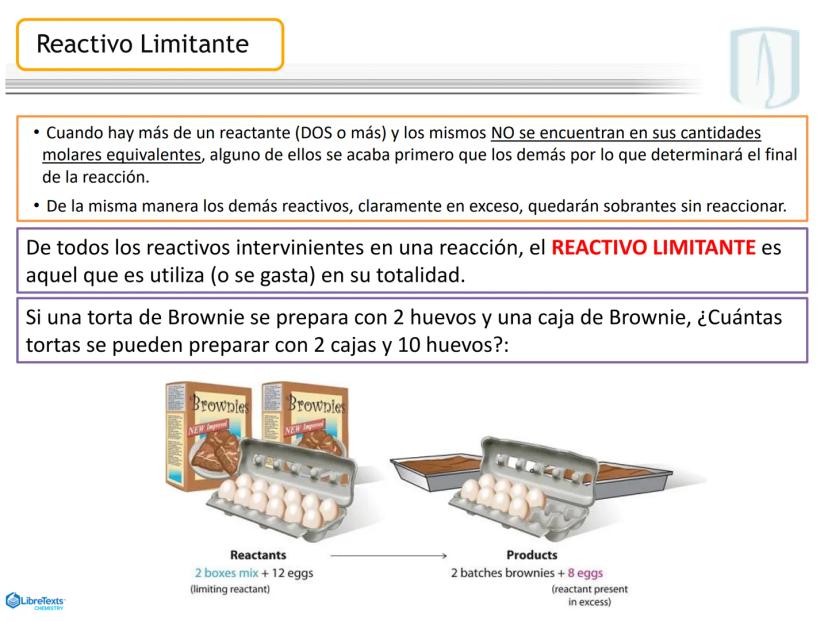
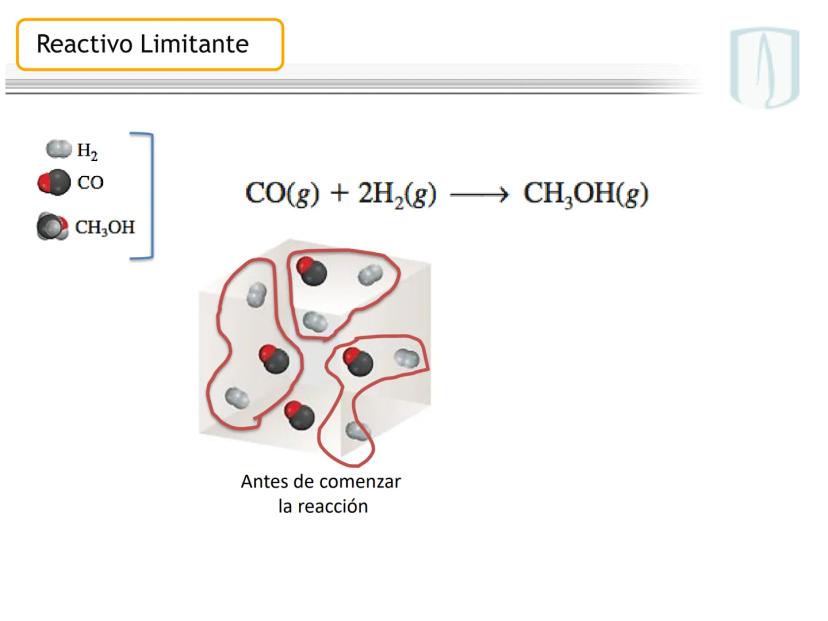
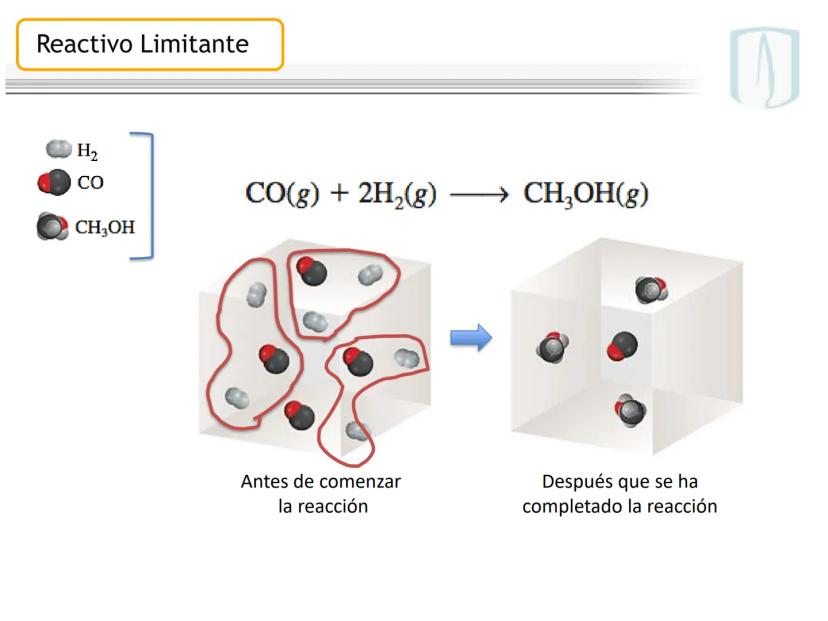
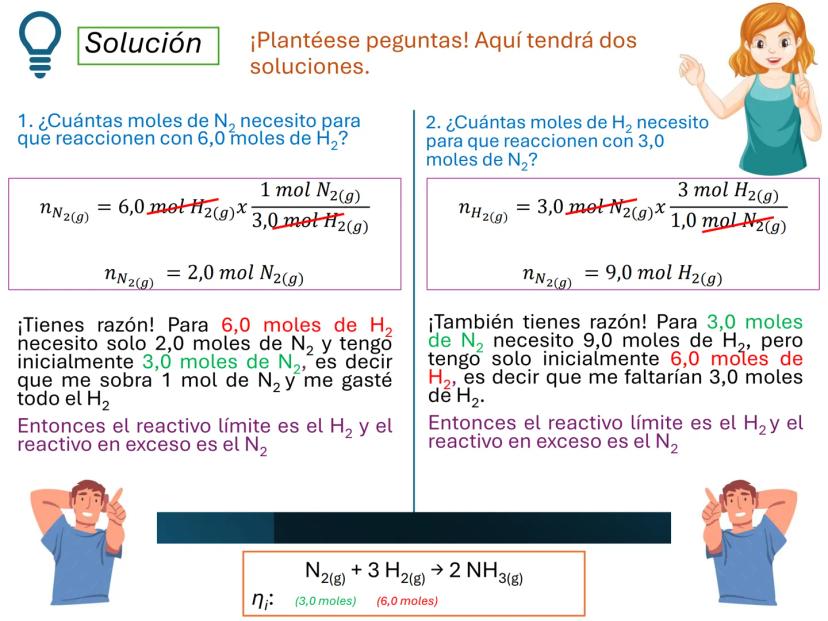
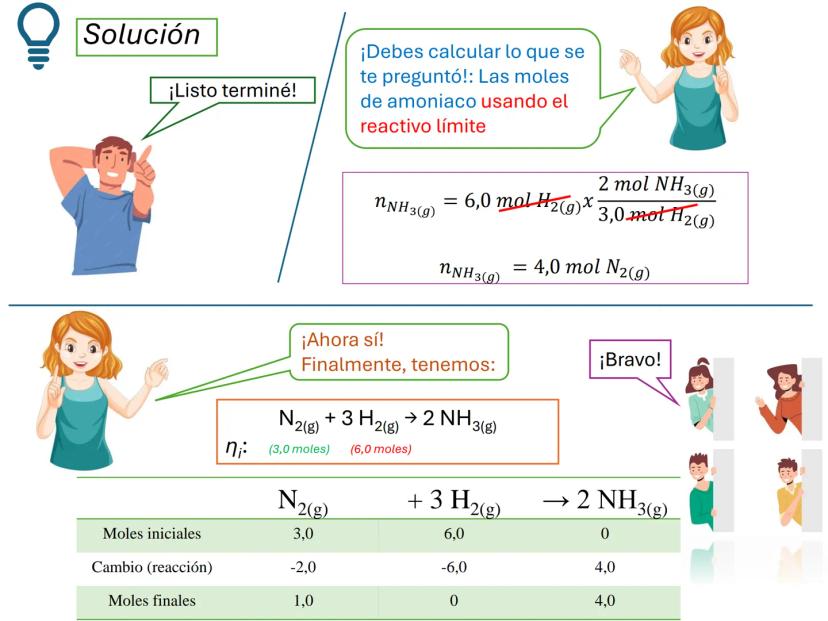
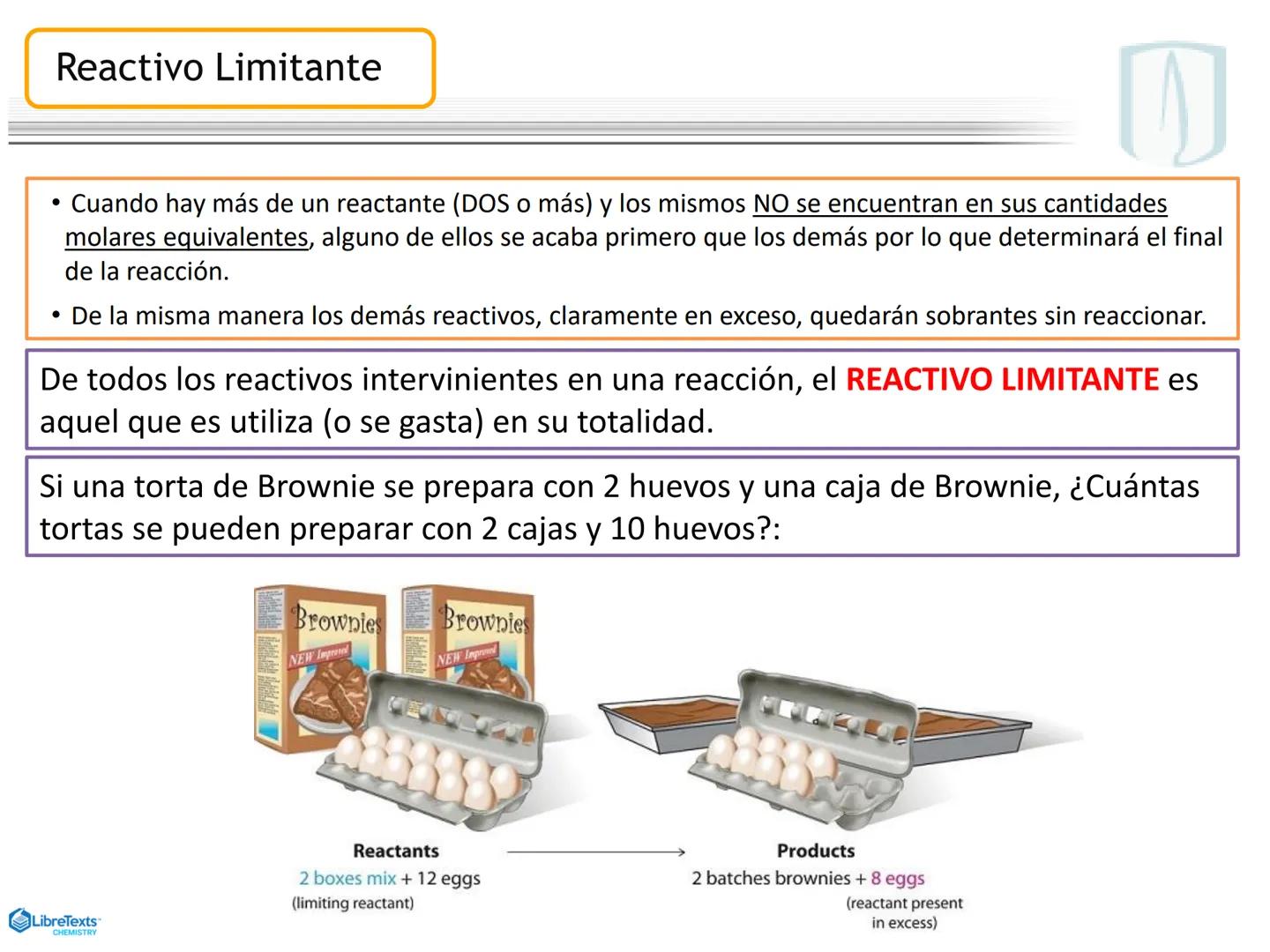
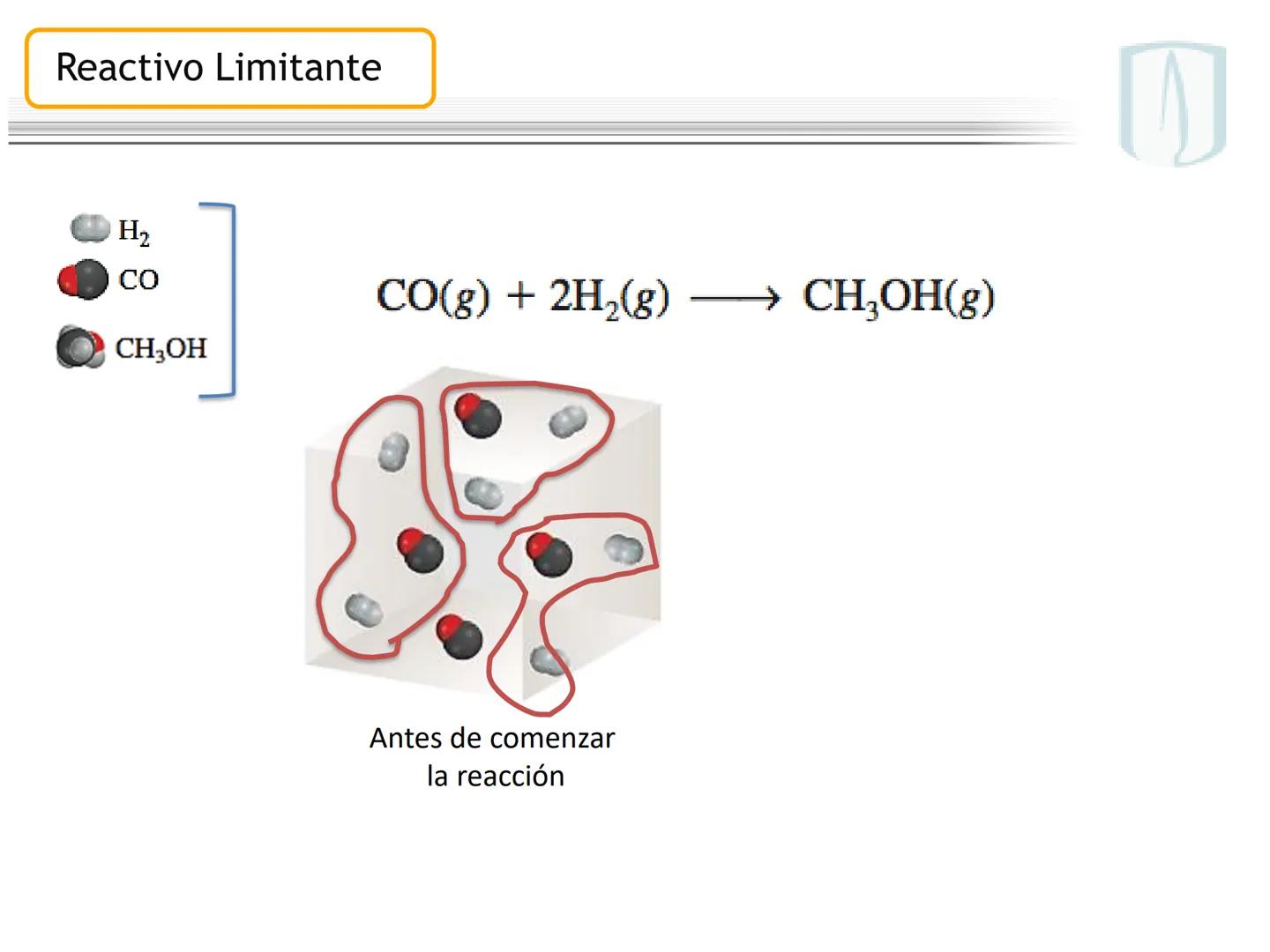
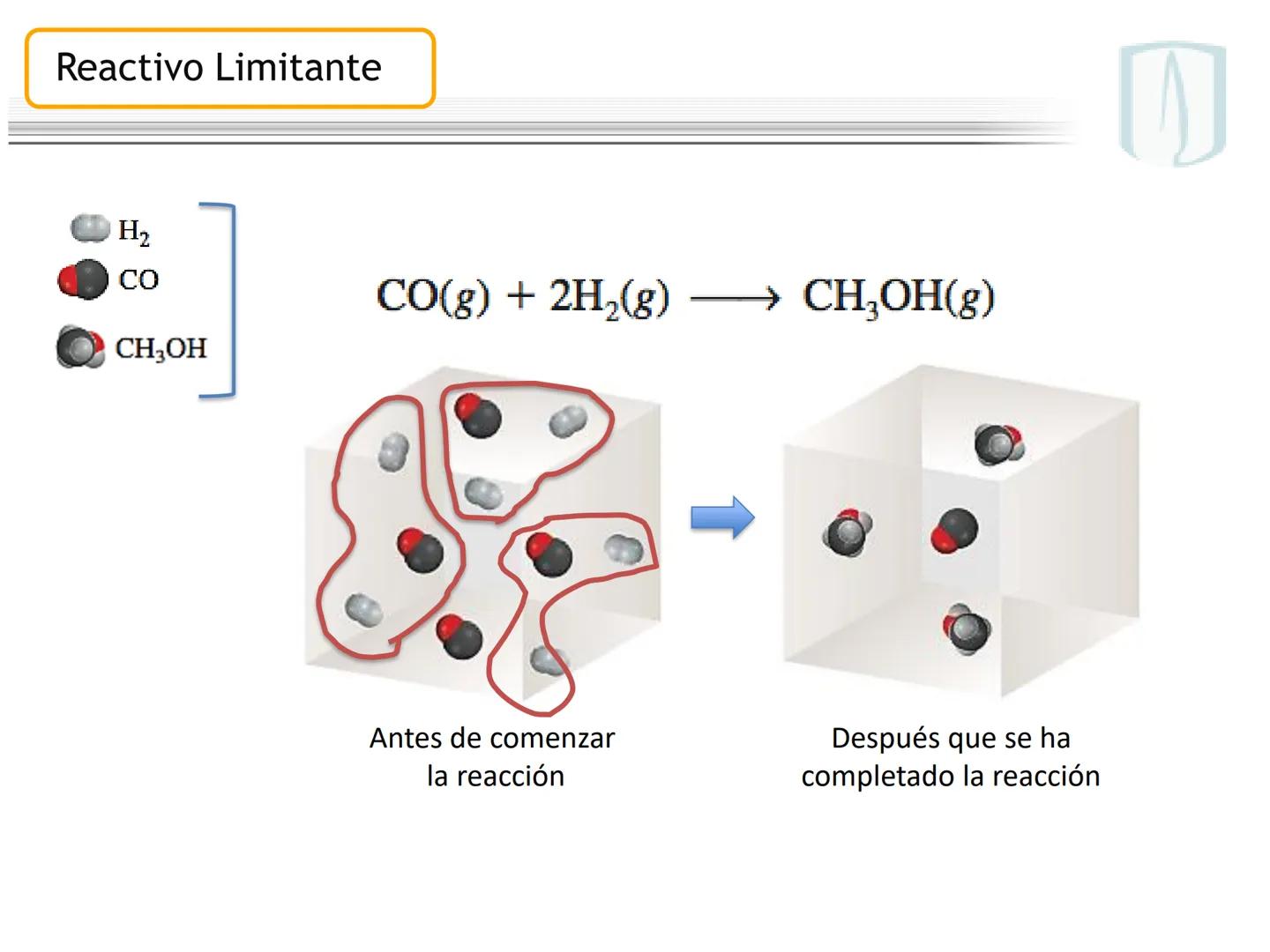
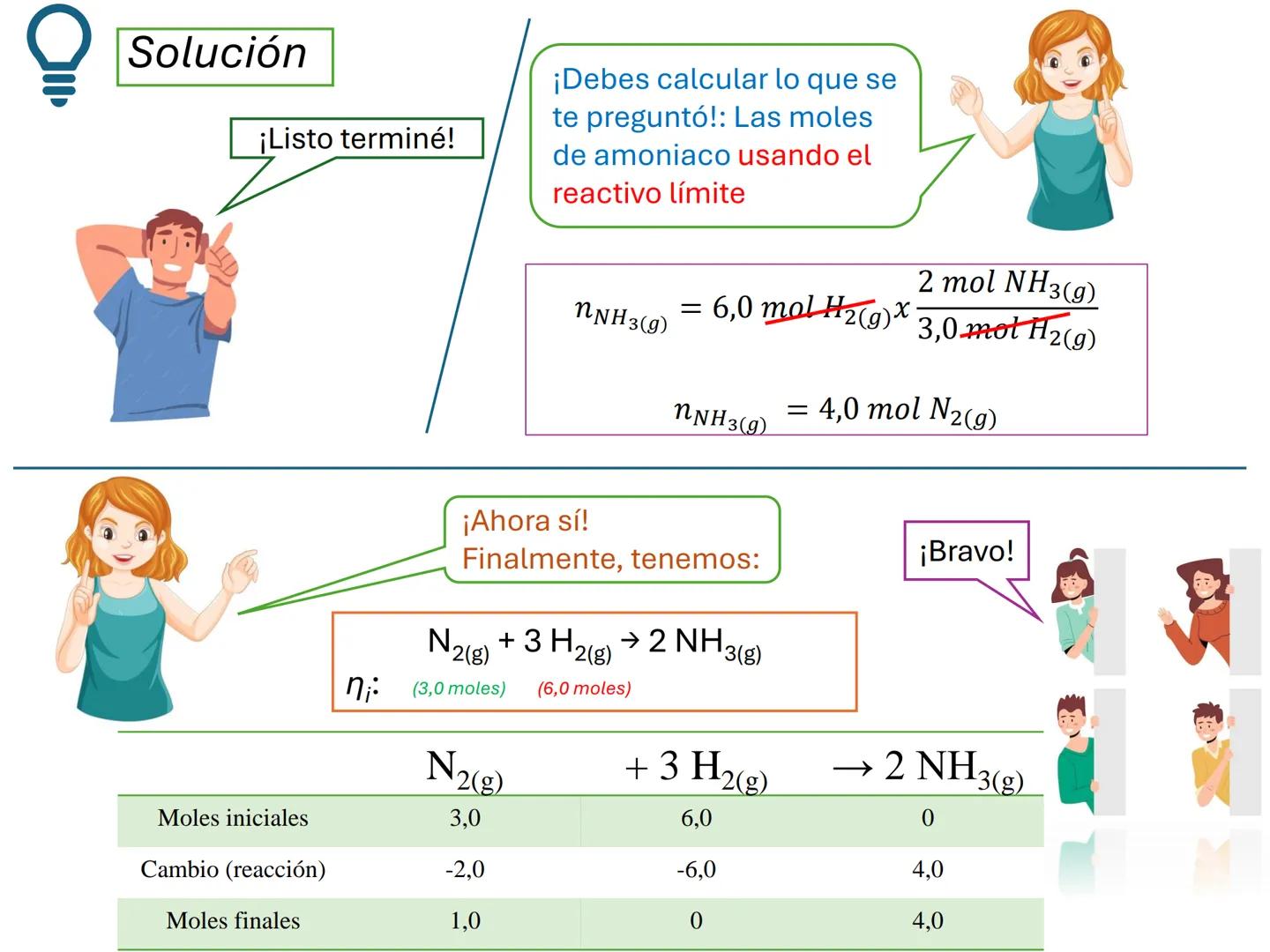
Cuando una reacción química involucra dos o más reactivos que no están en sus proporciones estequiométricas exactas, uno de ellos se agotará antes que los demás, determinando así el final de la reacción.
El reactivo limitante es aquel que se consume completamente y determina la cantidad máxima de producto que se puede formar. Los demás reactivos quedarán parcialmente sin reaccionar.
Es como preparar brownies: si una receta requiere 2 huevos y una caja de mezcla, y tienes 10 huevos pero solo 2 cajas, podrás hacer solamente 2 tandas de brownies porque las cajas son el reactivo limitante.
¡Importante! Identificar el reactivo limitante es fundamental para calcular correctamente el rendimiento de una reacción. ¡Siempre debes basarte en él para tus cálculos!






Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
María Juliana Falla Tovar
@marajulianafall
Las reacciones químicas son procesos fundamentales en química donde sustancias cambian para formar nuevas. Esta transformación se representa mediante ecuaciones químicas que nos permiten entender qué ocurre a nivel molecular y calcular las cantidades de reactivos y productos involucrados.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Este curso de Química (QUIM1103) del Departamento de Química de la Universidad de los Andes nos introduce a los conceptos fundamentales que rigen las transformaciones de la materia.
Aquí comenzaremos a comprender cómo las sustancias interactúan entre sí para formar nuevos compuestos, siguiendo leyes y principios que podemos predecir y calcular matemáticamente.
¡Dato clave! La química no solo explica cómo funciona el mundo a nivel molecular, sino que también nos permite crear y transformar materiales para aplicaciones prácticas.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las reacciones químicas están presentes en todo lo que nos rodea, desde la combustión de un fósforo hasta la fotosíntesis de las plantas. Estas transformaciones siguen patrones predecibles que podemos representar.
En química, expresamos estos cambios mediante ecuaciones químicas como , donde el metano reacciona con oxígeno para formar dióxido de carbono y agua.
Las ecuaciones nos muestran visualmente lo que sucede con los átomos durante una reacción: ninguno se crea ni se destruye, solo se reorganizan para formar nuevas sustancias.
¡Recuerda! Incluso cuando haces algo tan sencillo como quemar gas en la cocina, estás observando una reacción química que sigue exactamente las mismas leyes que estudiamos en clase.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Una reacción química es un proceso donde una o varias sustancias cambian para formar nuevas sustancias con propiedades diferentes. Durante este proceso, los átomos se reorganizan pero no desaparecen.
La ecuación química es la representación escrita de este proceso mediante fórmulas y símbolos. Incluye los reactivos (izquierda), productos (derecha), estados físicos y las proporciones entre moléculas.
Por ejemplo, en , los números al frente de las moléculas son los coeficientes estequiométricos que indican la proporción exacta en que participan las moléculas.
¡Ojo con esto! Los coeficientes estequiométricos son fundamentales para calcular cantidades en una reacción química. Sin ellos, no podríamos saber cuánto producto obtendremos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los coeficientes estequiométricos son números que balancean una ecuación química para cumplir con la ley de conservación de la materia. Son esenciales para representar correctamente las proporciones de reactivos y productos.
Tomemos la ecuación . A simple vista notamos que no está balanceada, pues los átomos no se conservan de reactivos a productos.
Para balancearla, debemos asegurarnos que la cantidad de cada tipo de átomo sea igual en ambos lados. Debemos agregar coeficientes adecuados para que la ley de conservación de masa se cumpla.
¡Inténtalo! Cuando balancees una ecuación, comienza con los elementos que aparecen en menor cantidad de compuestos, luego sigue con los demás. Es como resolver un rompecabezas.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
En la ecuación balanceada $4 NH_{3}(g) + 5 O_{2}(g) \longrightarrow 4 NO(g) + 6 H_{2}O (g)$, los coeficientes nos indican las proporciones molares exactas entre reactivos y productos.
Al verificar la conservación de la masa, vemos que los reactivos suman 228 g (68 g de NH₃ y 160 g de O₂) y los productos también suman 228 g (120 g de NO y 108 g de H₂O). La masa total se mantiene constante.
Esta relación se explica por la fórmula , que nos permite convertir entre masa y moles de una sustancia.
¡Concepto clave! La conservación de masa no solo es una ley fundamental de la química, sino que también nos permite predecir cuánto producto obtendremos en una reacción basándonos en los reactivos disponibles.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Al enfrentarnos a la ecuación , podemos calcular las relaciones entre los compuestos usando la estequiometría.
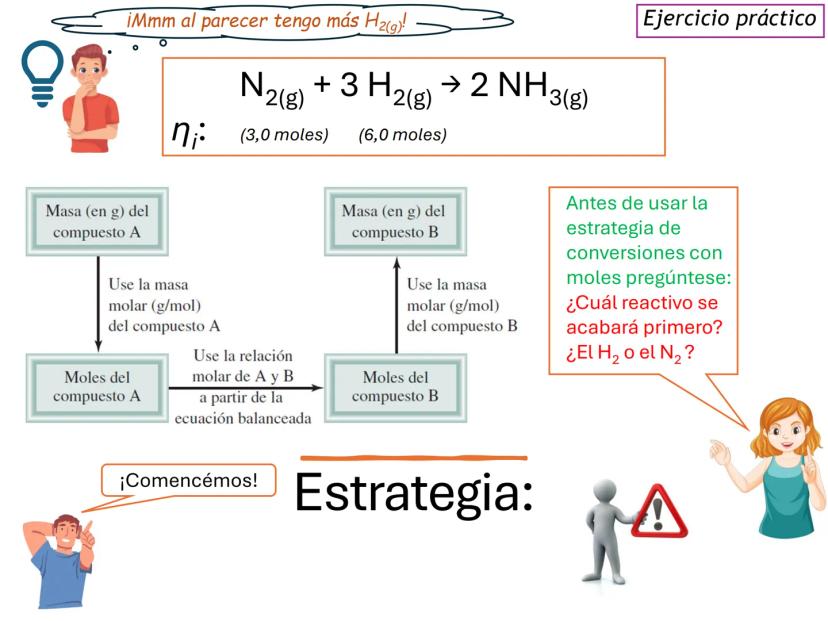
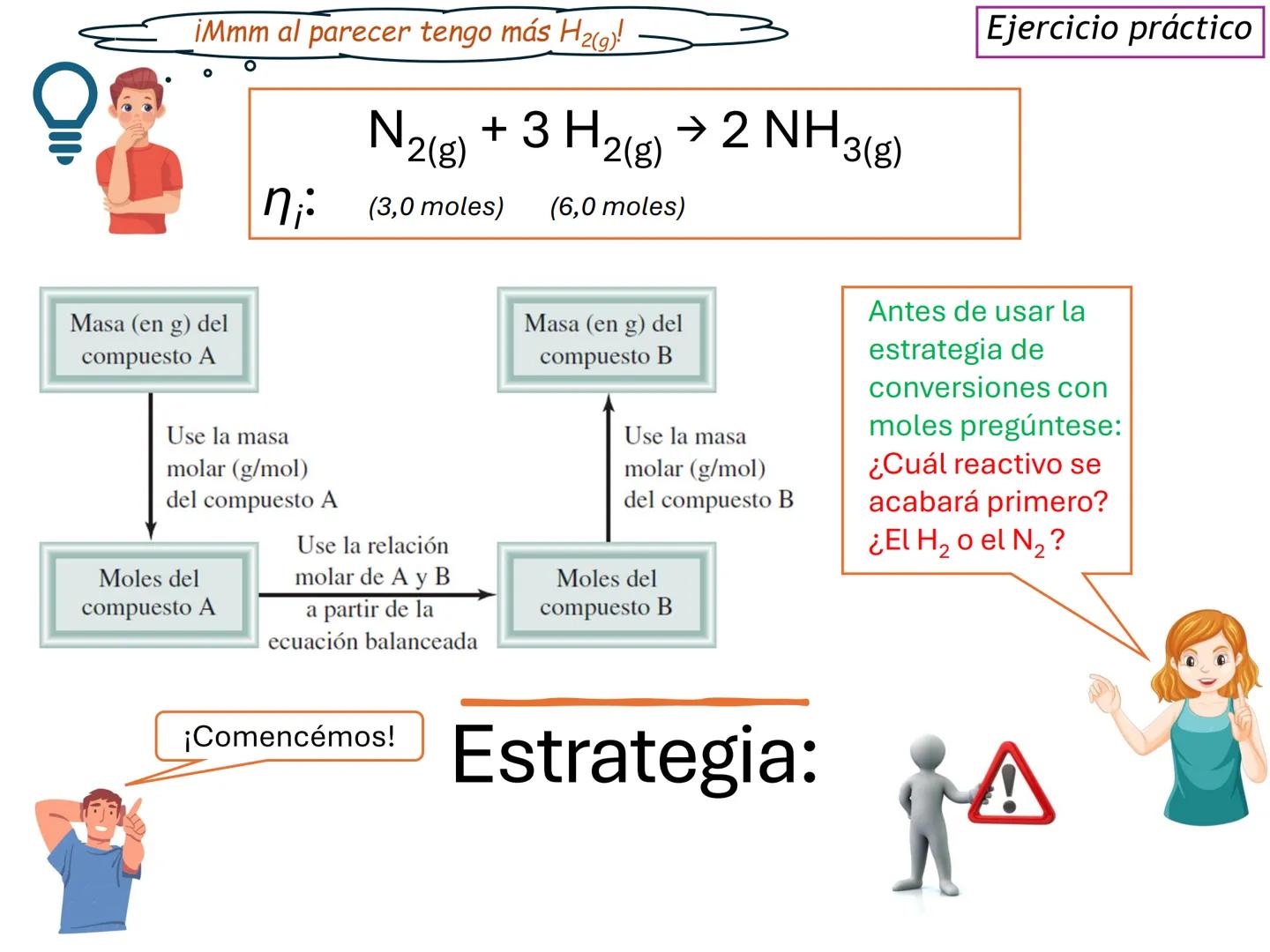
Para resolver problemas estequiométricos, necesitamos seguir una estrategia sistemática que conecte la masa del compuesto A con la masa del compuesto B que queremos encontrar.
Esta estrategia implica convertir masa a moles usando la masa molar, aplicar la relación molar de la ecuación balanceada, y luego convertir nuevamente a masa si es necesario.
¡Consejo útil! Dibuja un diagrama de flujo para tus conversiones: masa A → moles A → moles B → masa B. ¡Te ayudará a no perderte en los cálculos!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Para calcular la masa de agua que se produce a partir de 1.00 g de glucosa, utilizamos factores de conversión en secuencia para transformar unidades.
Primero convertimos gramos de glucosa a moles: $1.00g~C_{6}H_{12}O_{6} \times \frac{1~mol~C_{6}H_{12}O_{6}}{180.0~g~C_{6}H_{12}O_{6}} = 5.56 \times 10^{-3}~mol~C_{6}H_{12}O_{6}$
Luego, usamos la relación estequiométrica para calcular moles de agua: $5.56 \times 10^{-3}~mol~C_{6}H_{12}O_{6} \times \frac{6~mol~H_{2}O}{1~mol~C_{6}H_{12}O_{6}} = 3.33 \times 10^{-2}~mol~H_{2}O$
Finalmente, convertimos moles de agua a gramos: $3.33 \times 10^{-2}~mol~H_{2}O \times \frac{18.0~g~H_{2}O}{1~mol~H_{2}O} = 0.600~g~H_{2}O$
¡Fíjate bien! No existe una conversión directa de gramos de glucosa a gramos de agua. Siempre debes pasar por los moles y usar la relación estequiométrica.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Para calcular cuánta agua se produce a partir de 1.00 g de glucosa en la reacción , usamos factores de conversión encadenados.
Este método nos permite hacer la conversión en un solo cálculo:
Cada factor de conversión tiene un propósito: el primero convierte a moles, el segundo aplica la relación estequiométrica, y el tercero convierte de vuelta a gramos.
¡Simplifica tu trabajo! Organiza todos los factores de conversión en una sola línea para reducir errores y ver claramente la conexión entre lo que tienes y lo que buscas.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
En la reacción , debemos determinar cuánta masa de óxido de hierro(III) se necesita para producir 10.0 g de hierro metálico.
Para resolver este problema, necesitamos convertir la masa de hierro a moles, usar la relación estequiométrica para calcular moles de óxido de hierro, y finalmente convertir a gramos.
También se nos pide calcular la masa de dióxido de carbono producida, lo que requiere un procedimiento similar usando la relación entre hierro y CO₂ según la ecuación balanceada.
¡Ponte a prueba! Este ejercicio te permitirá practicar las conversiones estequiométricas. Recuerda verificar tus unidades en cada paso para asegurar un resultado correcto.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
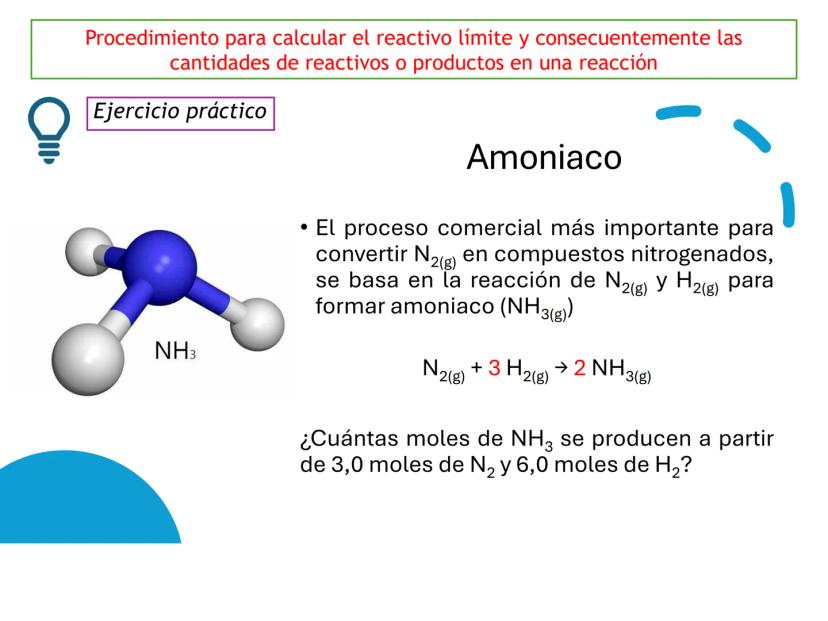
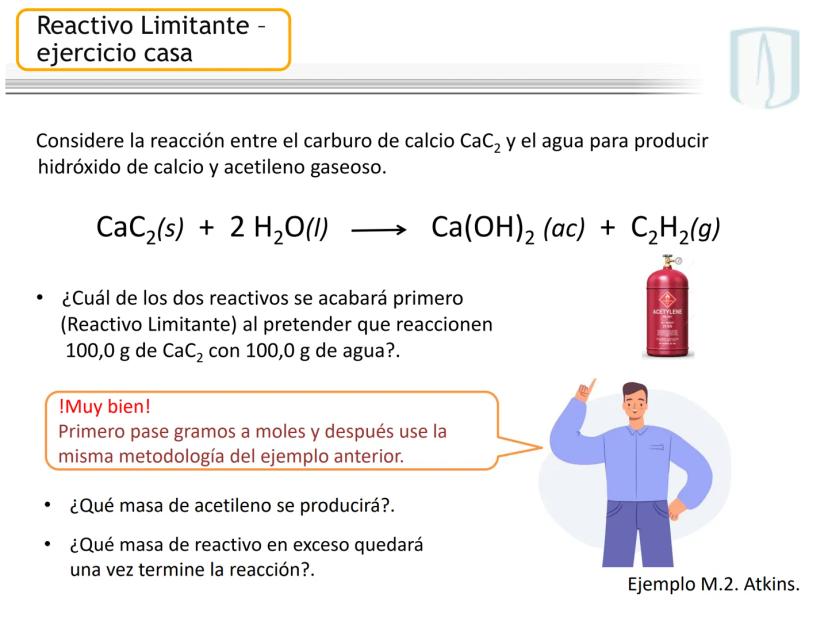
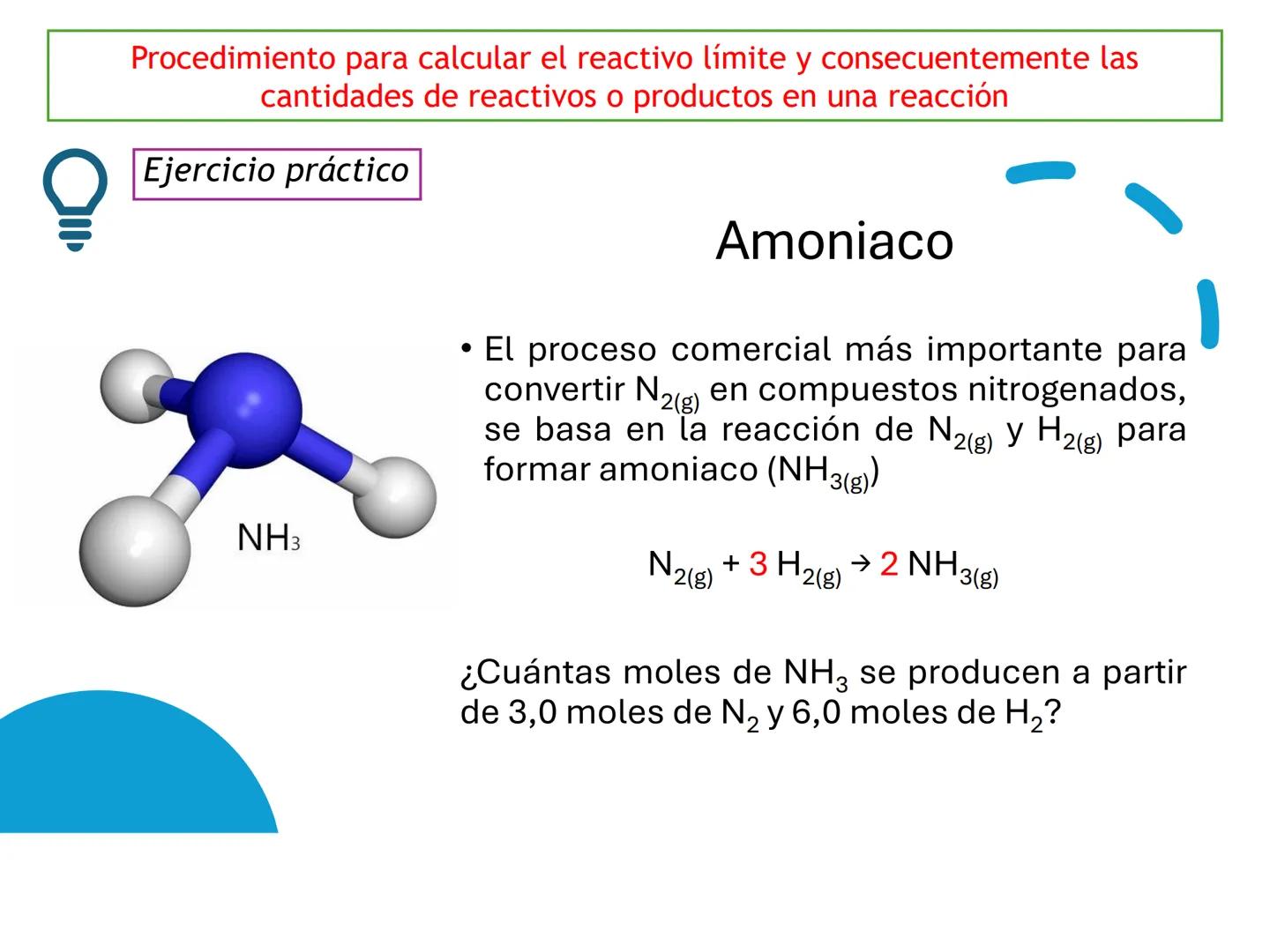
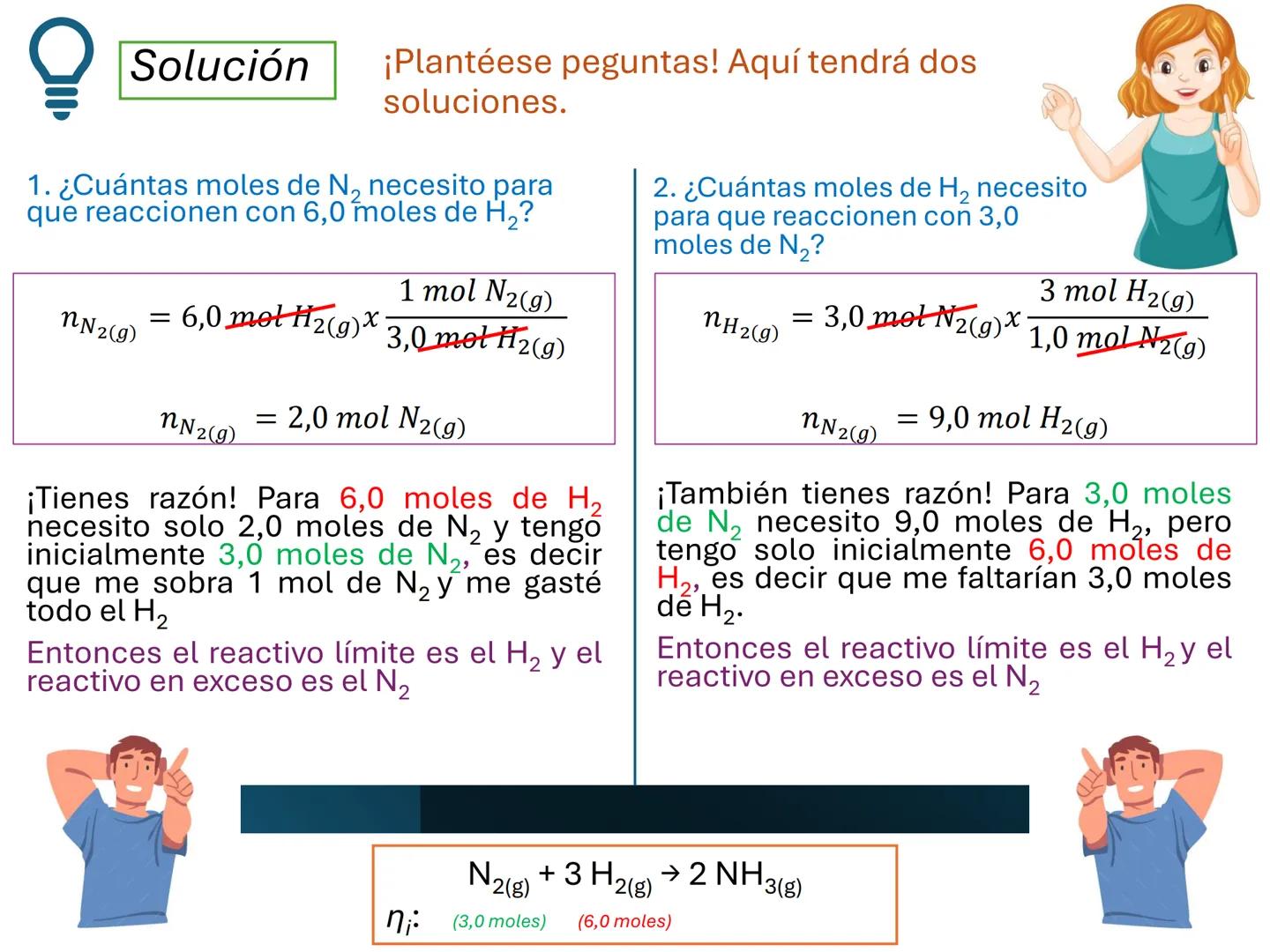
Cuando una reacción química involucra dos o más reactivos que no están en sus proporciones estequiométricas exactas, uno de ellos se agotará antes que los demás, determinando así el final de la reacción.
El reactivo limitante es aquel que se consume completamente y determina la cantidad máxima de producto que se puede formar. Los demás reactivos quedarán parcialmente sin reaccionar.
Es como preparar brownies: si una receta requiere 2 huevos y una caja de mezcla, y tienes 10 huevos pero solo 2 cajas, podrás hacer solamente 2 tandas de brownies porque las cajas son el reactivo limitante.
¡Importante! Identificar el reactivo limitante es fundamental para calcular correctamente el rendimiento de una reacción. ¡Siempre debes basarte en él para tus cálculos!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
17
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Fichas Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS