La química es la ciencia que estudia la materia, sus... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
24
•
Actualizado Apr 19, 2026
•
Luis David Angel Meza
@luisdavidangelm
La química es la ciencia que estudia la materia, sus... Mostrar más






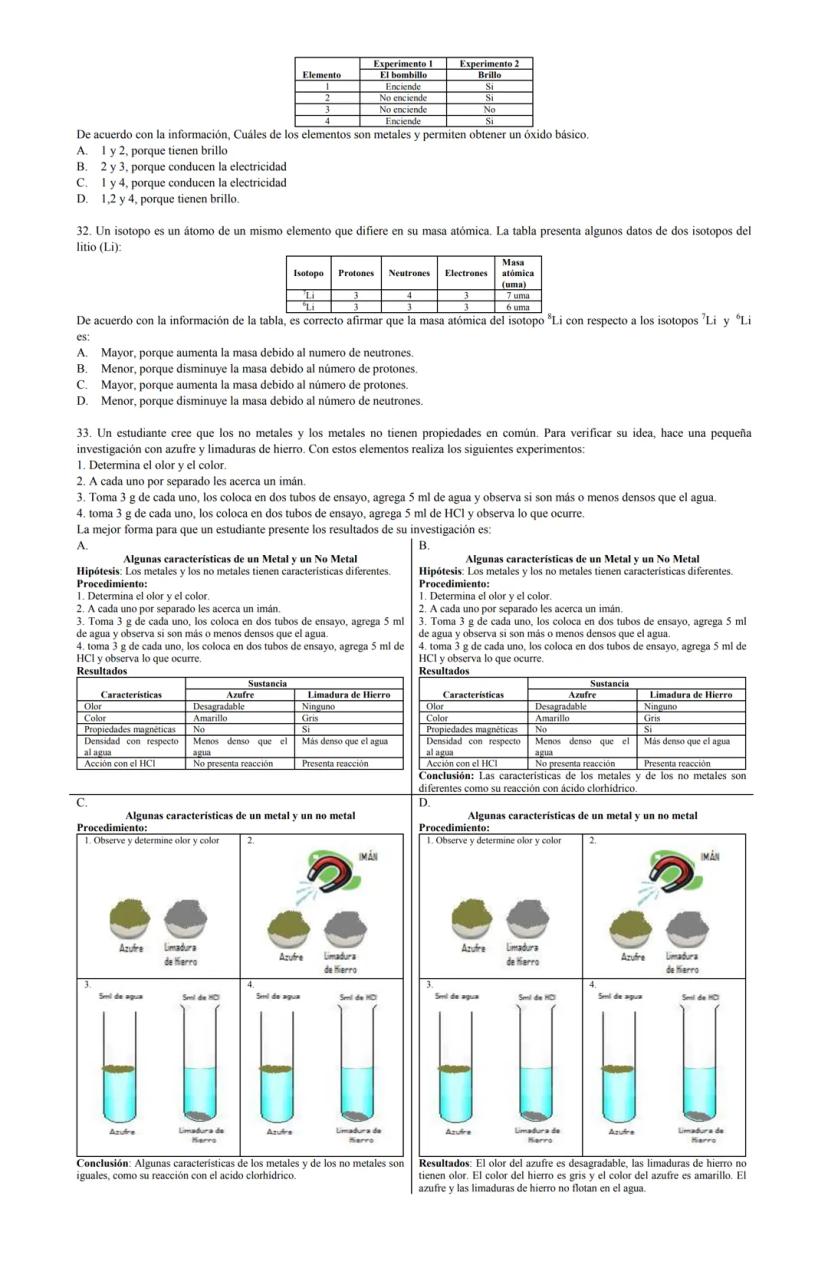




Los indicadores químicos son sustancias que cambian de color en presencia de ácidos o bases, permitiéndonos identificar el carácter de una sustancia. La fenolftaleína, por ejemplo, se torna rosa en medio básico y permanece incolora en medio ácido.
Al realizar pruebas con diferentes indicadores como la fenolftaleína y el papel tornasol, podemos clasificar sustancias cotidianas. Las sustancias ácidas como el vinagre y el zumo de limón mantienen incolora la fenolftaleína y vuelven rojo el papel tornasol azul. Por otro lado, las sustancias básicas como la leche de magnesia y limpiahornos tornan rosa la fenolftaleína y mantienen azul el papel tornasol.
Para comunicar adecuadamente los resultados de una investigación química, es importante presentar los patrones de coloración de manera organizada, incluyendo una clara explicación de las conclusiones obtenidas.
💡 Dato clave: Los ácidos y bases se pueden identificar fácilmente sin necesidad de equipos costosos, solo con indicadores como la fenolftaleína o el papel tornasol, ¡materiales accesibles para experimentos caseros!
Cuando trabajas con sustancias químicas, especialmente ácidos corrosivos como el ácido sulfúrico, debes utilizar recipientes de vidrio y trabajar en espacios bien ventilados para garantizar tu seguridad.

La estequiometría nos permite calcular las cantidades de reactivos y productos en una reacción química. Utilizando las masas molares de los elementos, podemos determinar cuánto producto se formará a partir de una cantidad específica de reactivo.
Por ejemplo, en la combustión del propano $C_3H_8 + 5O_2 \longrightarrow 3CO_2 + 4H_2O$, si quemamos 10g de propano, necesitamos aplicar las relaciones molares y las masas atómicas para calcular cuánto dióxido de carbono produciremos.
Las soluciones también pueden expresarse en diferentes unidades de concentración. En una solución de pigmento en pintura, por ejemplo, si la concentración es 1% p/v y se diluye 10 veces, la nueva concentración será 0,1% p/v, es decir, 1g de pigmento por litro.
💡 Dato práctico: Para resolver problemas de estequiometría, siempre convierte primero las masas en moles usando las masas molares, luego utiliza la proporción de la ecuación balanceada, y finalmente vuelve a convertir a gramos si es necesario.
El carácter químico o físico de un cambio depende de si se forman nuevas sustancias. Agregar un pigmento a una pintura es un cambio físico, ya que solo modifica la apariencia sin crear nuevos compuestos. El pigmento simplemente absorbe ciertas longitudes de onda de la luz, alterando el color percibido.

La solubilidad es la capacidad de una sustancia para disolverse en un solvente a determinada temperatura y presión. Este fenómeno varía significativamente entre diferentes sustancias y puede ser afectado por varios factores.
La temperatura ejerce efectos diferentes según el tipo de sustancia. Para la mayoría de los sólidos como el nitrato de plata (AgNO₃) o el cloruro de potasio (KCl), su solubilidad aumenta al incrementar la temperatura. Sin embargo, los gases como el oxígeno (O₂), dióxido de carbono (CO₂) y helio (He) muestran el comportamiento opuesto: su solubilidad disminuye al aumentar la temperatura.
La presión también influye significativamente en la solubilidad, especialmente en los gases. Según la Ley de Henry, la solubilidad de un gas es directamente proporcional a la presión e inversamente proporcional a la temperatura.
💡 Aplicación práctica: ¿Sabías que las bebidas gaseosas se embotellan a alta presión y baja temperatura para maximizar la cantidad de CO₂ disuelto? Al abrir la botella, la presión disminuye y el gas escapa formando burbujas.
Los principios de conservación de la materia se aplican en todas las reacciones químicas. Cuando ocurre una reacción química como la de cinc con ácido clorhídrico , la masa total se mantiene constante, aunque parte del hidrógeno se escape como gas. Esto demuestra que en un sistema cerrado, la materia no se crea ni se destruye, solo se transforma.

El agua presenta propiedades físicas que la distinguen de la mayoría de las sustancias. A diferencia de muchos compuestos, el agua en estado sólido (hielo) es menos densa que en estado líquido, lo que explica por qué el hielo flota.
Observando la tabla de densidades del agua a diferentes temperaturas, notamos que alcanza su máxima densidad a 4°C y disminuye tanto a temperaturas mayores como menores. Esta anomalía tiene importantes consecuencias para la vida acuática, ya que permite que los lagos se congelen desde la superficie hacia abajo, protegiendo la vida en las profundidades.
La estructura atómica determina las propiedades de los elementos. Un átomo con 8 protones, 8 neutrones y 8 electrones corresponde al oxígeno, con número atómico 8 y masa atómica de 16 uma. El número atómico siempre equivale al número de protones, mientras que la masa atómica es aproximadamente la suma de protones y neutrones.
💡 Concepto clave: La densidad anómala del agua es fundamental para la vida en la Tierra. Si el hielo fuera más denso que el agua líquida, los cuerpos de agua se congelarían desde el fondo, haciendo imposible la vida acuática en climas fríos.
La solubilidad puede expresarse en diferentes unidades de concentración. Para una solución de nitrato de potasio (KNO₃) a 80°C, si se disuelven 170g en 100g de agua, su concentración porcentual en masa es aproximadamente 63%. Esta concentración relaciona los gramos de soluto con los gramos totales de solución .

Los gases responden a cambios en temperatura, presión y volumen de manera predecible. La ley de Charles establece que a presión constante, el volumen de un gas es directamente proporcional a su temperatura absoluta.
Cuando aumentamos la temperatura de un gas en un pistón manteniendo constante la presión, observamos que su volumen aumenta. Esta relación directamente proporcional explica por qué los globos aerostáticos se elevan al calentar el aire en su interior.
Las configuraciones electrónicas determinan cómo los átomos forman enlaces químicos. El flúor, con número atómico 9 y configuración 1s²2s²2p⁵, al enlazarse con el sodio recibe un electrón para completar su octeto, quedando con configuración 1s²2s²2p⁶, similar a la del neón.
💡 Truco para recordar: Para las leyes de los gases, recuerda que "a mayor temperatura, mayor volumen" (si la presión es constante), y "a mayor presión, menor volumen" (si la temperatura es constante).
Los métodos de separación como la destilación, evaporación, filtración y decantación permiten separar los componentes de una mezcla basándose en sus propiedades físicas. Para separar sal disuelta en agua, el método más apropiado es la destilación, que permite obtener tanto la sal como el agua por separado, aprovechando los diferentes puntos de ebullición.

Los elementos químicos están organizados en la tabla periódica según sus propiedades. Los metales se caracterizan por ser buenos conductores de electricidad, tener brillo y ser generalmente maleables, mientras que los no metales tienen propiedades opuestas.
Un experimento para comparar metales y no metales podría incluir pruebas de conductividad eléctrica, reacción con ácidos, propiedades magnéticas y densidad. Por ejemplo, el hierro (metal) reacciona con ácido clorhídrico liberando hidrógeno, mientras que el azufre (no metal) no reacciona.
En el equilibrio químico, los cambios en las concentraciones, temperaturas o presiones pueden desplazar la reacción. El principio de Le Châtelier establece que cuando se perturba un sistema en equilibrio, este reacciona para contrarrestar esa perturbación.
💡 Aplicación clínica: El equilibrio ácido-base en la sangre es crucial para la salud. Cuando el CO₂ aumenta en la sangre (acidosis), el equilibrio se desplaza para producir más iones bicarbonato (HCO₃⁻), ayudando a neutralizar el exceso de ácido.
En las reacciones entre átomos, los estados de oxidación se relacionan con la ganancia o pérdida de electrones. El hierro (Fe) en estado de oxidación +2 (Fe²⁺) ha perdido dos electrones de su nivel más externo, modificando su configuración electrónica original. Estos cambios son fundamentales en reacciones de corrosión, baterías y muchos procesos industriales.

Los enlaces químicos determinan las propiedades macroscópicas de las sustancias. En la molécula de agua, se forman enlaces covalentes porque el oxígeno y el hidrógeno comparten electrones de valencia para alcanzar una configuración electrónica más estable.
El agua forma enlaces covalentes porque el oxígeno, con 6 electrones de valencia, necesita 2 más para completar su octeto, mientras que cada hidrógeno necesita 1 más para alcanzar la configuración del helio. Esta compartición de electrones crea una molécula polar que explica las propiedades únicas del agua como su alto punto de ebullición.
Las reacciones químicas siempre deben estar balanceadas, lo que refleja el principio de conservación de la materia. Una ecuación como CH₄ + O₂ → CO₂ + H₂O no está balanceada porque el número de átomos de oxígeno e hidrógeno no coincide entre reactivos y productos.
💡 Consejo práctico: Para balancear ecuaciones químicas, cuenta primero los átomos de cada elemento en ambos lados y luego ajusta los coeficientes (no los subíndices) hasta igualar las cantidades.
Los métodos de separación de mezclas aprovechan las diferencias en las propiedades físicas de sus componentes. En una mezcla de limaduras de hierro, sal y arena con agua, solo la sal pasa a través del papel filtro por ser soluble en agua. Las limaduras de hierro, aunque pueden reaccionar con el agua, no se disuelven completamente, y la arena es insoluble.

La termodinámica estudia las transformaciones energéticas en las reacciones químicas. La entalpía (ΔH) indica si una reacción libera calor (exotérmica, ΔH<0) o absorbe calor (endotérmica, ΔH>0).
La energía libre de Gibbs (ΔG) determina la espontaneidad de una reacción a temperatura y presión constantes. Cuando ΔG es negativo, la reacción es espontánea; cuando es positivo, no es espontánea. Por ejemplo, la reacción entre CaO y HCl con ΔG=145.4 kJ es no espontánea, mientras que la combustión del carbono con ΔG=-394.4 kJ es espontánea.
La velocidad de reacción está influenciada por varios factores, siendo la temperatura uno de los más importantes. Un experimento con peróxido de hidrógeno demuestra que al aumentar la temperatura, la descomposición ocurre más rápidamente, reduciendo el tiempo de reacción de 15 a 5 minutos.
💡 Dato interesante: Muchas reacciones espontáneas (ΔG<0) ocurren muy lentamente debido a una alta energía de activación. Los catalizadores aceleran estas reacciones sin ser consumidos, siendo fundamentales en procesos industriales y biológicos.
La presión afecta significativamente el volumen de los gases. En un experimento con un émbolo, se observa que al aumentar la presión (añadiendo más libros), el volumen disminuye proporcionalmente, lo que ilustra la ley de Boyle: a temperatura constante, el volumen es inversamente proporcional a la presión.

La destilación fraccionada es un proceso crucial en la refinación del petróleo que permite separar sus componentes según sus diferentes puntos de ebullición. A medida que aumenta la temperatura en la torre de destilación, se van separando productos desde gases ligeros (a bajas temperaturas) hasta aceites pesados y parafina (a altas temperaturas).
Si el sistema de calentamiento de una torre de destilación se daña, limitando la temperatura máxima a 250°C, solo se podrían obtener los productos con puntos de ebullición inferiores a esa temperatura: gases, gasolina y queroseno. Los productos más pesados como diesel y aceites quedarían sin separar.
La solubilidad de compuestos orgánicos como los alcoholes en agua sigue patrones específicos. Para los alcoholes lineales, la solubilidad en agua disminuye a medida que aumenta la cadena de carbonos. Esto se debe al aumento del carácter apolar de la molécula con el incremento de la cadena hidrocarbonada.
💡 Aplicación práctica: El conocimiento de la solubilidad de diferentes alcoholes es fundamental en la industria farmacéutica, pues determina cómo se absorben y distribuyen los medicamentos en el cuerpo humano.
Los elementos químicos se organizan en la tabla periódica siguiendo patrones de propiedades. La electronegatividad, por ejemplo, aumenta de izquierda a derecha en un período. Los elementos con baja electronegatividad y alta conductividad suelen ser metales ubicados a la izquierda, mientras que los de alta electronegatividad y baja conductividad son no metales ubicados a la derecha.

En la química ambiental, entender las reacciones que ocurren en la atmósfera es crucial. La lluvia ácida se forma cuando óxidos de nitrógeno y azufre, producidos en procesos industriales, reaccionan con el agua atmosférica formando soluciones ácidas diluidas.
Estas lluvias ácidas deterioran estructuras como edificios y monumentos, especialmente aquellos construidos con materiales sensibles a los ácidos como el mármol o la caliza. También pueden dañar ecosistemas acuáticos y forestales al alterar el pH natural del agua y suelo.
El balanceo de ecuaciones químicas asegura que se cumpla el principio de conservación de la materia. Para la combustión del metano (CH₄), la ecuación CH₄ + O₂ → CO₂ + H₂O no está balanceada porque hay 4 átomos de hidrógeno en los reactivos pero solo 2 en los productos. La forma correcta sería CH₄ + 2O₂ → CO₂ + 2H₂O.
💡 Conexión interdisciplinaria: La química atmosférica conecta directamente con problemas ambientales globales. Comprender las reacciones que producen la lluvia ácida te ayudará a entender mejor otros fenómenos como el calentamiento global o el agujero de la capa de ozono.
La estructura de Lewis de una molécula muestra cómo se comparten los electrones en los enlaces covalentes. En la molécula de agua, cada átomo de hidrógeno comparte su único electrón con uno de los seis electrones de valencia del oxígeno, permitiendo que el hidrógeno complete su nivel energético y que el oxígeno se acerque a la regla del octeto.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
Luis David Angel Meza
@luisdavidangelm
La química es la ciencia que estudia la materia, sus propiedades, transformaciones y la energía involucrada en estos procesos. En este resumen, exploraremos conceptos fundamentales de química que te ayudarán a entender desde las reacciones ácido-base hasta el equilibrio químico,... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los indicadores químicos son sustancias que cambian de color en presencia de ácidos o bases, permitiéndonos identificar el carácter de una sustancia. La fenolftaleína, por ejemplo, se torna rosa en medio básico y permanece incolora en medio ácido.
Al realizar pruebas con diferentes indicadores como la fenolftaleína y el papel tornasol, podemos clasificar sustancias cotidianas. Las sustancias ácidas como el vinagre y el zumo de limón mantienen incolora la fenolftaleína y vuelven rojo el papel tornasol azul. Por otro lado, las sustancias básicas como la leche de magnesia y limpiahornos tornan rosa la fenolftaleína y mantienen azul el papel tornasol.
Para comunicar adecuadamente los resultados de una investigación química, es importante presentar los patrones de coloración de manera organizada, incluyendo una clara explicación de las conclusiones obtenidas.
💡 Dato clave: Los ácidos y bases se pueden identificar fácilmente sin necesidad de equipos costosos, solo con indicadores como la fenolftaleína o el papel tornasol, ¡materiales accesibles para experimentos caseros!
Cuando trabajas con sustancias químicas, especialmente ácidos corrosivos como el ácido sulfúrico, debes utilizar recipientes de vidrio y trabajar en espacios bien ventilados para garantizar tu seguridad.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La estequiometría nos permite calcular las cantidades de reactivos y productos en una reacción química. Utilizando las masas molares de los elementos, podemos determinar cuánto producto se formará a partir de una cantidad específica de reactivo.
Por ejemplo, en la combustión del propano $C_3H_8 + 5O_2 \longrightarrow 3CO_2 + 4H_2O$, si quemamos 10g de propano, necesitamos aplicar las relaciones molares y las masas atómicas para calcular cuánto dióxido de carbono produciremos.
Las soluciones también pueden expresarse en diferentes unidades de concentración. En una solución de pigmento en pintura, por ejemplo, si la concentración es 1% p/v y se diluye 10 veces, la nueva concentración será 0,1% p/v, es decir, 1g de pigmento por litro.
💡 Dato práctico: Para resolver problemas de estequiometría, siempre convierte primero las masas en moles usando las masas molares, luego utiliza la proporción de la ecuación balanceada, y finalmente vuelve a convertir a gramos si es necesario.
El carácter químico o físico de un cambio depende de si se forman nuevas sustancias. Agregar un pigmento a una pintura es un cambio físico, ya que solo modifica la apariencia sin crear nuevos compuestos. El pigmento simplemente absorbe ciertas longitudes de onda de la luz, alterando el color percibido.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La solubilidad es la capacidad de una sustancia para disolverse en un solvente a determinada temperatura y presión. Este fenómeno varía significativamente entre diferentes sustancias y puede ser afectado por varios factores.
La temperatura ejerce efectos diferentes según el tipo de sustancia. Para la mayoría de los sólidos como el nitrato de plata (AgNO₃) o el cloruro de potasio (KCl), su solubilidad aumenta al incrementar la temperatura. Sin embargo, los gases como el oxígeno (O₂), dióxido de carbono (CO₂) y helio (He) muestran el comportamiento opuesto: su solubilidad disminuye al aumentar la temperatura.
La presión también influye significativamente en la solubilidad, especialmente en los gases. Según la Ley de Henry, la solubilidad de un gas es directamente proporcional a la presión e inversamente proporcional a la temperatura.
💡 Aplicación práctica: ¿Sabías que las bebidas gaseosas se embotellan a alta presión y baja temperatura para maximizar la cantidad de CO₂ disuelto? Al abrir la botella, la presión disminuye y el gas escapa formando burbujas.
Los principios de conservación de la materia se aplican en todas las reacciones químicas. Cuando ocurre una reacción química como la de cinc con ácido clorhídrico , la masa total se mantiene constante, aunque parte del hidrógeno se escape como gas. Esto demuestra que en un sistema cerrado, la materia no se crea ni se destruye, solo se transforma.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El agua presenta propiedades físicas que la distinguen de la mayoría de las sustancias. A diferencia de muchos compuestos, el agua en estado sólido (hielo) es menos densa que en estado líquido, lo que explica por qué el hielo flota.
Observando la tabla de densidades del agua a diferentes temperaturas, notamos que alcanza su máxima densidad a 4°C y disminuye tanto a temperaturas mayores como menores. Esta anomalía tiene importantes consecuencias para la vida acuática, ya que permite que los lagos se congelen desde la superficie hacia abajo, protegiendo la vida en las profundidades.
La estructura atómica determina las propiedades de los elementos. Un átomo con 8 protones, 8 neutrones y 8 electrones corresponde al oxígeno, con número atómico 8 y masa atómica de 16 uma. El número atómico siempre equivale al número de protones, mientras que la masa atómica es aproximadamente la suma de protones y neutrones.
💡 Concepto clave: La densidad anómala del agua es fundamental para la vida en la Tierra. Si el hielo fuera más denso que el agua líquida, los cuerpos de agua se congelarían desde el fondo, haciendo imposible la vida acuática en climas fríos.
La solubilidad puede expresarse en diferentes unidades de concentración. Para una solución de nitrato de potasio (KNO₃) a 80°C, si se disuelven 170g en 100g de agua, su concentración porcentual en masa es aproximadamente 63%. Esta concentración relaciona los gramos de soluto con los gramos totales de solución .

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los gases responden a cambios en temperatura, presión y volumen de manera predecible. La ley de Charles establece que a presión constante, el volumen de un gas es directamente proporcional a su temperatura absoluta.
Cuando aumentamos la temperatura de un gas en un pistón manteniendo constante la presión, observamos que su volumen aumenta. Esta relación directamente proporcional explica por qué los globos aerostáticos se elevan al calentar el aire en su interior.
Las configuraciones electrónicas determinan cómo los átomos forman enlaces químicos. El flúor, con número atómico 9 y configuración 1s²2s²2p⁵, al enlazarse con el sodio recibe un electrón para completar su octeto, quedando con configuración 1s²2s²2p⁶, similar a la del neón.
💡 Truco para recordar: Para las leyes de los gases, recuerda que "a mayor temperatura, mayor volumen" (si la presión es constante), y "a mayor presión, menor volumen" (si la temperatura es constante).
Los métodos de separación como la destilación, evaporación, filtración y decantación permiten separar los componentes de una mezcla basándose en sus propiedades físicas. Para separar sal disuelta en agua, el método más apropiado es la destilación, que permite obtener tanto la sal como el agua por separado, aprovechando los diferentes puntos de ebullición.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los elementos químicos están organizados en la tabla periódica según sus propiedades. Los metales se caracterizan por ser buenos conductores de electricidad, tener brillo y ser generalmente maleables, mientras que los no metales tienen propiedades opuestas.
Un experimento para comparar metales y no metales podría incluir pruebas de conductividad eléctrica, reacción con ácidos, propiedades magnéticas y densidad. Por ejemplo, el hierro (metal) reacciona con ácido clorhídrico liberando hidrógeno, mientras que el azufre (no metal) no reacciona.
En el equilibrio químico, los cambios en las concentraciones, temperaturas o presiones pueden desplazar la reacción. El principio de Le Châtelier establece que cuando se perturba un sistema en equilibrio, este reacciona para contrarrestar esa perturbación.
💡 Aplicación clínica: El equilibrio ácido-base en la sangre es crucial para la salud. Cuando el CO₂ aumenta en la sangre (acidosis), el equilibrio se desplaza para producir más iones bicarbonato (HCO₃⁻), ayudando a neutralizar el exceso de ácido.
En las reacciones entre átomos, los estados de oxidación se relacionan con la ganancia o pérdida de electrones. El hierro (Fe) en estado de oxidación +2 (Fe²⁺) ha perdido dos electrones de su nivel más externo, modificando su configuración electrónica original. Estos cambios son fundamentales en reacciones de corrosión, baterías y muchos procesos industriales.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los enlaces químicos determinan las propiedades macroscópicas de las sustancias. En la molécula de agua, se forman enlaces covalentes porque el oxígeno y el hidrógeno comparten electrones de valencia para alcanzar una configuración electrónica más estable.
El agua forma enlaces covalentes porque el oxígeno, con 6 electrones de valencia, necesita 2 más para completar su octeto, mientras que cada hidrógeno necesita 1 más para alcanzar la configuración del helio. Esta compartición de electrones crea una molécula polar que explica las propiedades únicas del agua como su alto punto de ebullición.
Las reacciones químicas siempre deben estar balanceadas, lo que refleja el principio de conservación de la materia. Una ecuación como CH₄ + O₂ → CO₂ + H₂O no está balanceada porque el número de átomos de oxígeno e hidrógeno no coincide entre reactivos y productos.
💡 Consejo práctico: Para balancear ecuaciones químicas, cuenta primero los átomos de cada elemento en ambos lados y luego ajusta los coeficientes (no los subíndices) hasta igualar las cantidades.
Los métodos de separación de mezclas aprovechan las diferencias en las propiedades físicas de sus componentes. En una mezcla de limaduras de hierro, sal y arena con agua, solo la sal pasa a través del papel filtro por ser soluble en agua. Las limaduras de hierro, aunque pueden reaccionar con el agua, no se disuelven completamente, y la arena es insoluble.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La termodinámica estudia las transformaciones energéticas en las reacciones químicas. La entalpía (ΔH) indica si una reacción libera calor (exotérmica, ΔH<0) o absorbe calor (endotérmica, ΔH>0).
La energía libre de Gibbs (ΔG) determina la espontaneidad de una reacción a temperatura y presión constantes. Cuando ΔG es negativo, la reacción es espontánea; cuando es positivo, no es espontánea. Por ejemplo, la reacción entre CaO y HCl con ΔG=145.4 kJ es no espontánea, mientras que la combustión del carbono con ΔG=-394.4 kJ es espontánea.
La velocidad de reacción está influenciada por varios factores, siendo la temperatura uno de los más importantes. Un experimento con peróxido de hidrógeno demuestra que al aumentar la temperatura, la descomposición ocurre más rápidamente, reduciendo el tiempo de reacción de 15 a 5 minutos.
💡 Dato interesante: Muchas reacciones espontáneas (ΔG<0) ocurren muy lentamente debido a una alta energía de activación. Los catalizadores aceleran estas reacciones sin ser consumidos, siendo fundamentales en procesos industriales y biológicos.
La presión afecta significativamente el volumen de los gases. En un experimento con un émbolo, se observa que al aumentar la presión (añadiendo más libros), el volumen disminuye proporcionalmente, lo que ilustra la ley de Boyle: a temperatura constante, el volumen es inversamente proporcional a la presión.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La destilación fraccionada es un proceso crucial en la refinación del petróleo que permite separar sus componentes según sus diferentes puntos de ebullición. A medida que aumenta la temperatura en la torre de destilación, se van separando productos desde gases ligeros (a bajas temperaturas) hasta aceites pesados y parafina (a altas temperaturas).
Si el sistema de calentamiento de una torre de destilación se daña, limitando la temperatura máxima a 250°C, solo se podrían obtener los productos con puntos de ebullición inferiores a esa temperatura: gases, gasolina y queroseno. Los productos más pesados como diesel y aceites quedarían sin separar.
La solubilidad de compuestos orgánicos como los alcoholes en agua sigue patrones específicos. Para los alcoholes lineales, la solubilidad en agua disminuye a medida que aumenta la cadena de carbonos. Esto se debe al aumento del carácter apolar de la molécula con el incremento de la cadena hidrocarbonada.
💡 Aplicación práctica: El conocimiento de la solubilidad de diferentes alcoholes es fundamental en la industria farmacéutica, pues determina cómo se absorben y distribuyen los medicamentos en el cuerpo humano.
Los elementos químicos se organizan en la tabla periódica siguiendo patrones de propiedades. La electronegatividad, por ejemplo, aumenta de izquierda a derecha en un período. Los elementos con baja electronegatividad y alta conductividad suelen ser metales ubicados a la izquierda, mientras que los de alta electronegatividad y baja conductividad son no metales ubicados a la derecha.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
En la química ambiental, entender las reacciones que ocurren en la atmósfera es crucial. La lluvia ácida se forma cuando óxidos de nitrógeno y azufre, producidos en procesos industriales, reaccionan con el agua atmosférica formando soluciones ácidas diluidas.
Estas lluvias ácidas deterioran estructuras como edificios y monumentos, especialmente aquellos construidos con materiales sensibles a los ácidos como el mármol o la caliza. También pueden dañar ecosistemas acuáticos y forestales al alterar el pH natural del agua y suelo.
El balanceo de ecuaciones químicas asegura que se cumpla el principio de conservación de la materia. Para la combustión del metano (CH₄), la ecuación CH₄ + O₂ → CO₂ + H₂O no está balanceada porque hay 4 átomos de hidrógeno en los reactivos pero solo 2 en los productos. La forma correcta sería CH₄ + 2O₂ → CO₂ + 2H₂O.
💡 Conexión interdisciplinaria: La química atmosférica conecta directamente con problemas ambientales globales. Comprender las reacciones que producen la lluvia ácida te ayudará a entender mejor otros fenómenos como el calentamiento global o el agujero de la capa de ozono.
La estructura de Lewis de una molécula muestra cómo se comparten los electrones en los enlaces covalentes. En la molécula de agua, cada átomo de hidrógeno comparte su único electrón con uno de los seis electrones de valencia del oxígeno, permitiendo que el hidrógeno complete su nivel energético y que el oxígeno se acerque a la regla del octeto.
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
0
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Fichas Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS