Las tablas de propiedades termodinámicas son herramientas esenciales para resolver... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
24
•
Actualizado May 18, 2026
•
Danna Contreras
@dannacont_qqt8s
Las tablas de propiedades termodinámicas son herramientas esenciales para resolver... Mostrar más



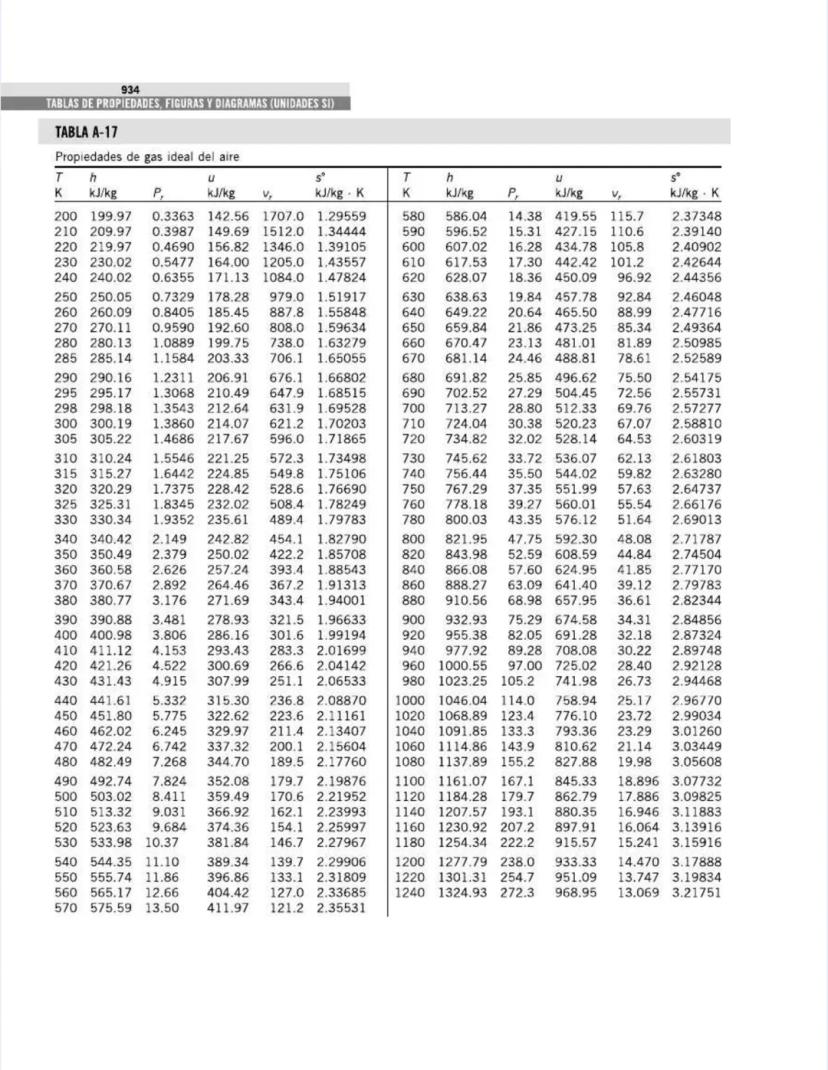
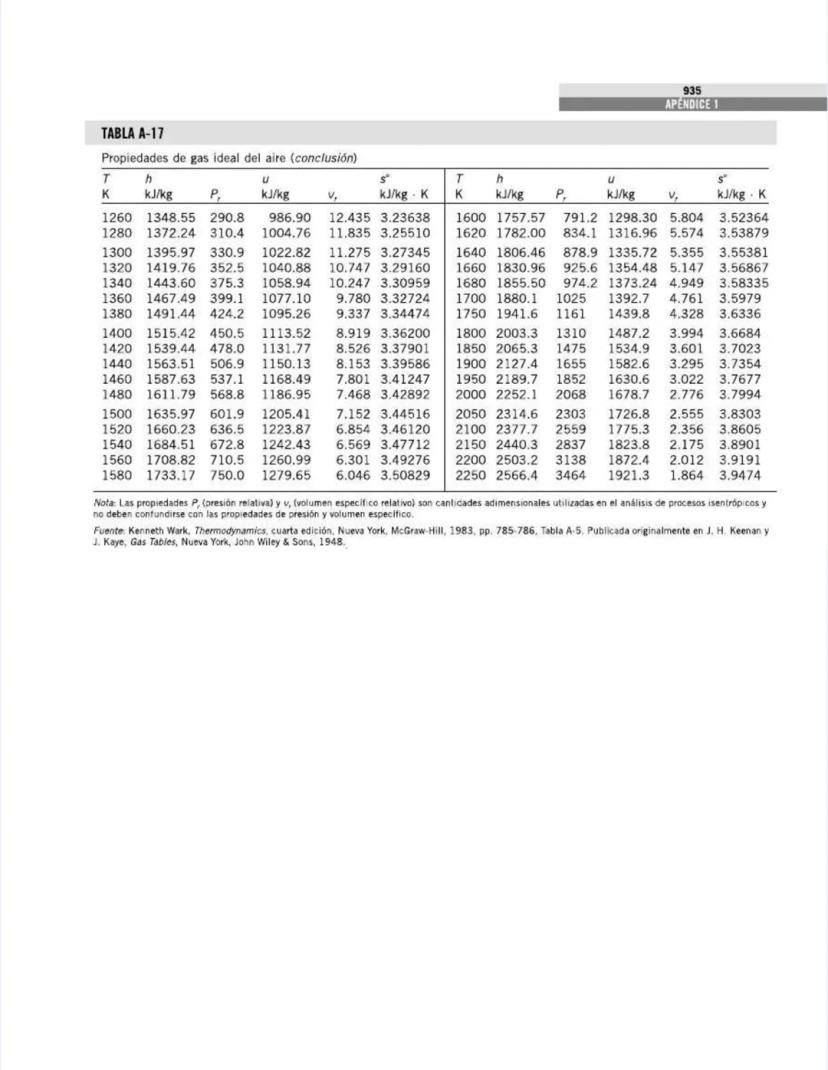
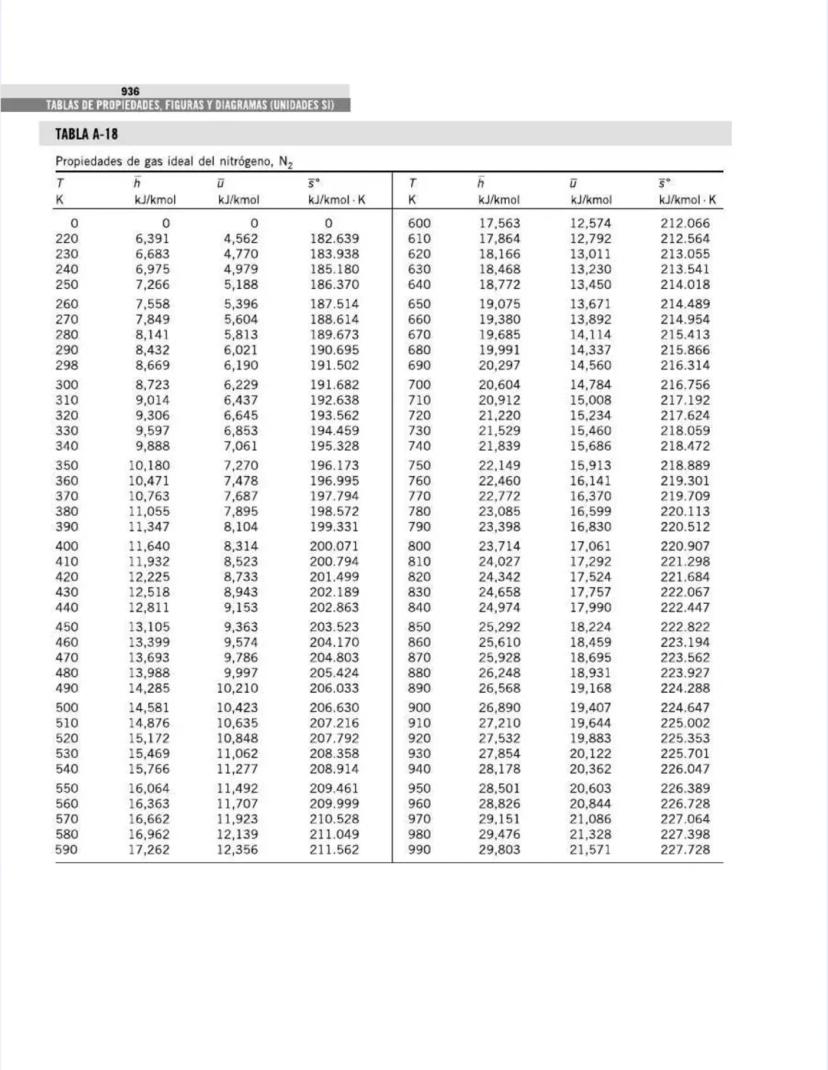
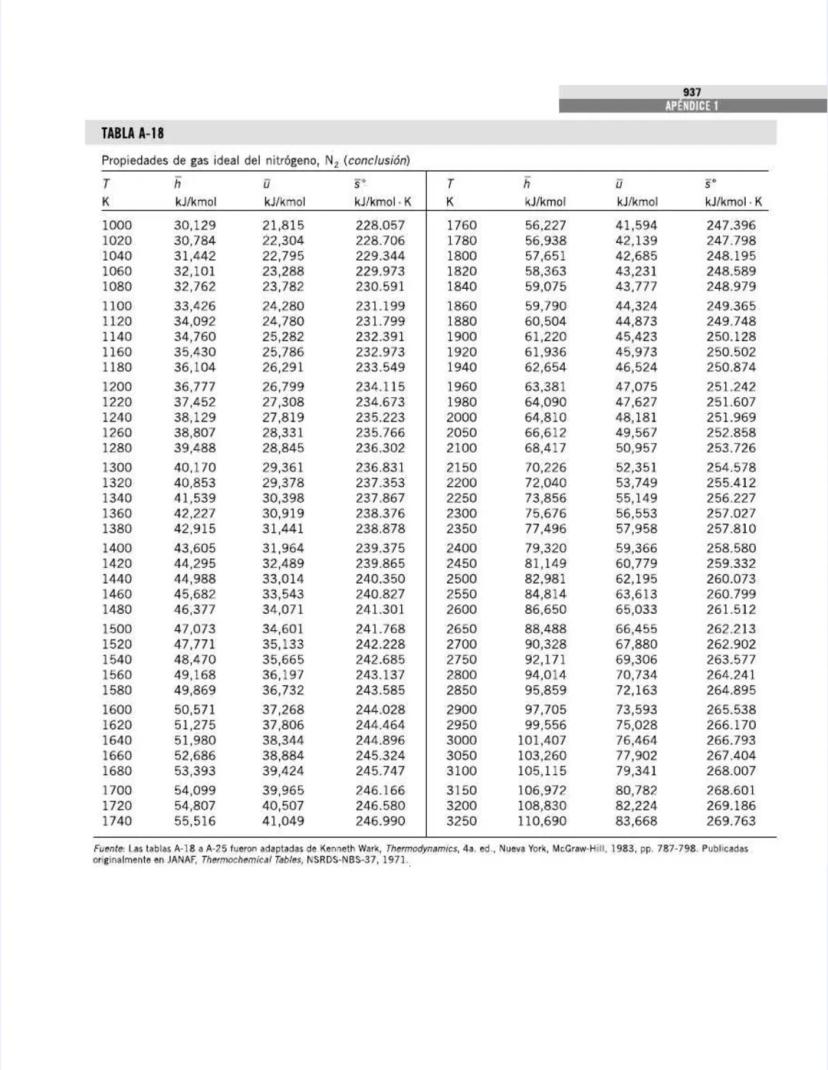
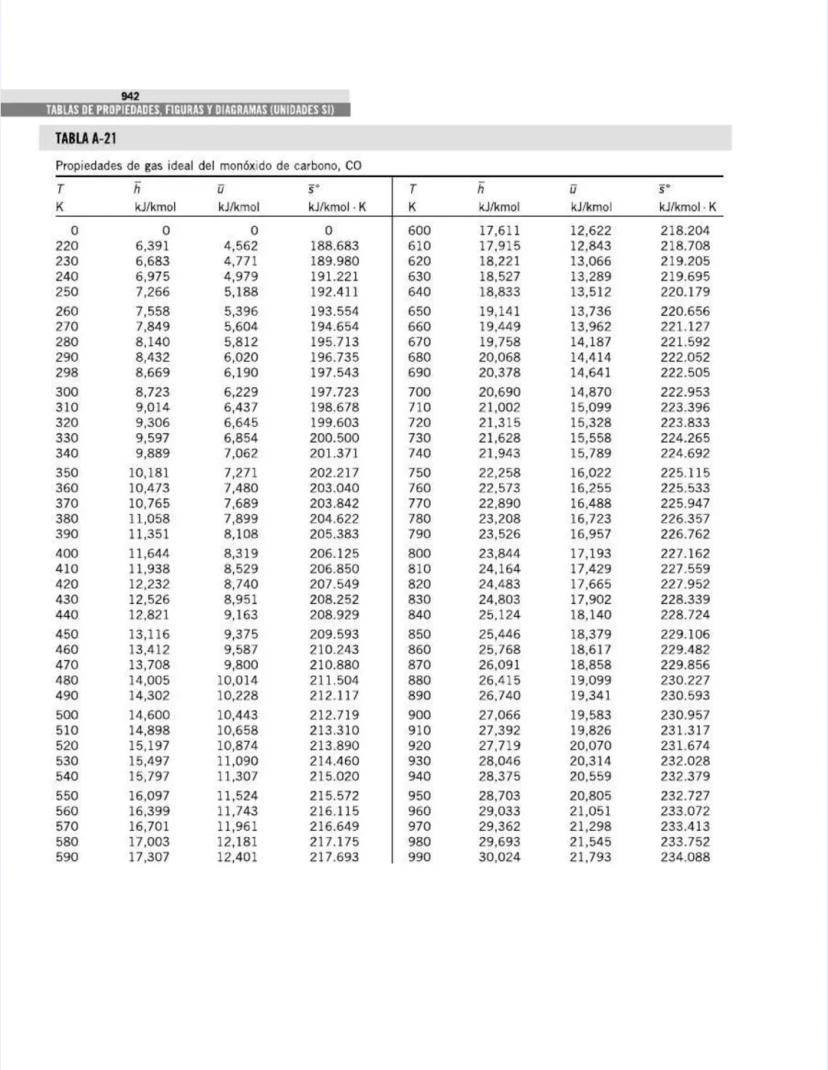
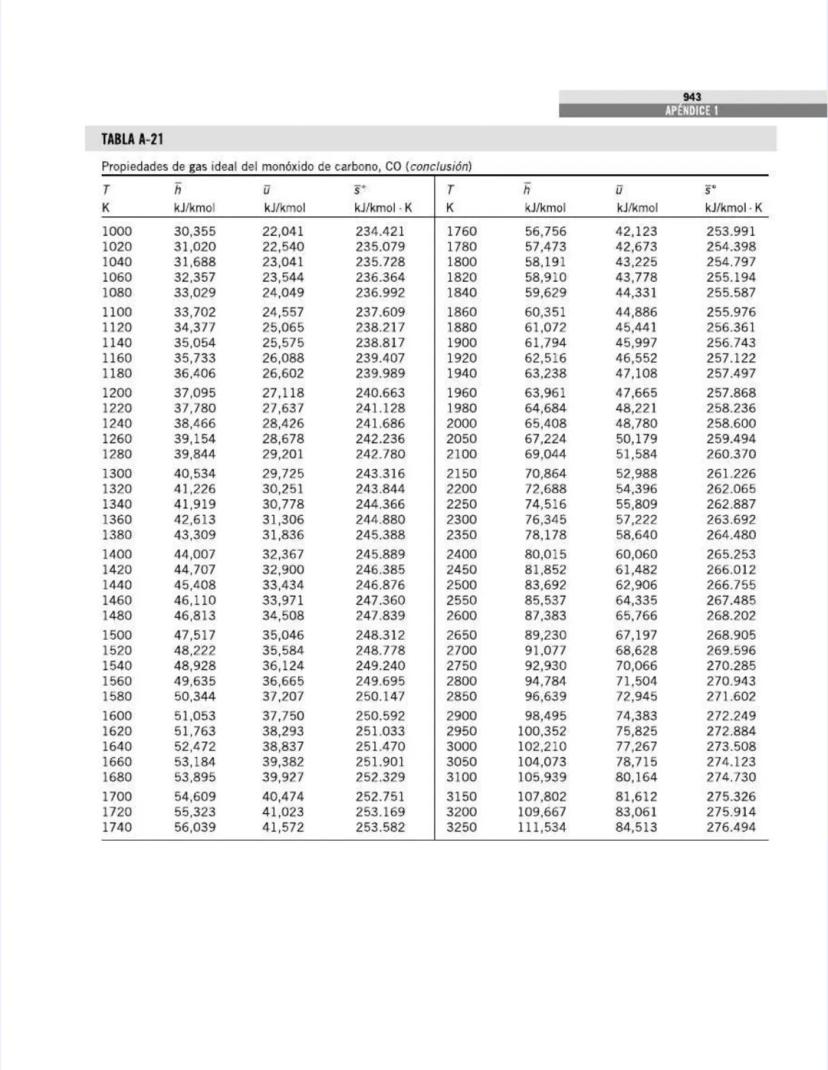
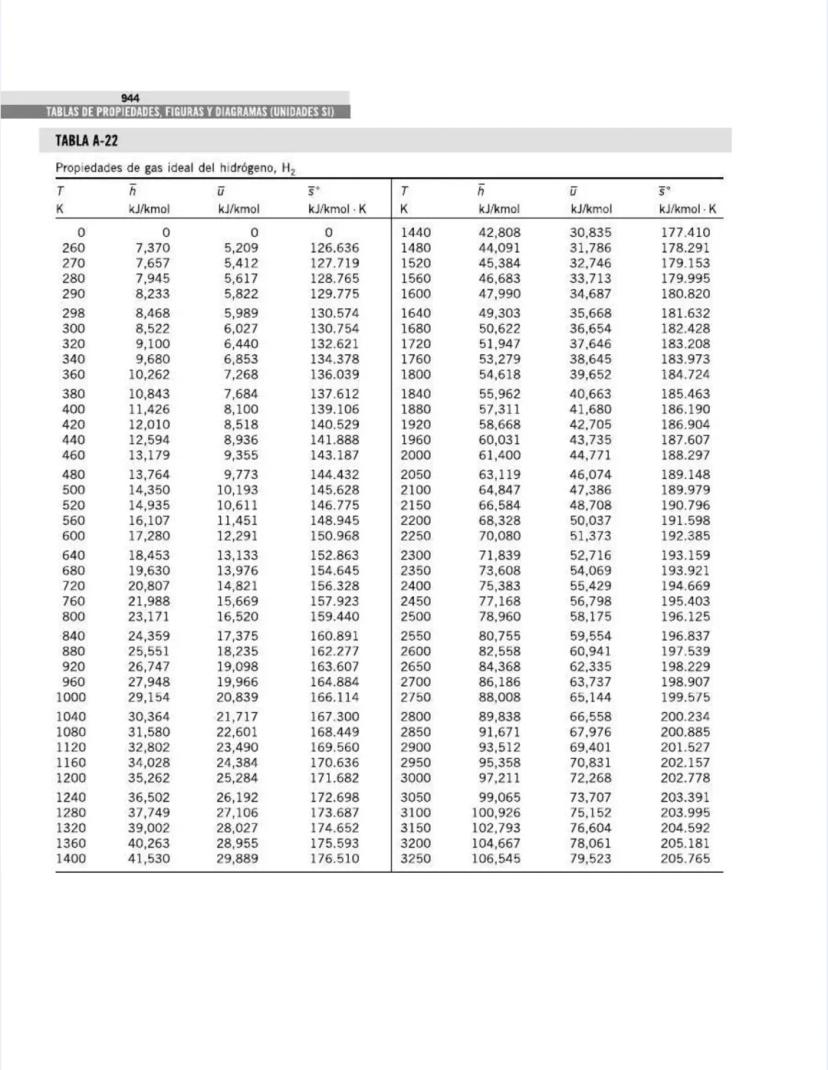
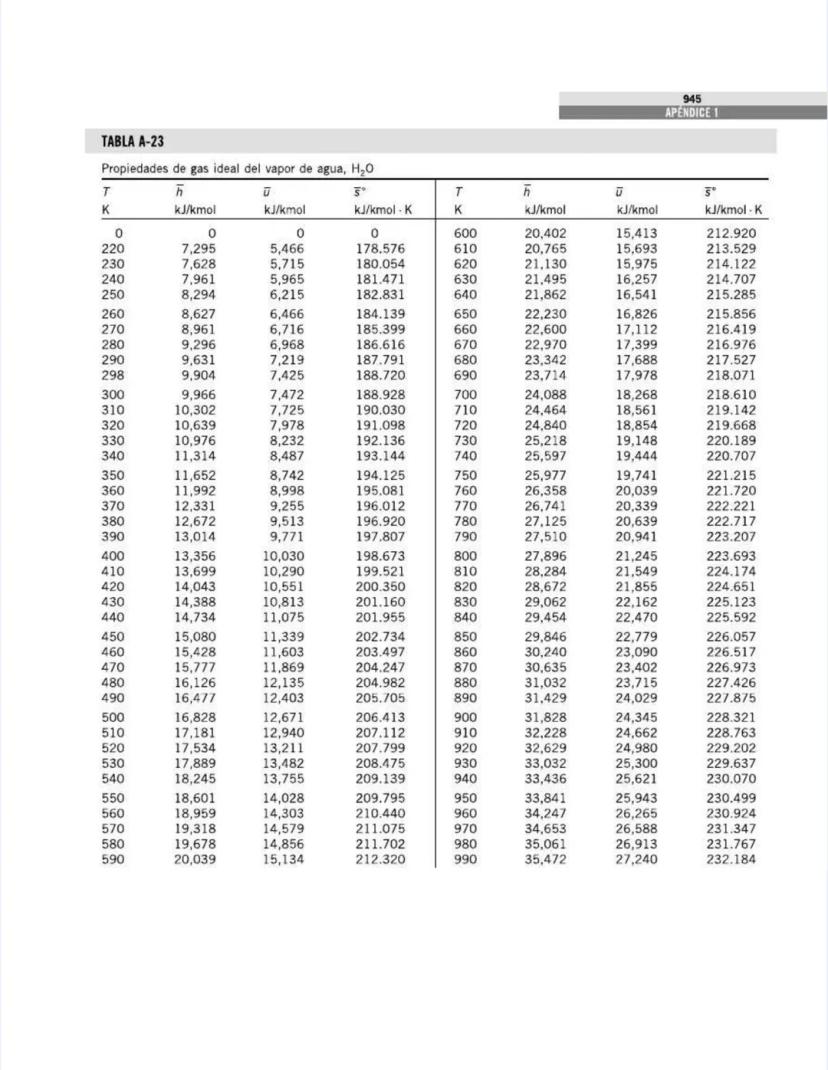
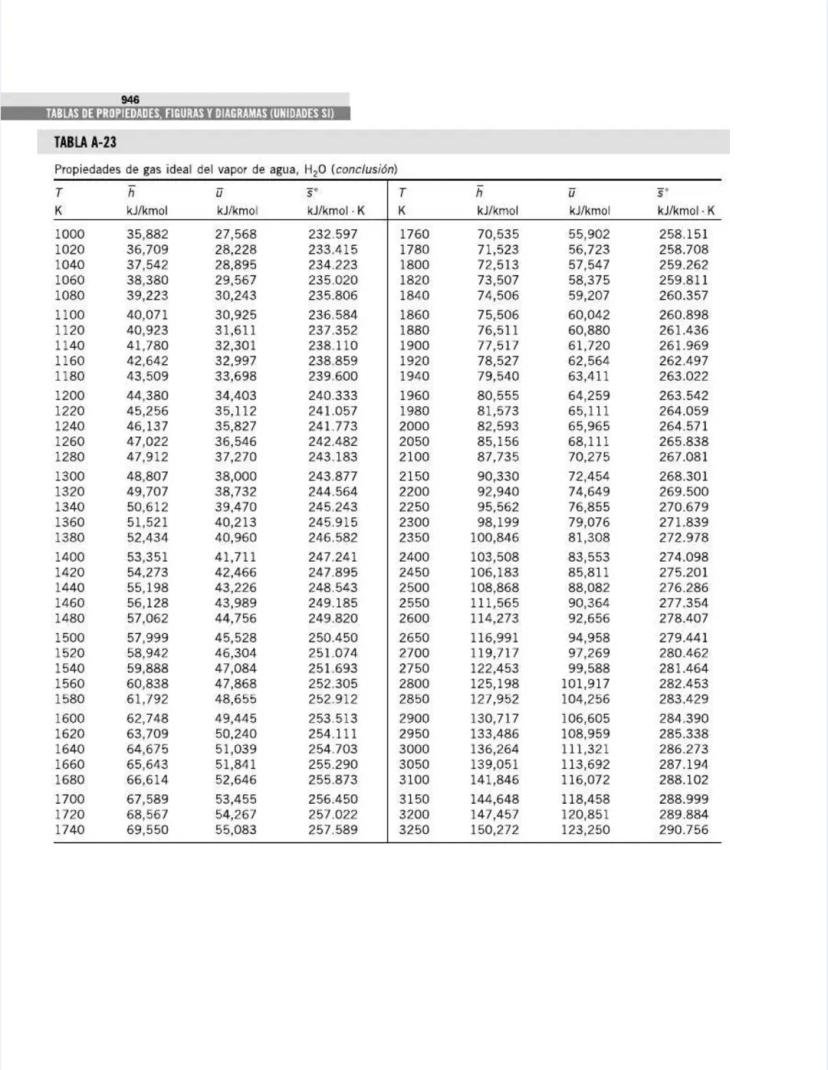
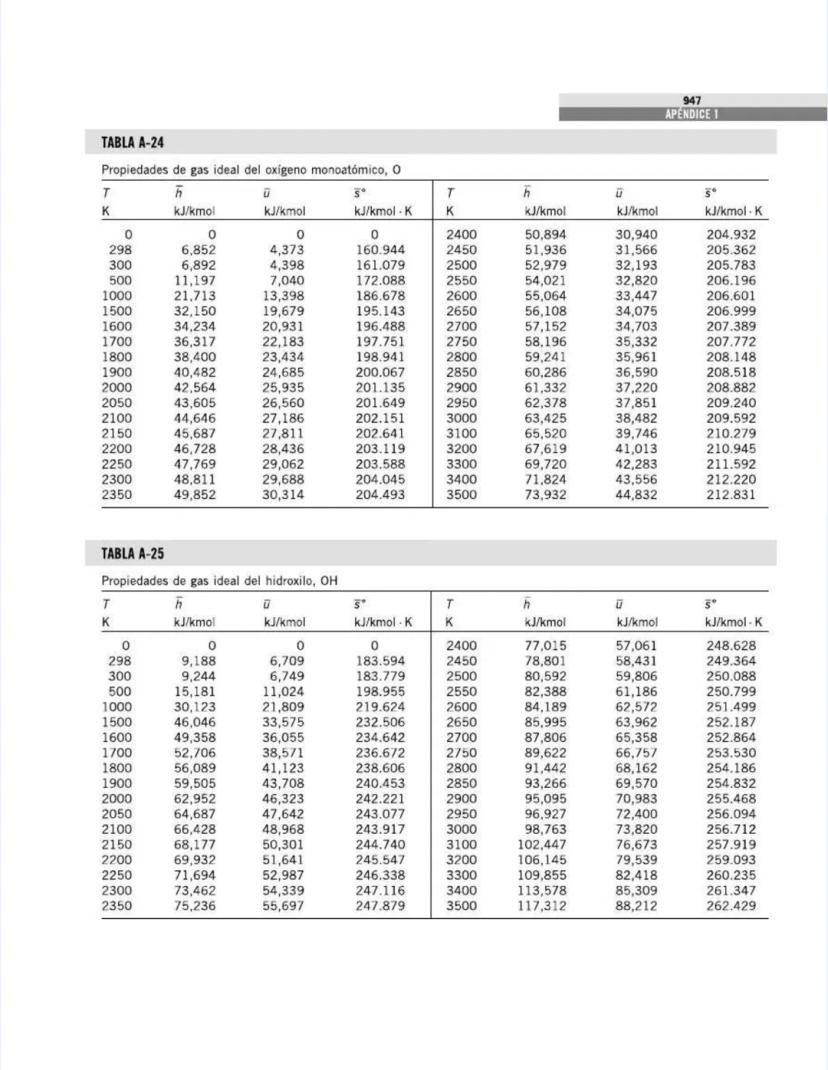
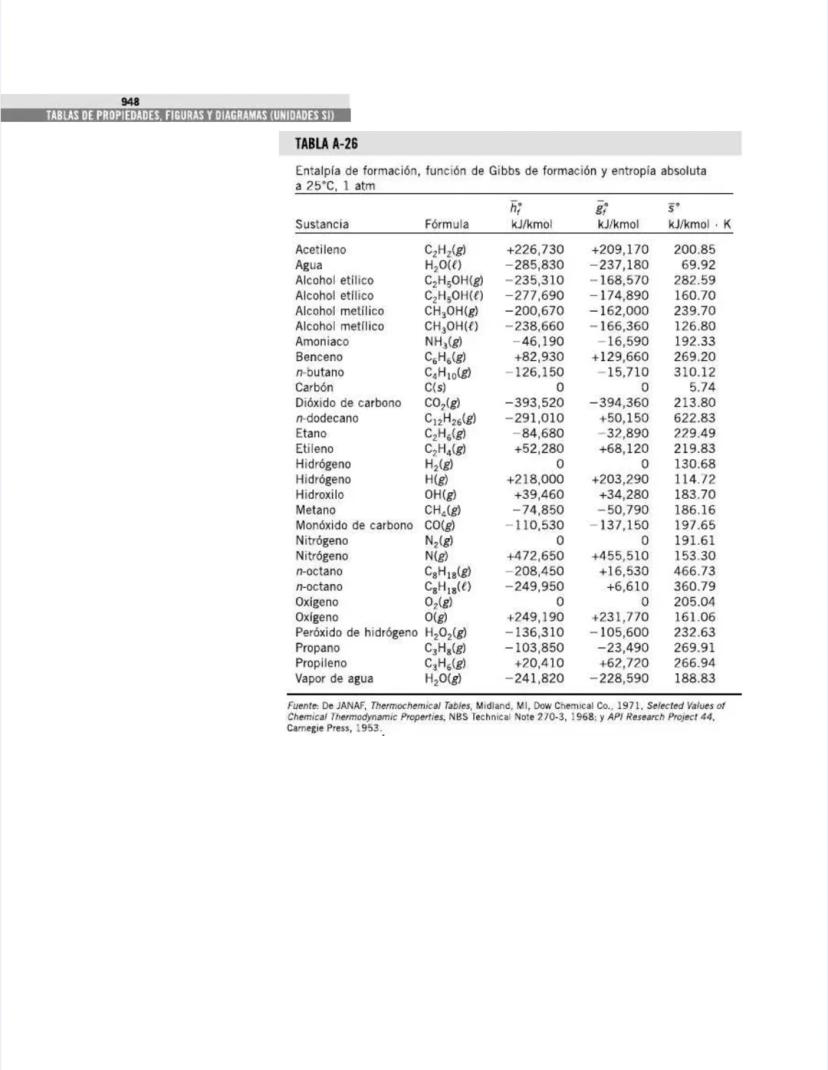
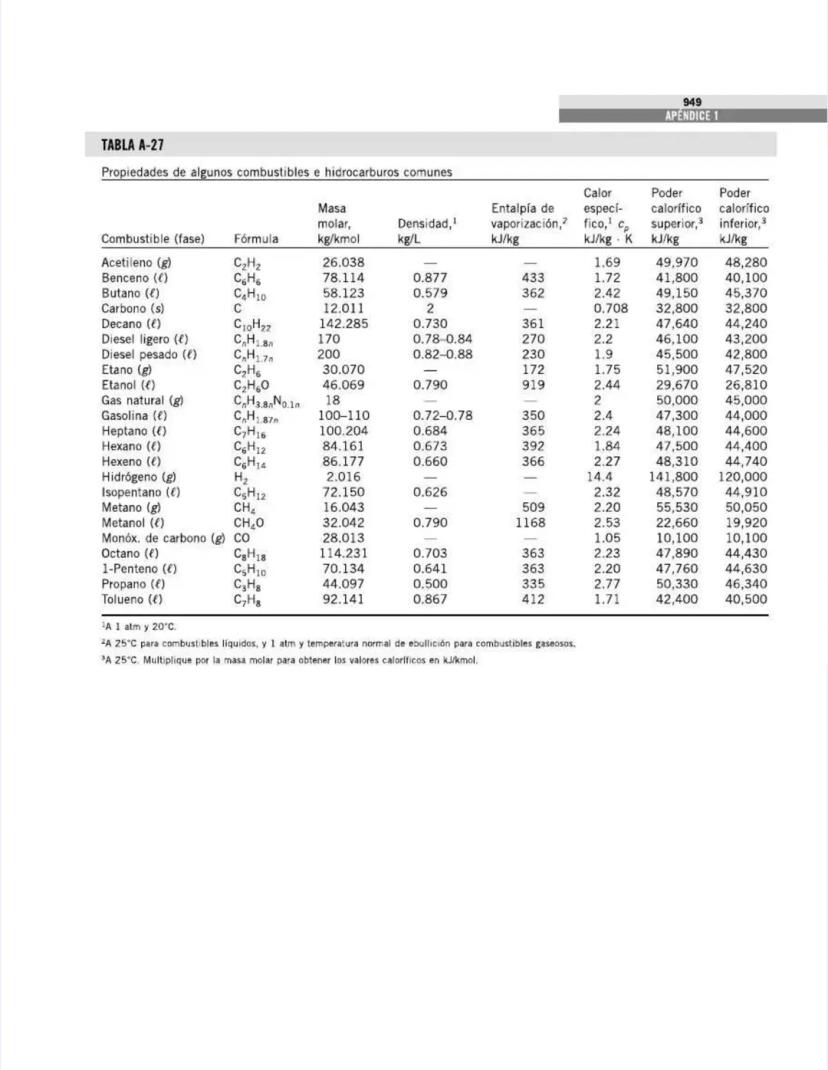
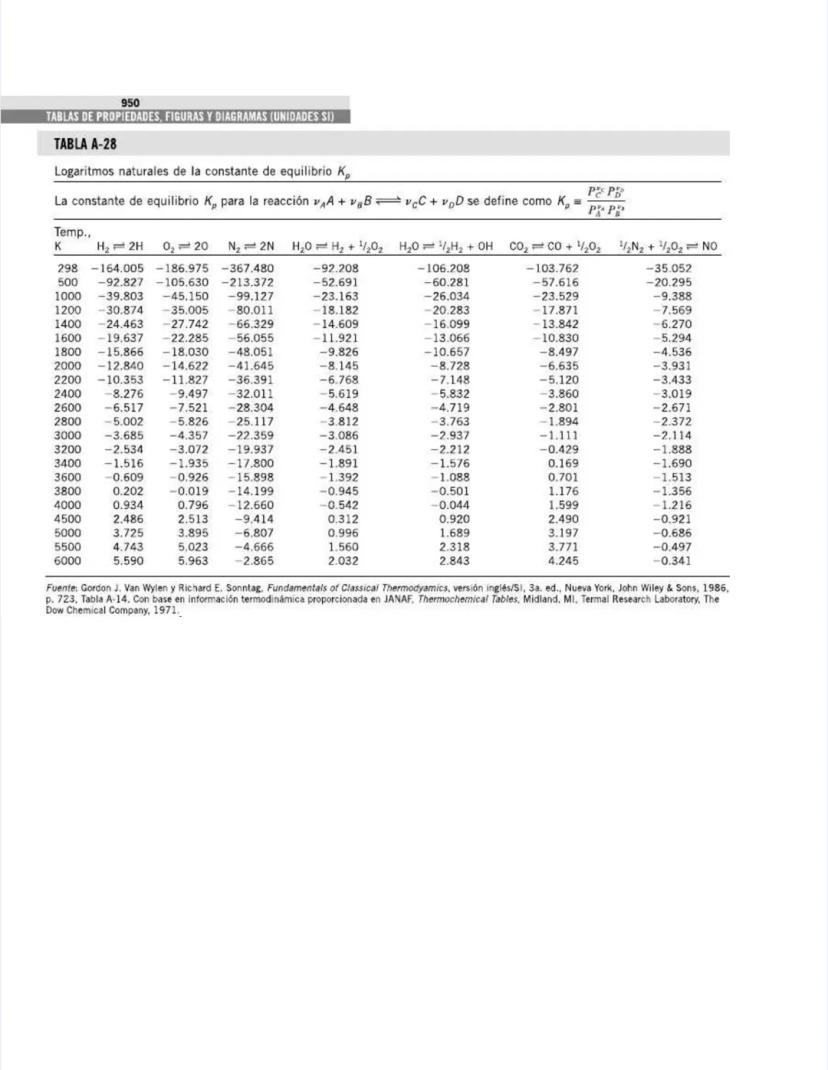
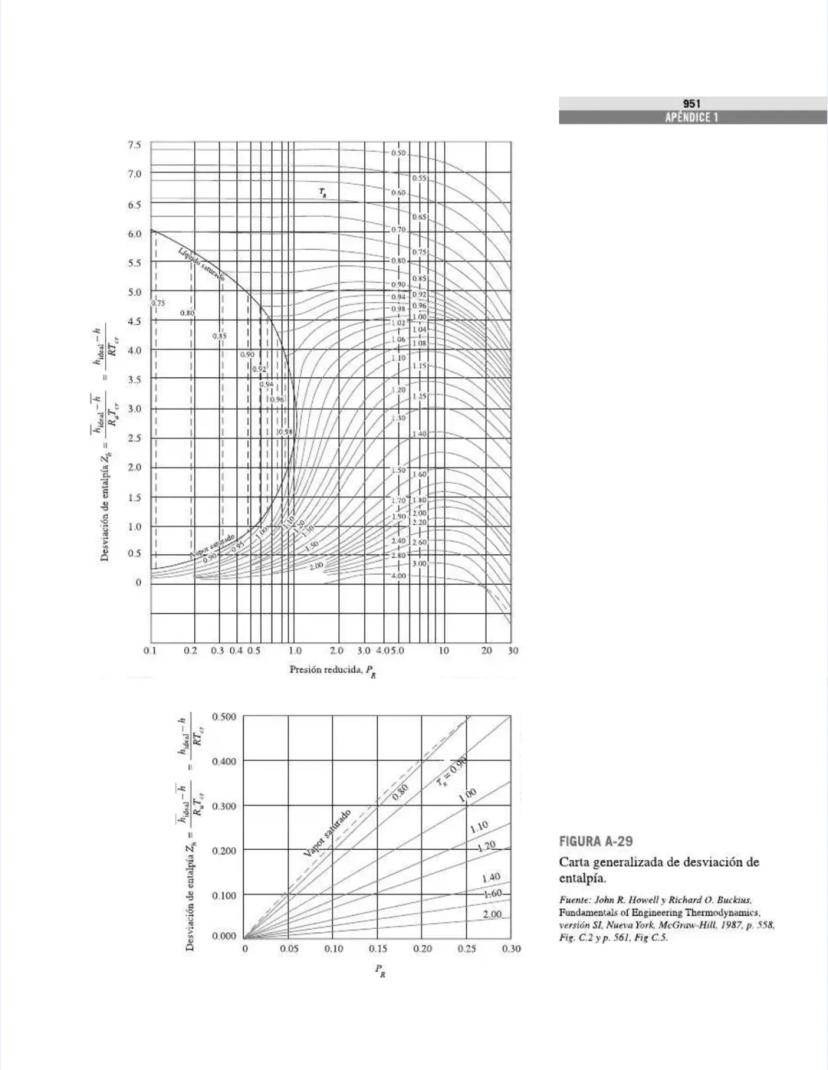
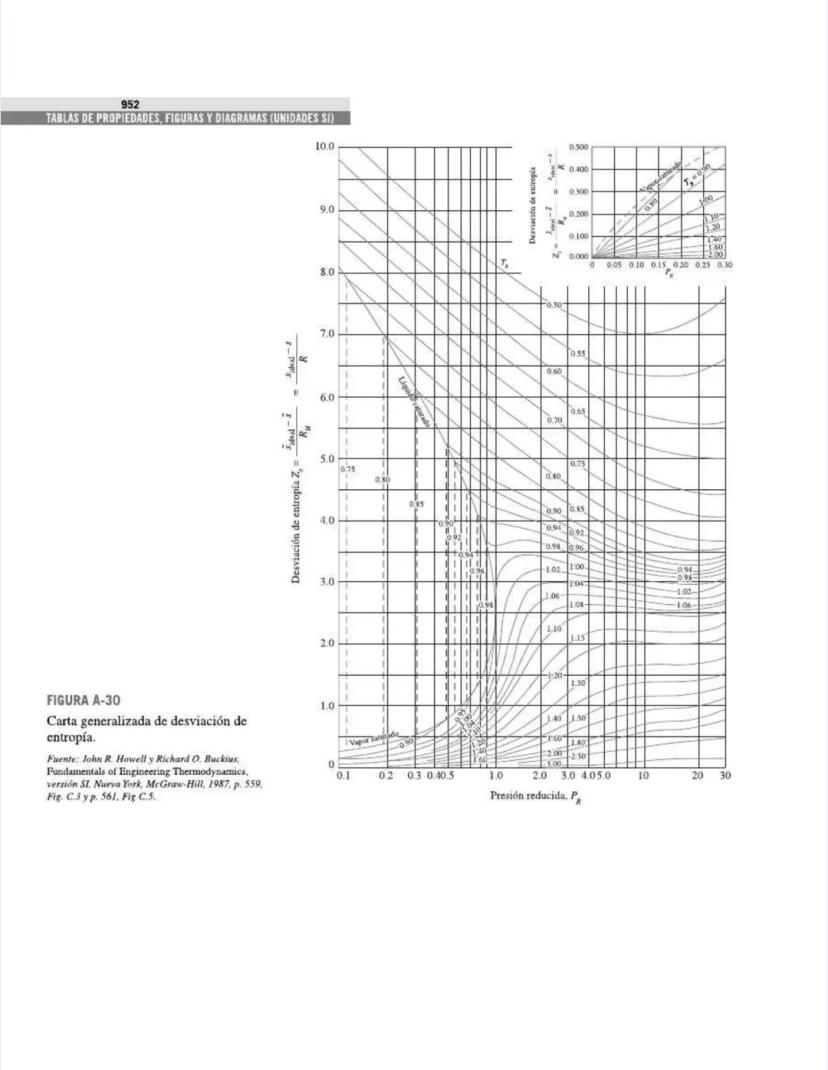
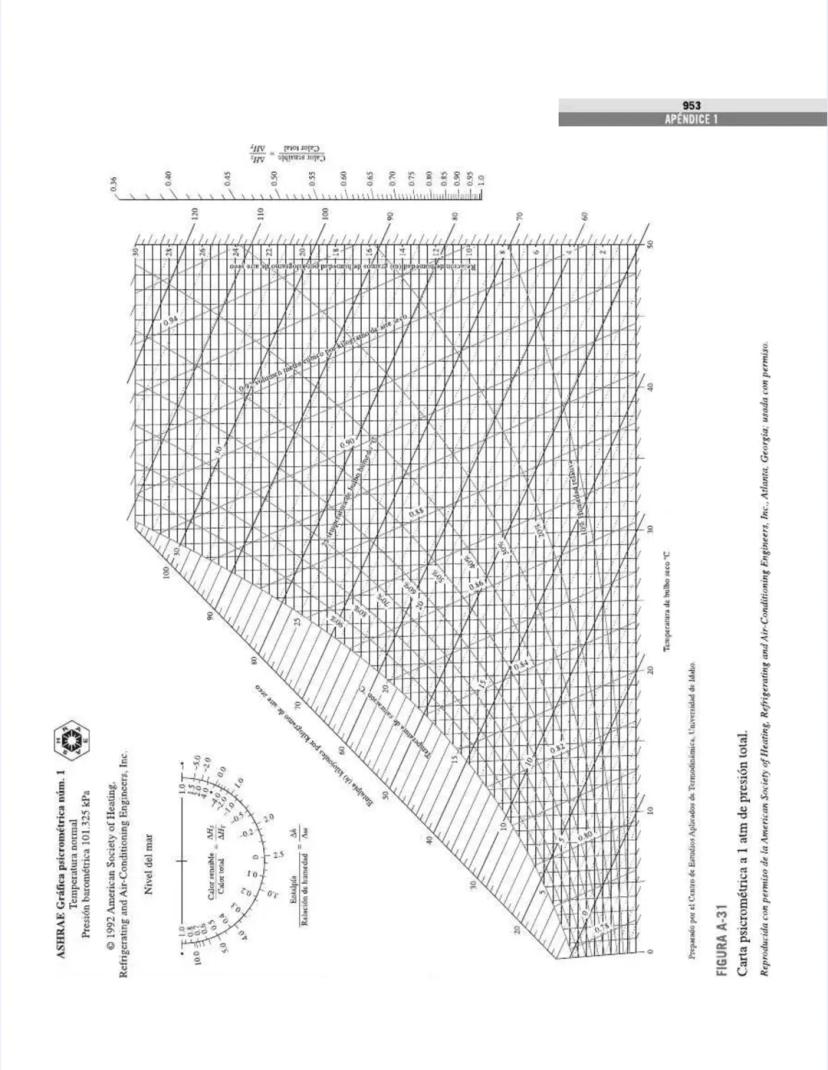
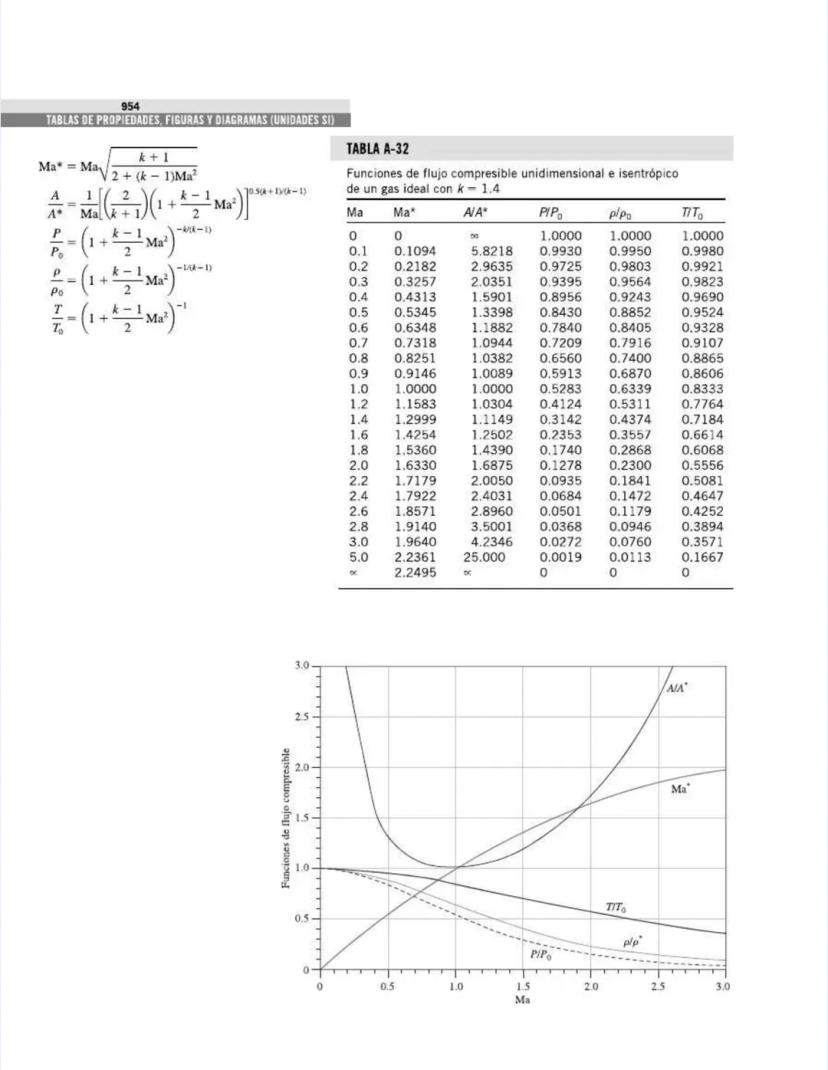
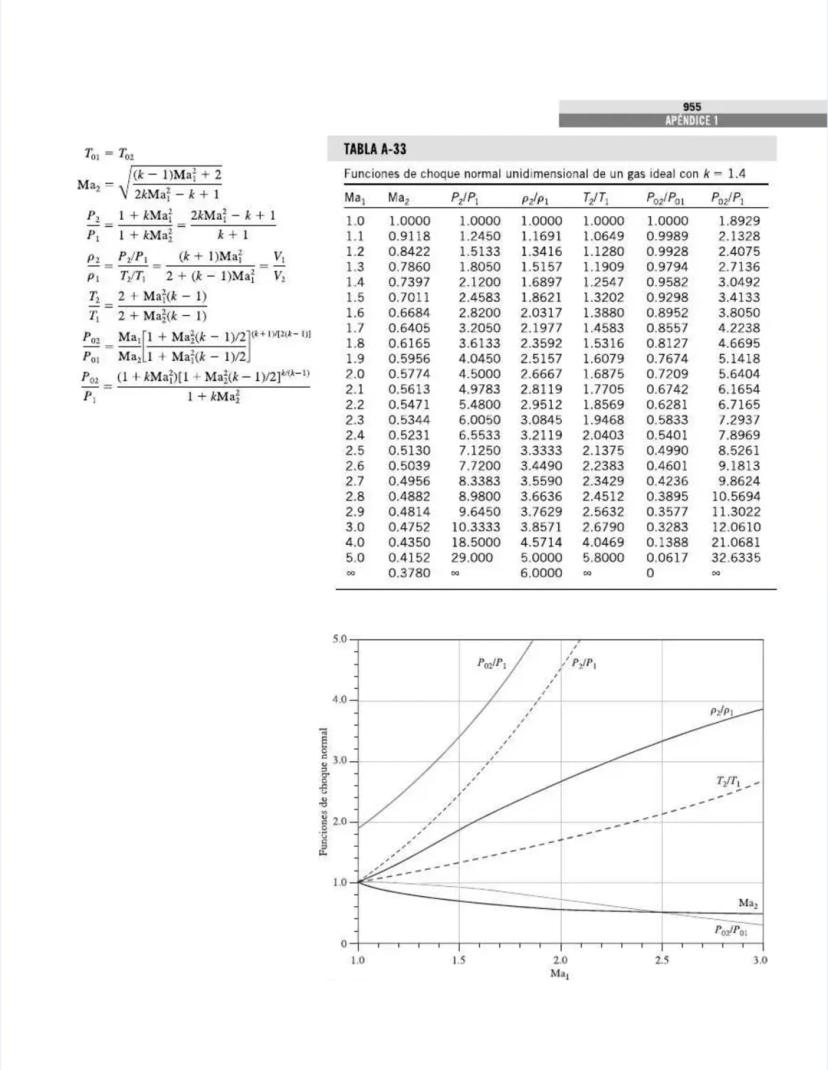
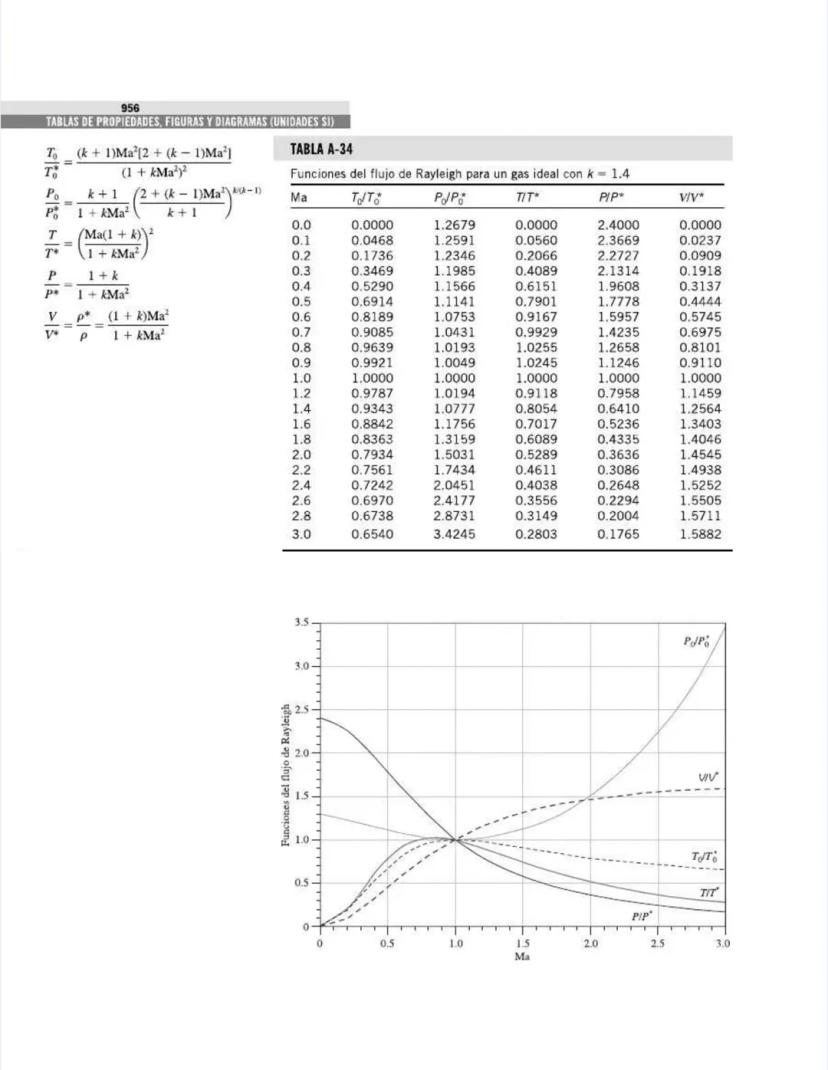

¡Tienes en tus manos un tesoro para ingenieros! Esta página nos presenta el contenido de las tablas y figuras que usarás constantemente en tus clases de termodinámica.
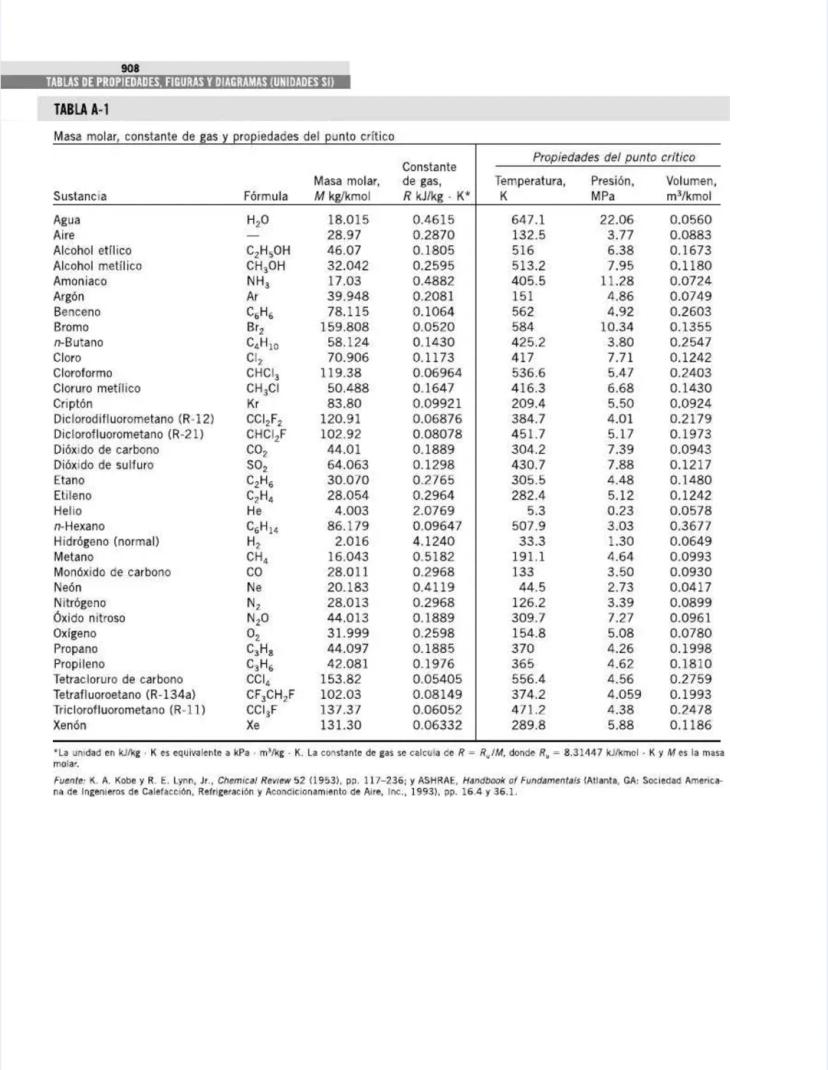
Las tablas están organizadas por tipo de sustancia y propiedades. En la Tabla A-1 encontrarás información fundamental como la masa molar y las constantes de gas para diversas sustancias, desde el agua hasta gases nobles como el helio. Estas propiedades son la base para muchos cálculos termodinámicos.
Las tablas incluyen datos de propiedades críticas (temperatura, presión y volumen) que son cruciales para entender el comportamiento de las sustancias cerca de sus puntos críticos, donde las fases líquida y gaseosa se vuelven indistinguibles.
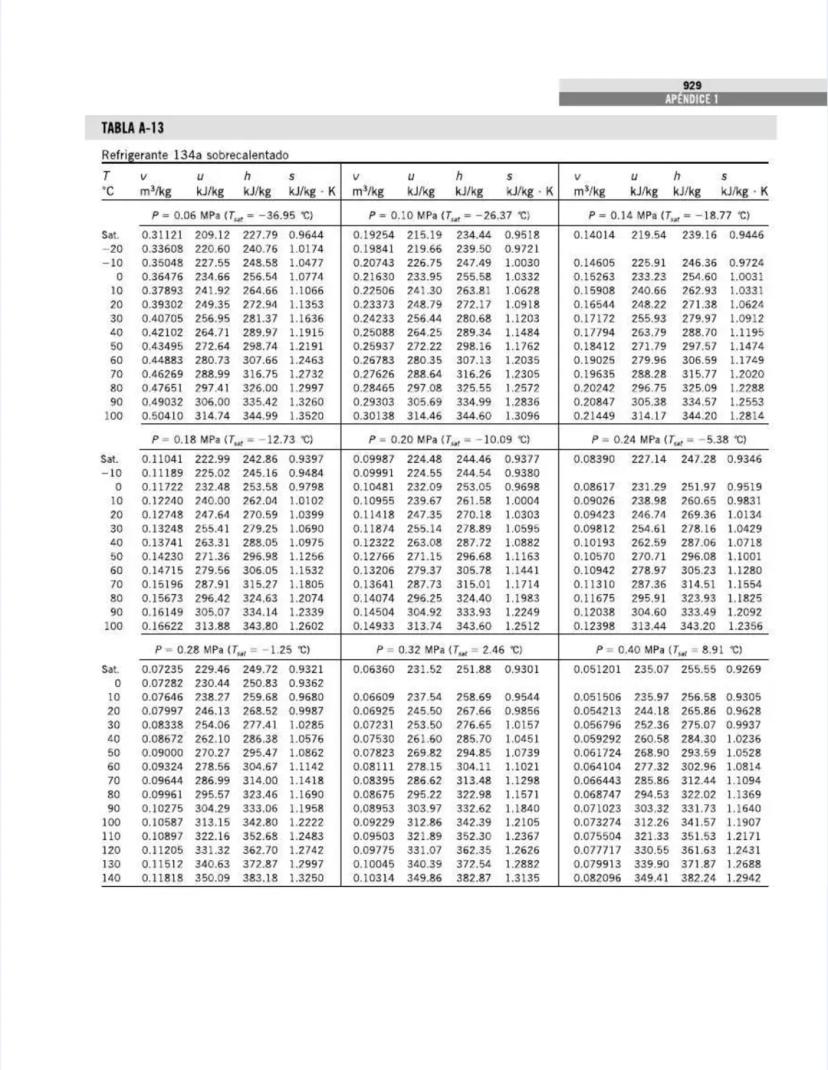
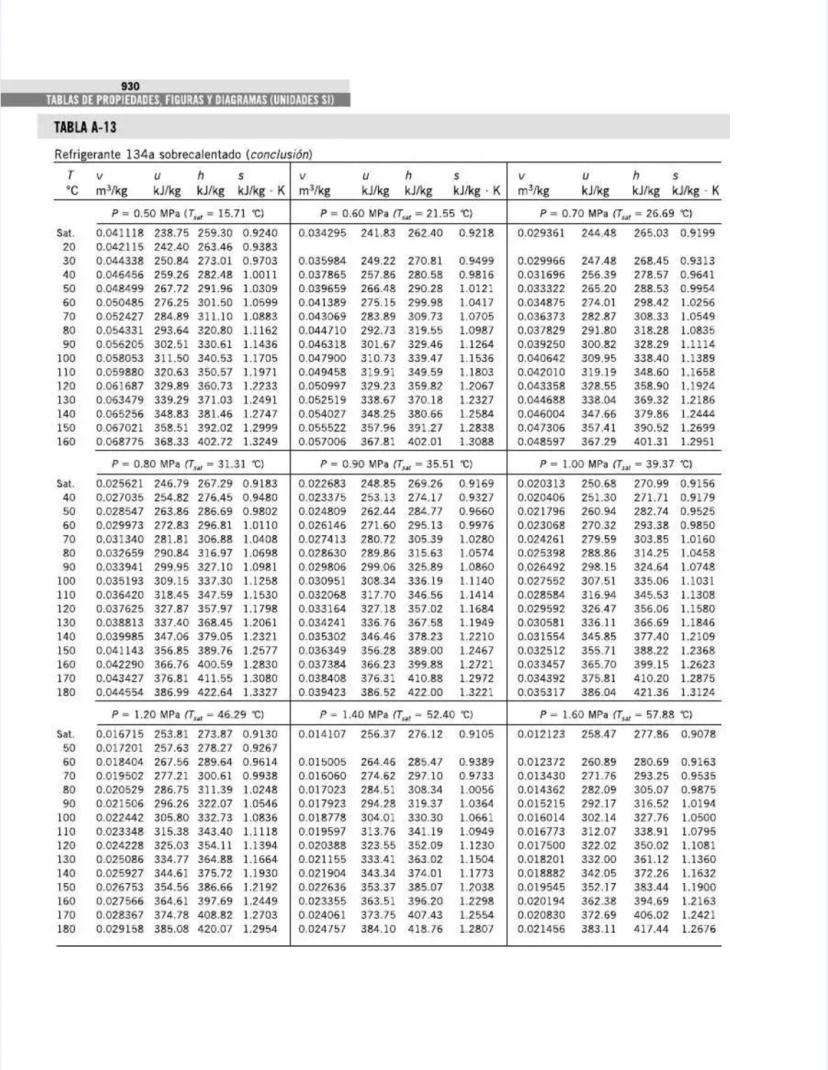
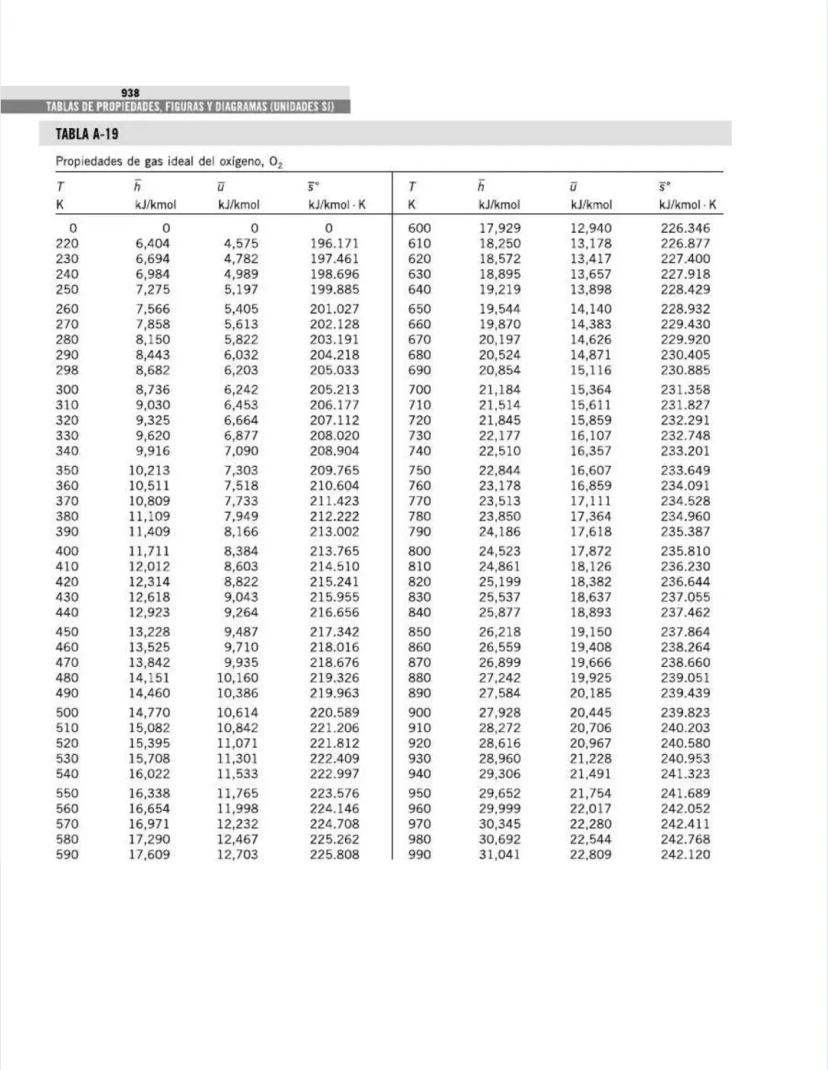
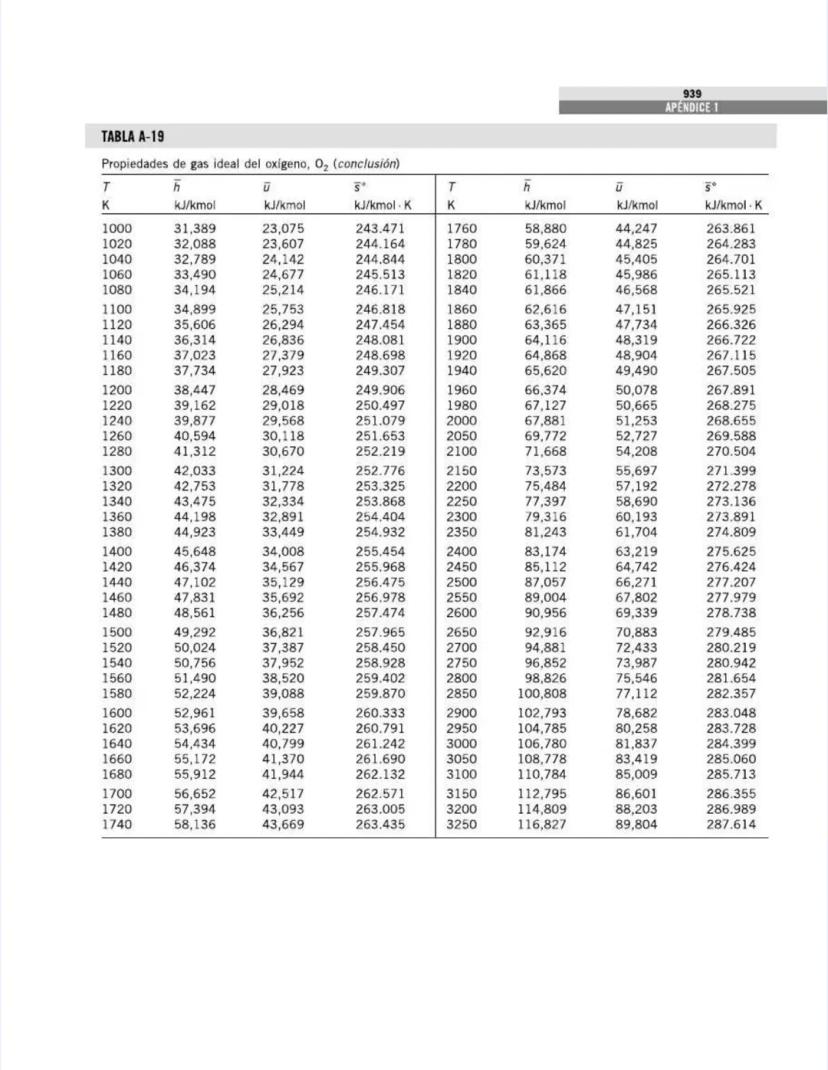
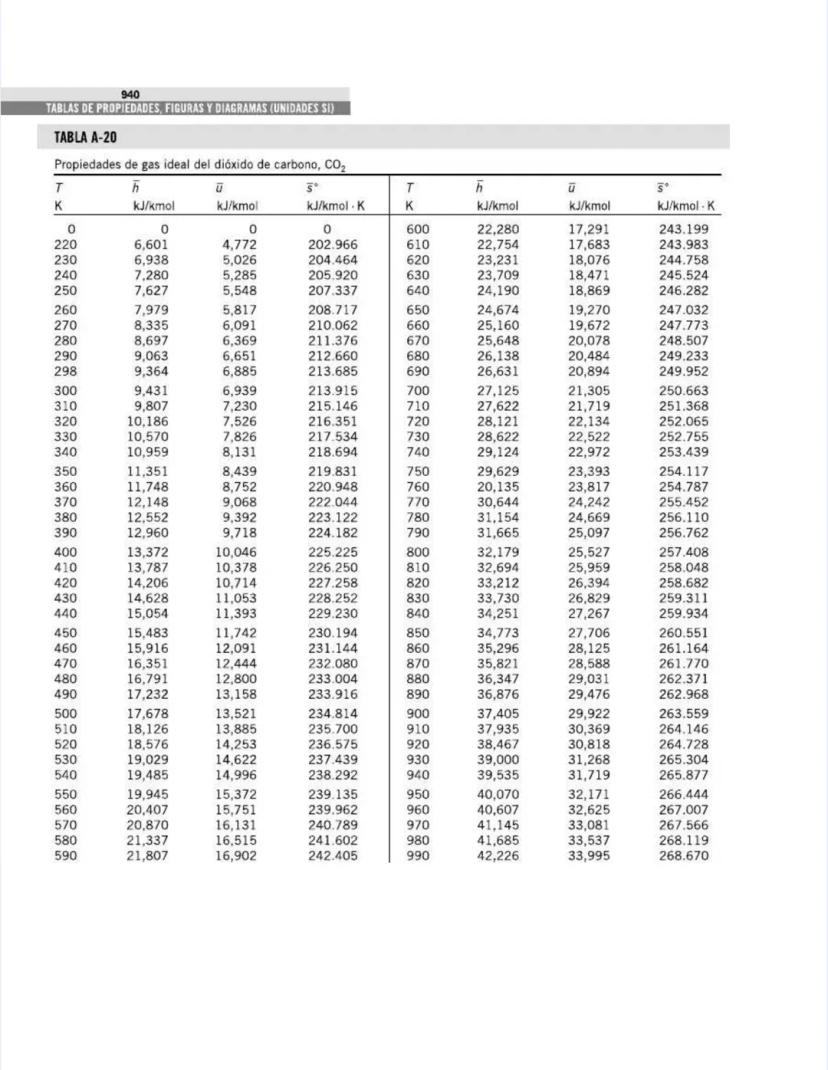
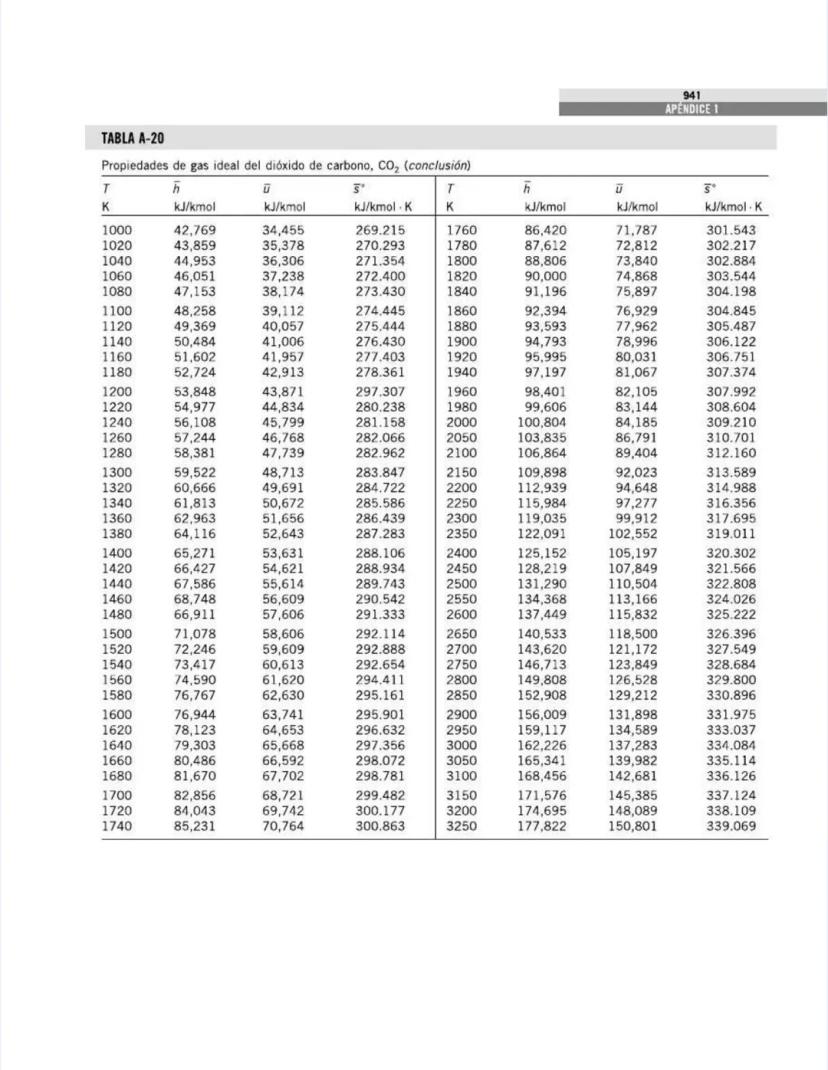
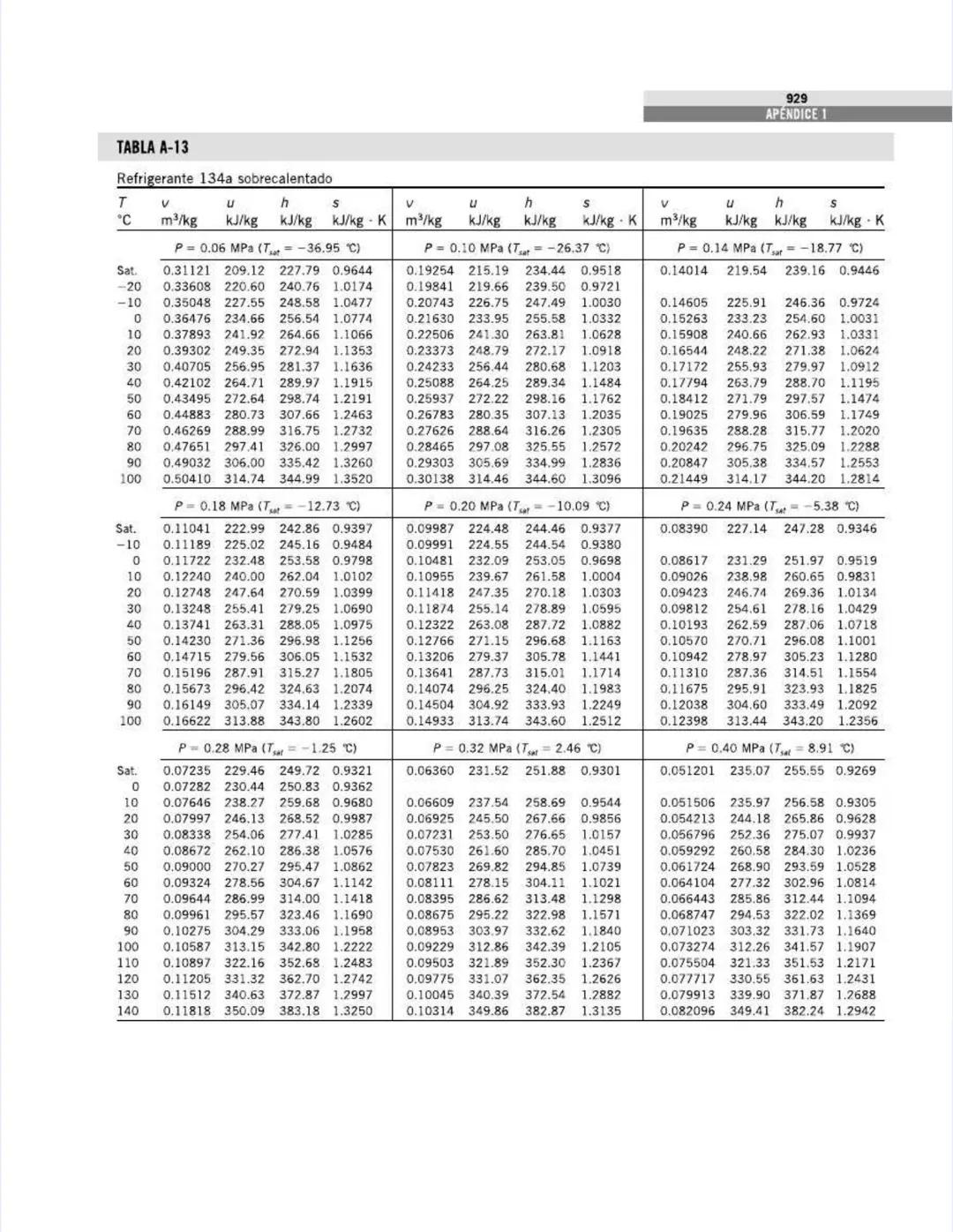
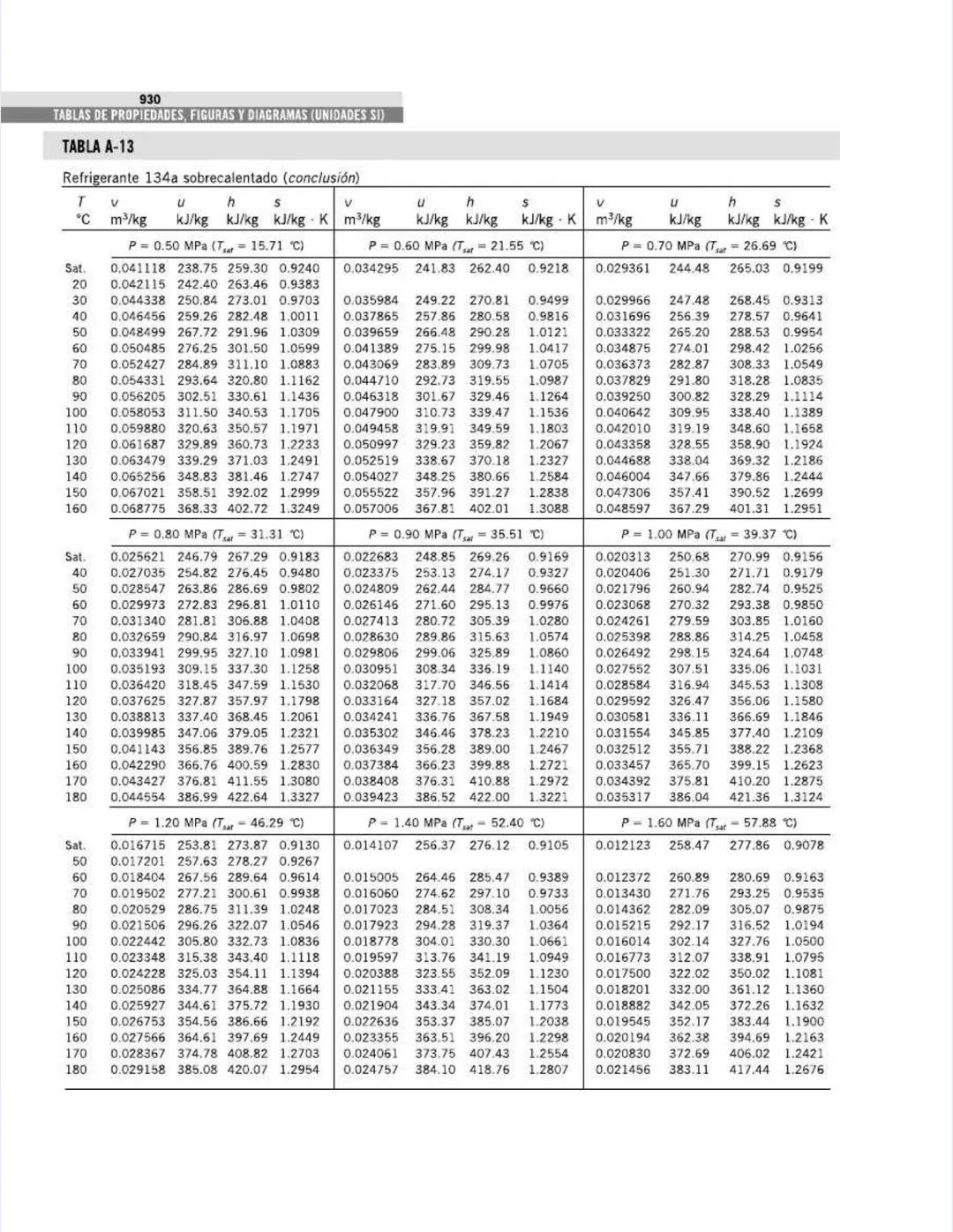
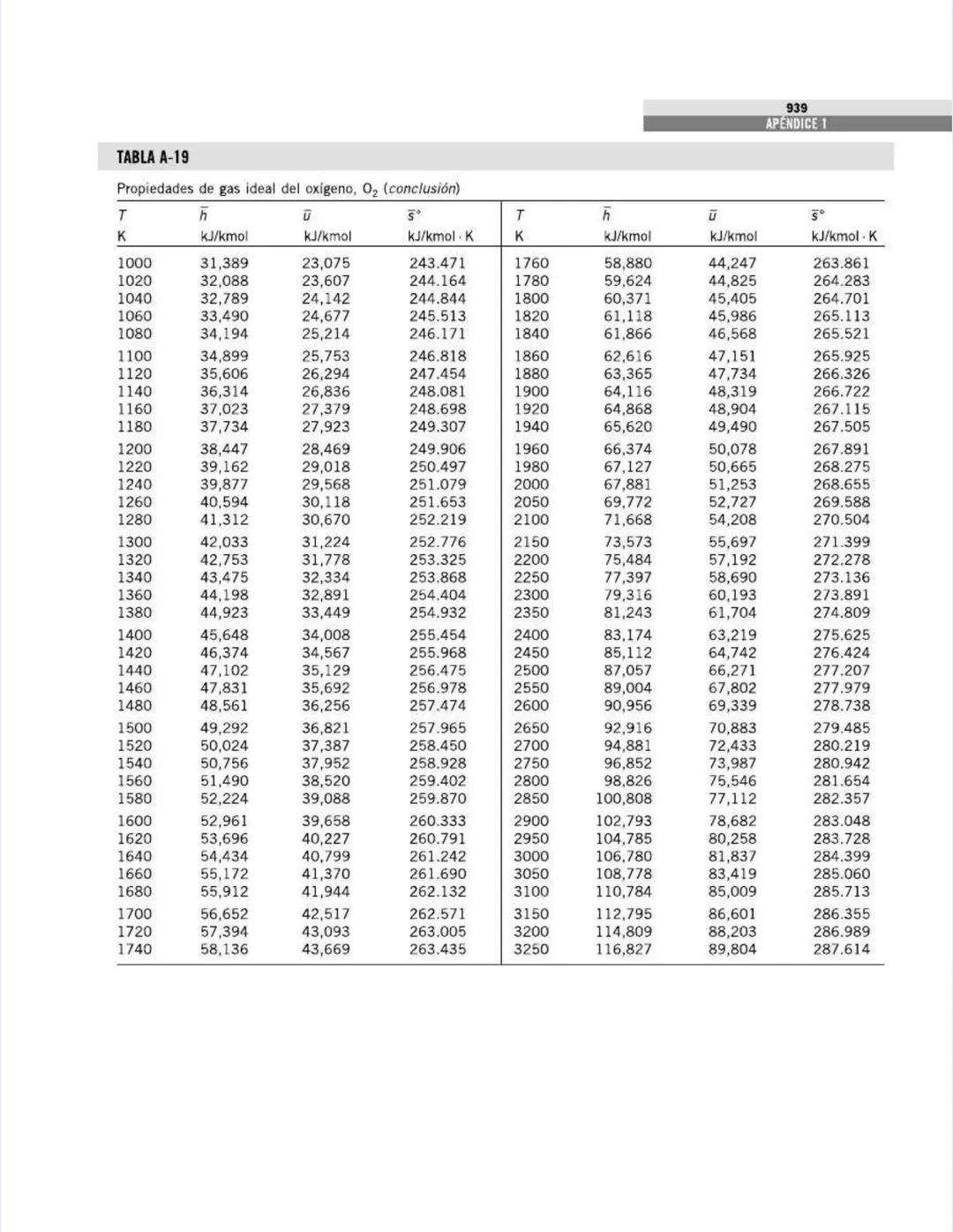
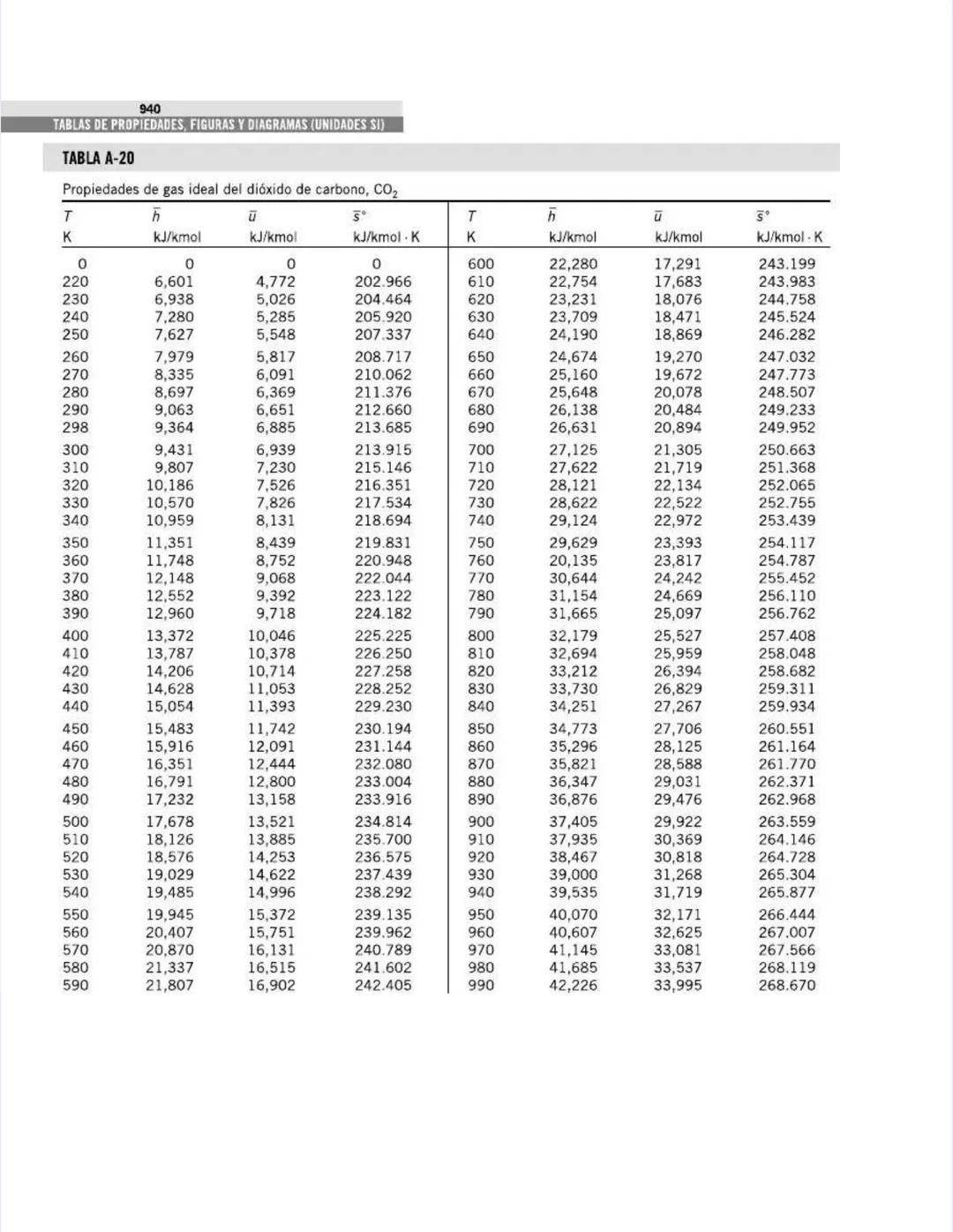
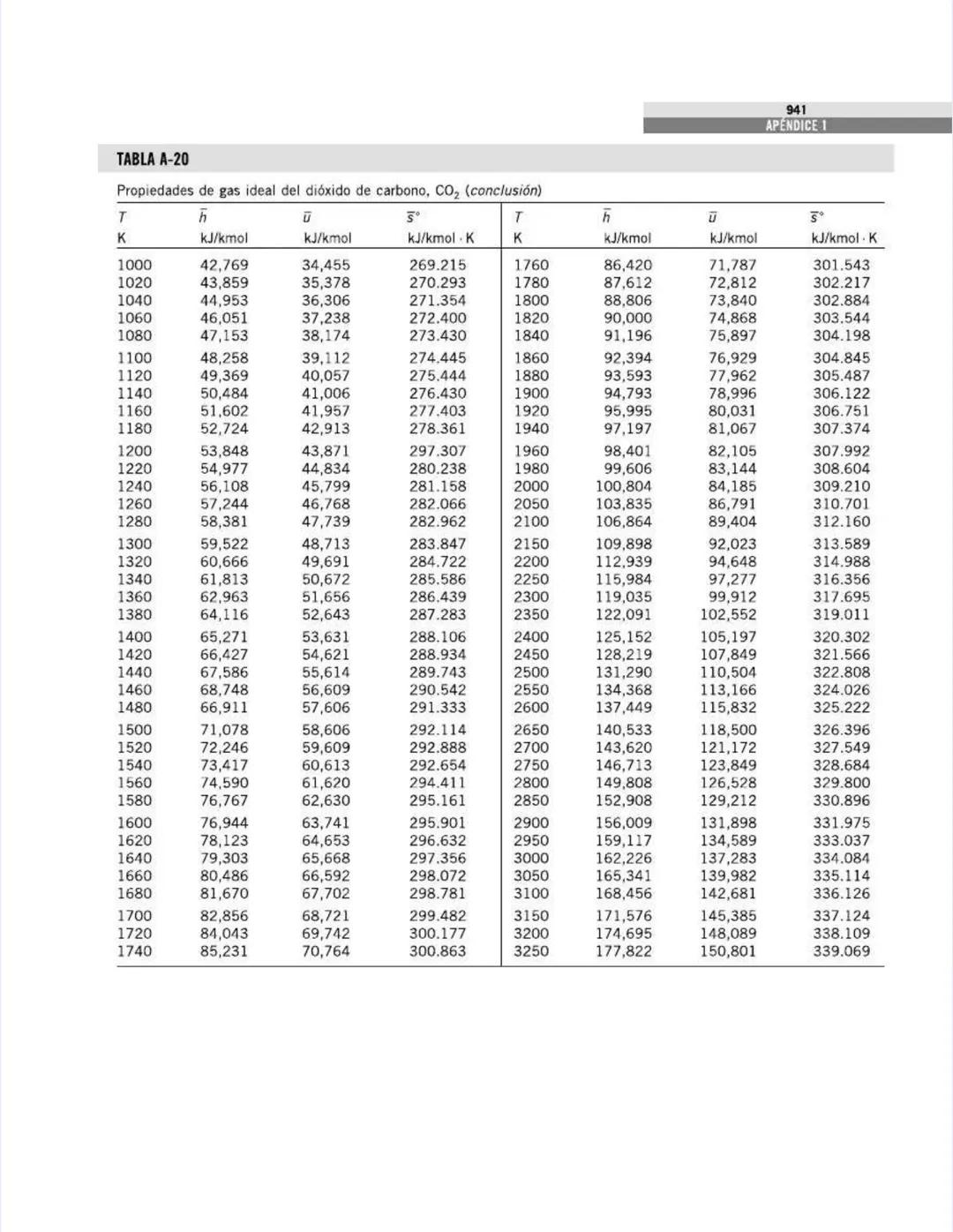
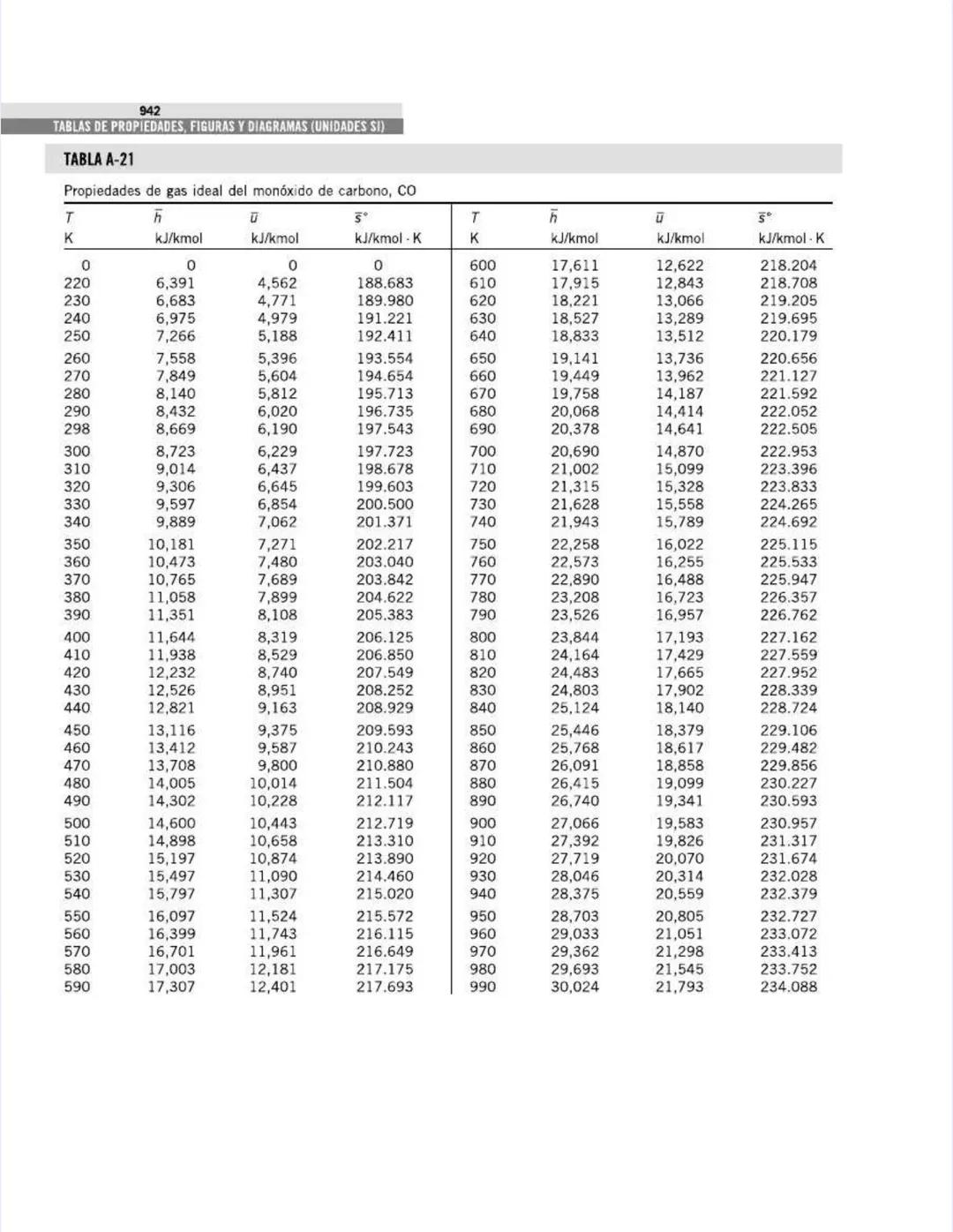
También encontrarás tablas específicas para sustancias comunes como agua, refrigerantes, y gases como nitrógeno, oxígeno y dióxido de carbono. Estas tablas te permitirán determinar propiedades como entalpía, entropía y energía interna a diferentes temperaturas y presiones.
💡 No memorices estos datos, pero familiarízate con la organización de las tablas. Saber dónde encontrar cada propiedad te ahorrará tiempo valioso durante exámenes y proyectos.
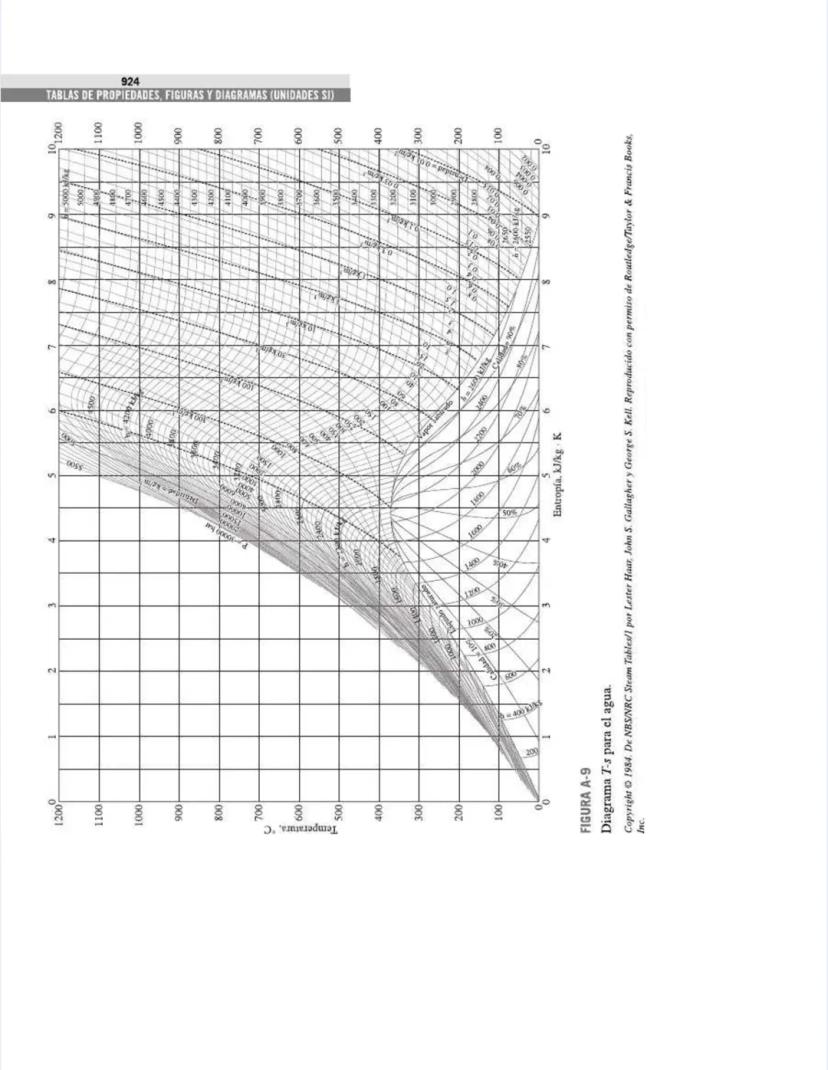
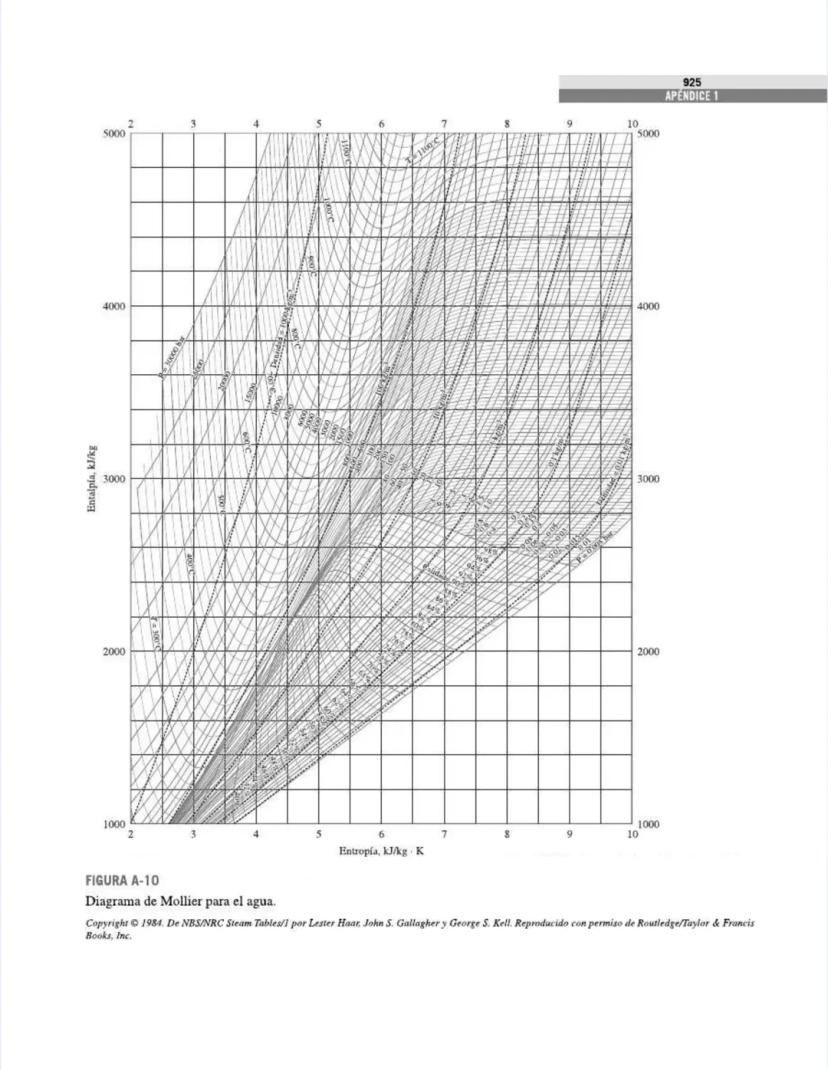
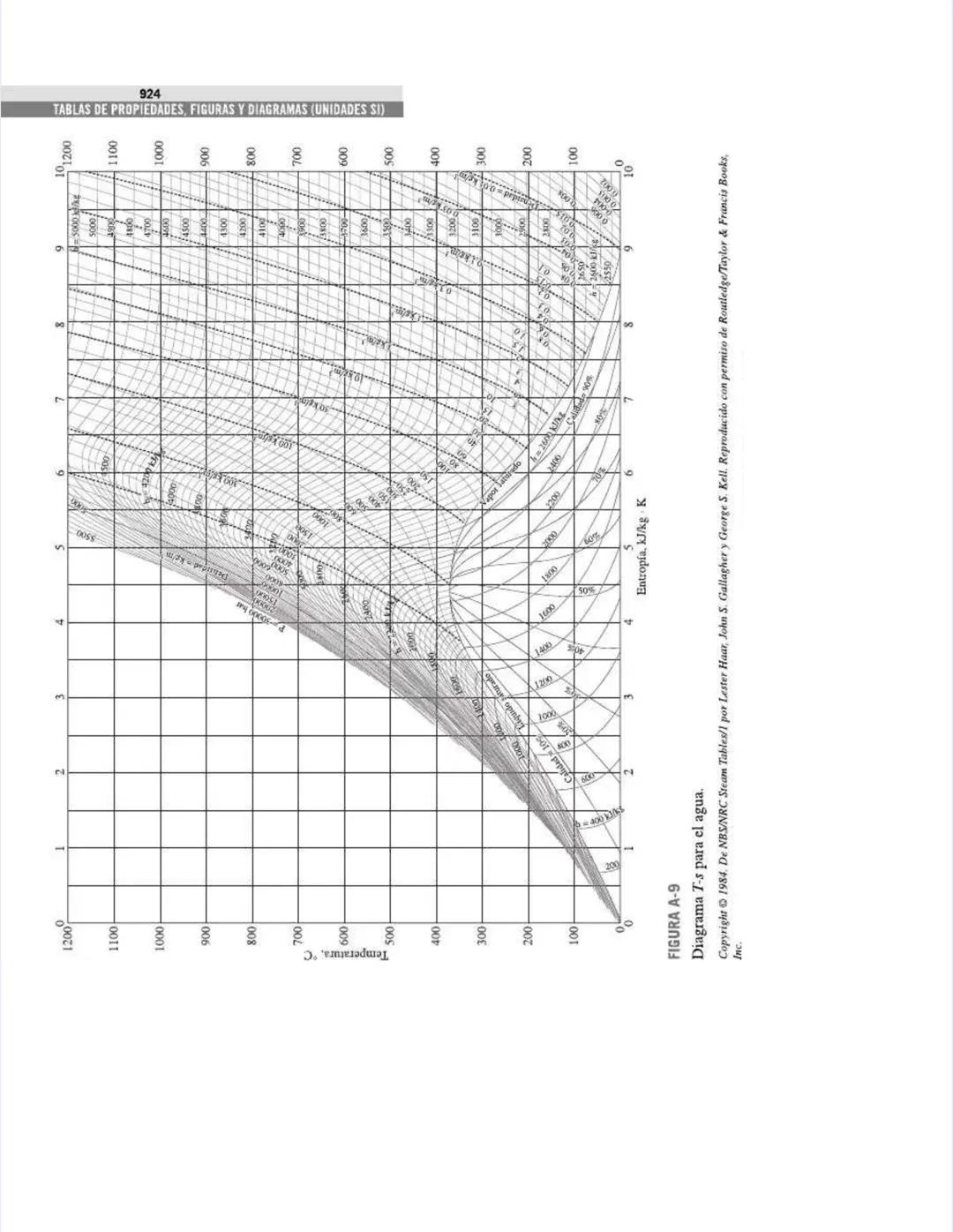
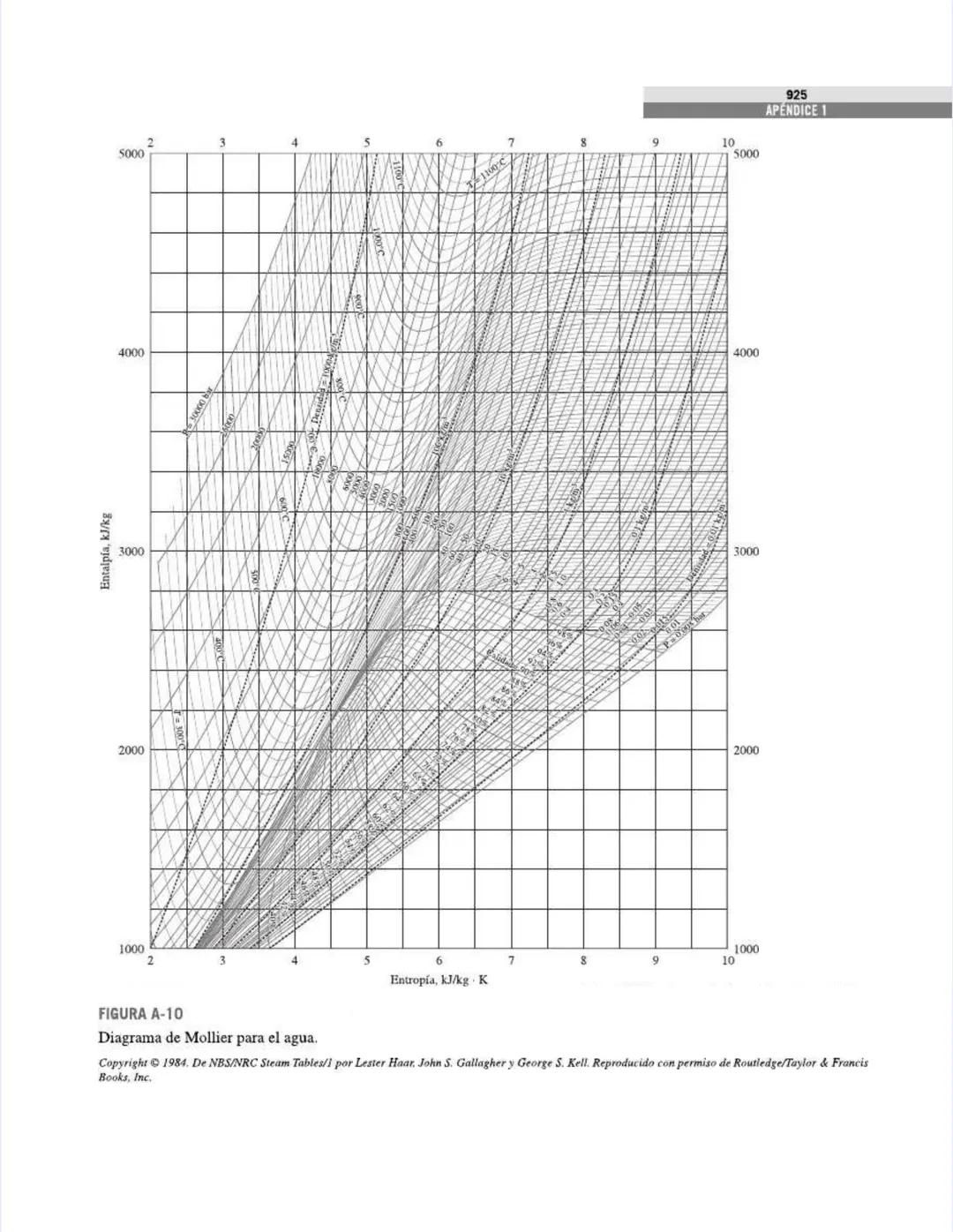
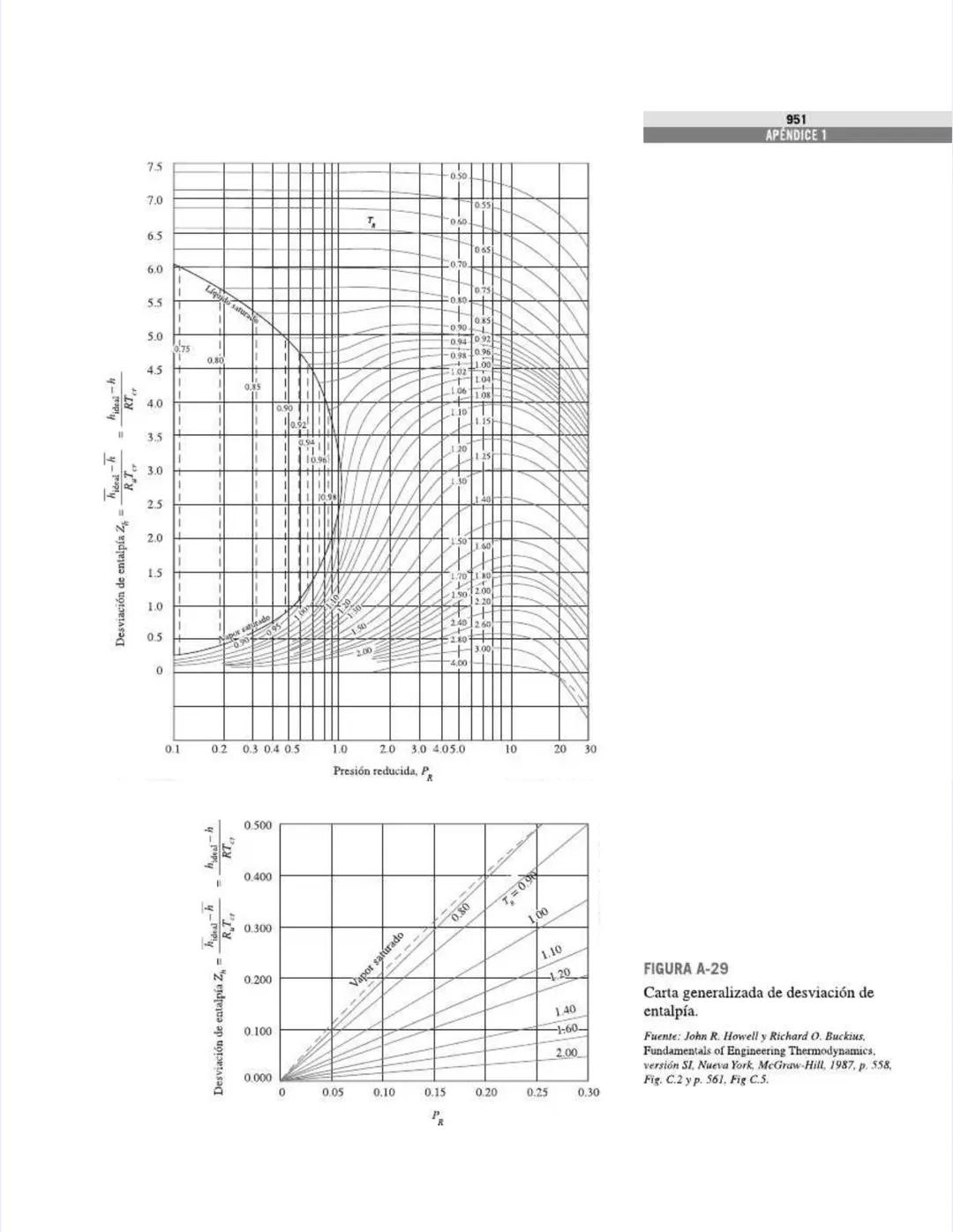
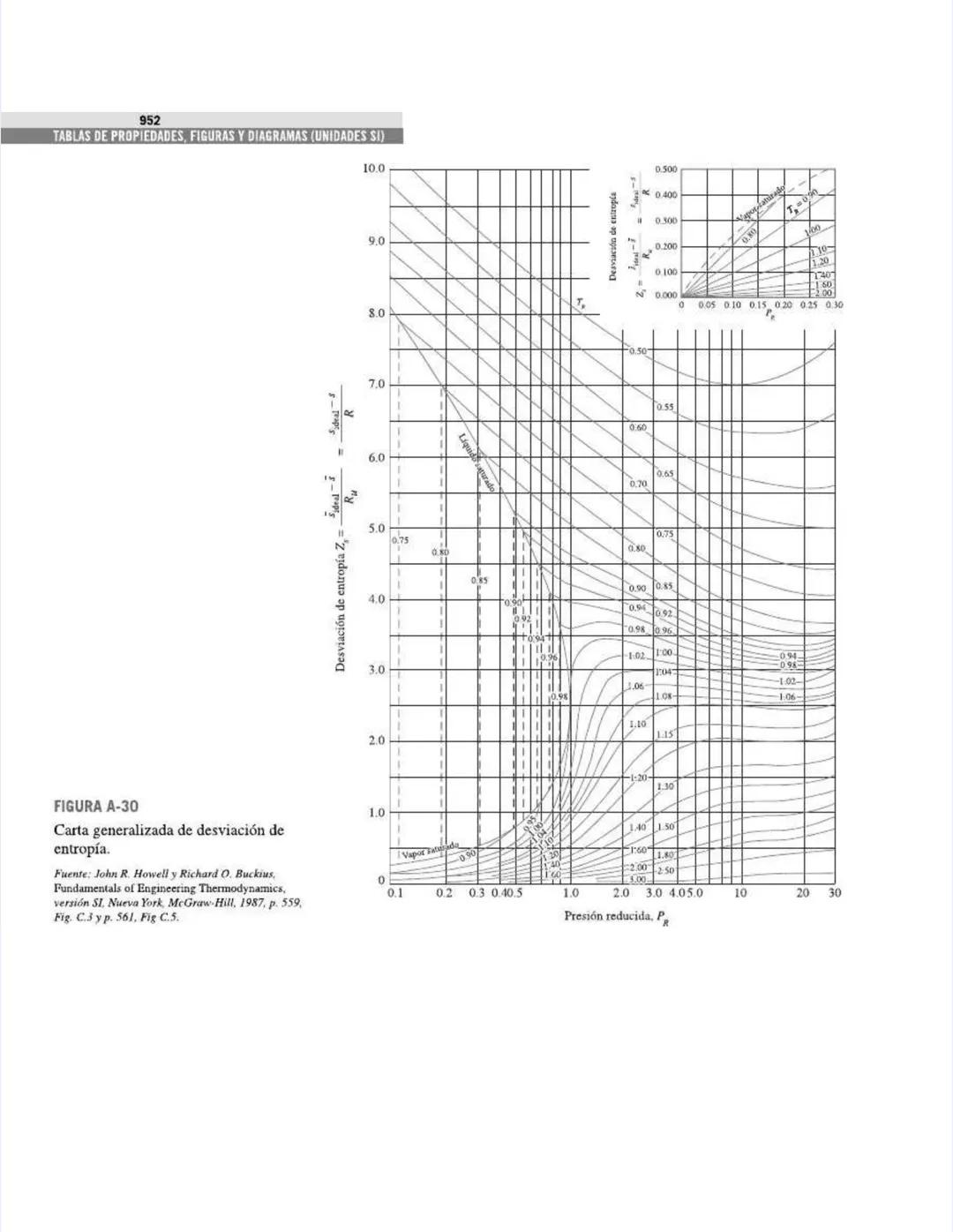
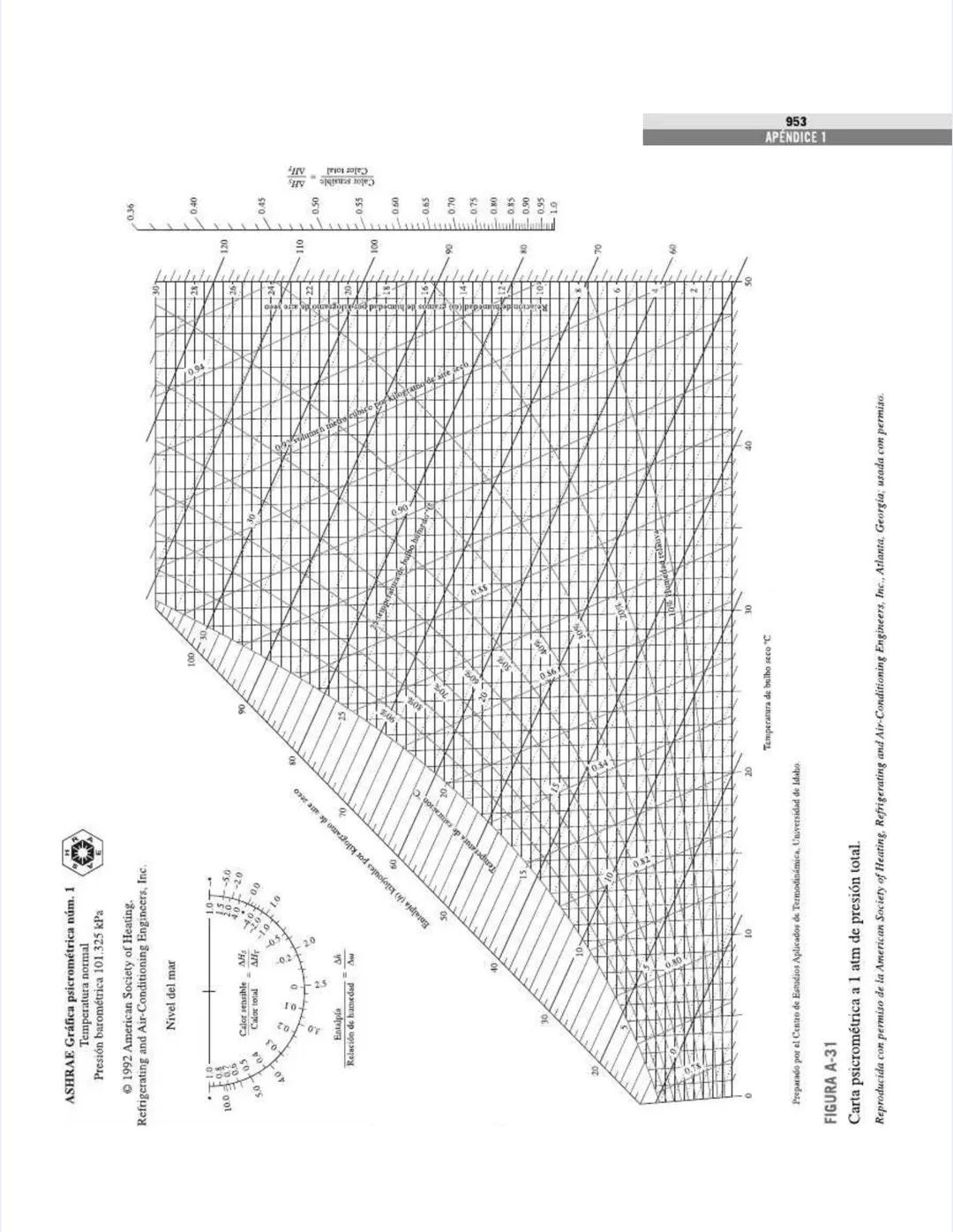
Las figuras y diagramas incluyen herramientas visuales importantes como el diagrama T-s y el diagrama de Mollier para el agua, que te ayudarán a analizar ciclos termodinámicos de manera eficiente.
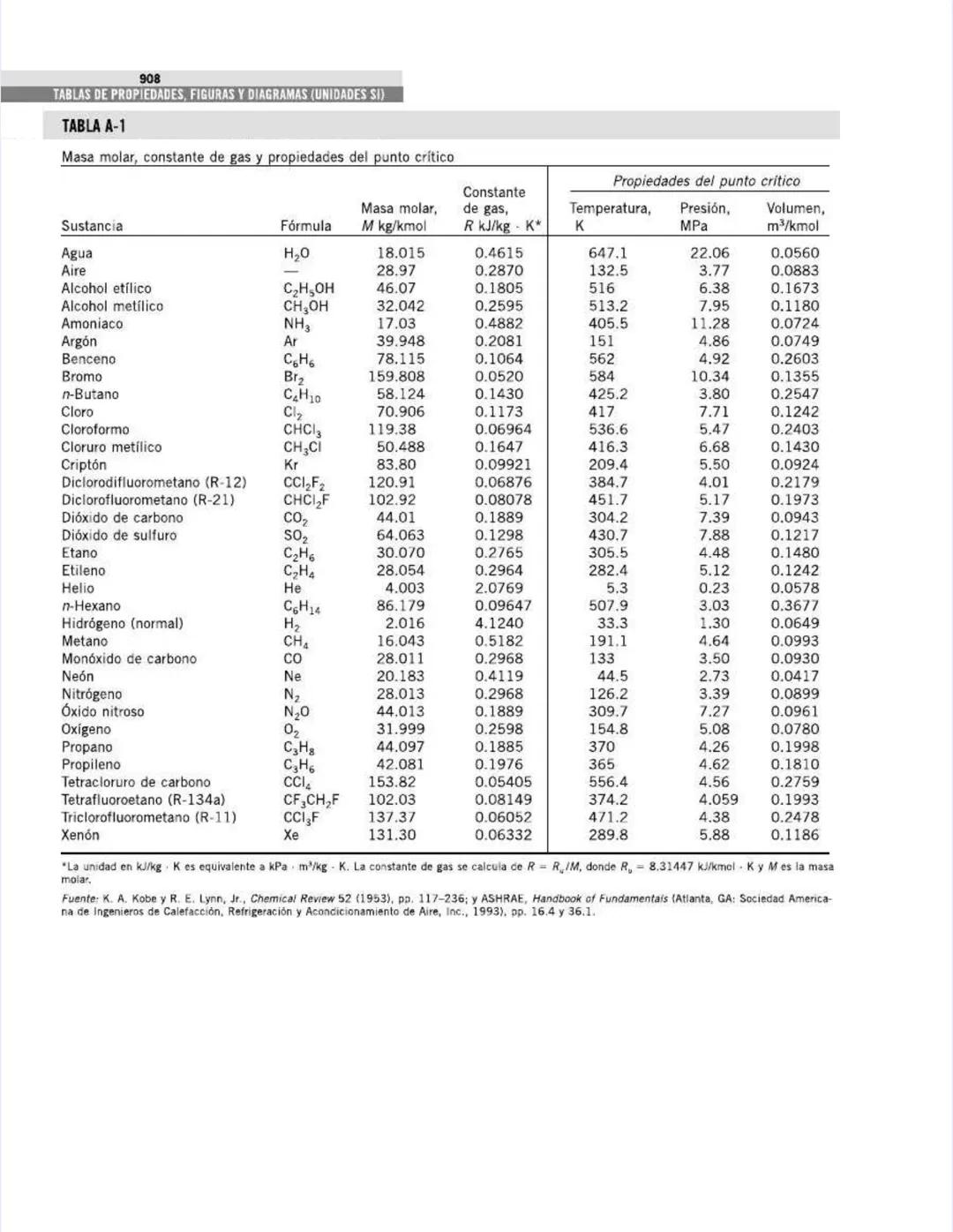
Esta tabla es una mina de oro para tus cálculos termodinámicos. Contiene la masa molar, la constante de gas y las propiedades del punto crítico para diversas sustancias.
La masa molar (M) se expresa en kg/kmol y es fundamental para convertir entre unidades molares y másicas. Por ejemplo, el agua (H₂O) tiene una masa molar de 18.015 kg/kmol, mientras que el aire tiene 28.97 kg/kmol.
La constante específica de gas (R) varía para cada sustancia y es crucial para la ecuación de estado de gases ideales . Para el agua es 0.4615 kJ/kg·K, mientras que para el hidrógeno es 4.1240 kJ/kg·K, ¡casi diez veces mayor!
Las propiedades críticas son valores límite donde el comportamiento de las sustancias cambia drásticamente:
Estas propiedades críticas son esenciales cuando trabajas con ciclos de refrigeración, procesos de extracción supercrítica o sistemas de generación de energía.
💡 La relación entre la constante universal de gases R₀ = 8.31447 kJ/kmol·K y la constante específica R para cualquier sustancia es: R = R₀/M, donde M es la masa molar de la sustancia.
Esta tabla será tu referencia para numerosos problemas que involucren ecuaciones de estado y cálculos de propiedades de gases.
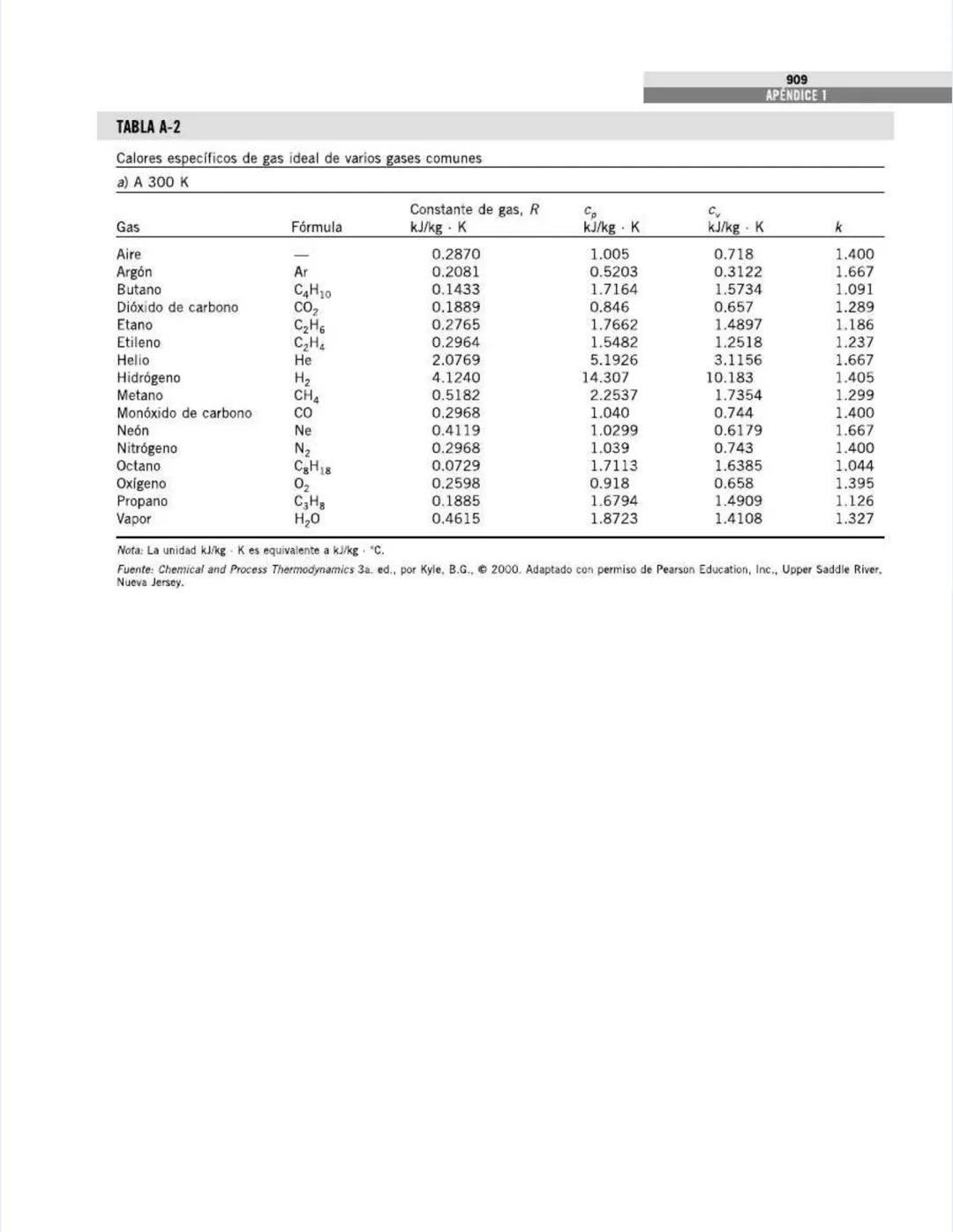
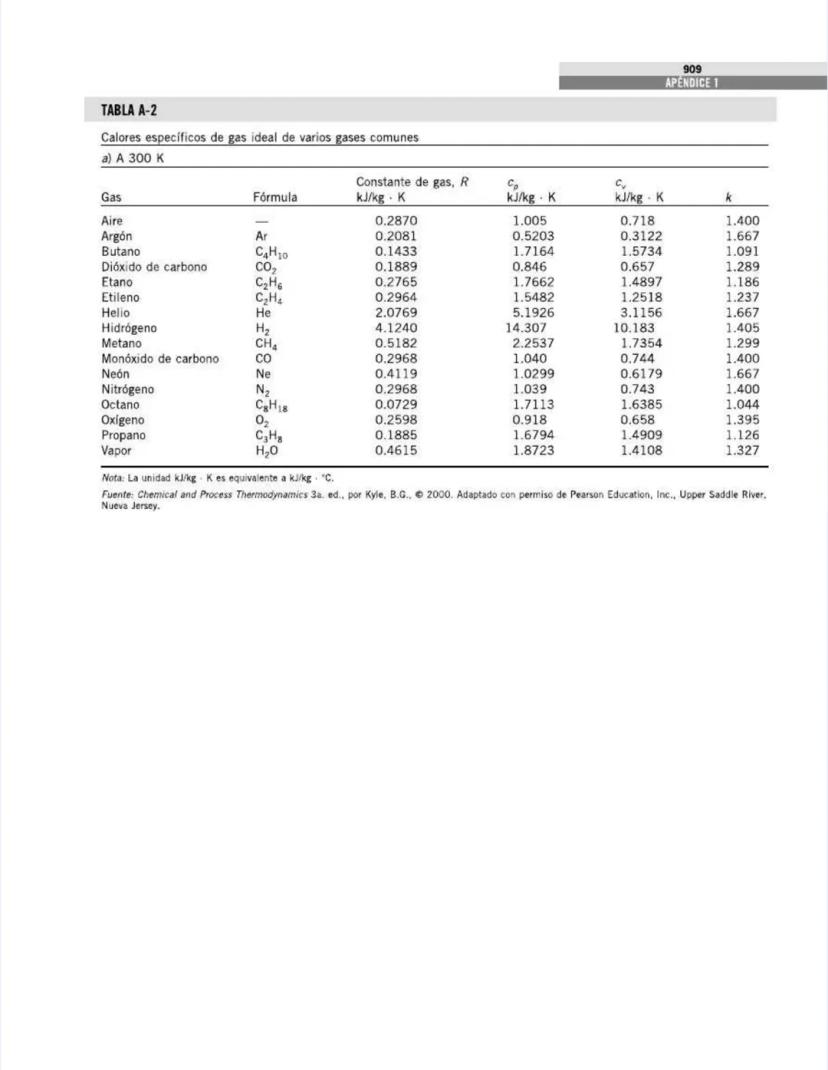
Esta tabla es fundamental para tus cálculos de energía térmica. Los calores específicos representan la cantidad de energía necesaria para cambiar la temperatura de una sustancia y son propiedades esenciales en termodinámica.
A 300 K (temperatura ambiente), observa las diferencias significativas entre gases:
La relación entre calores específicos es crucial para calcular procesos isentrópicos:
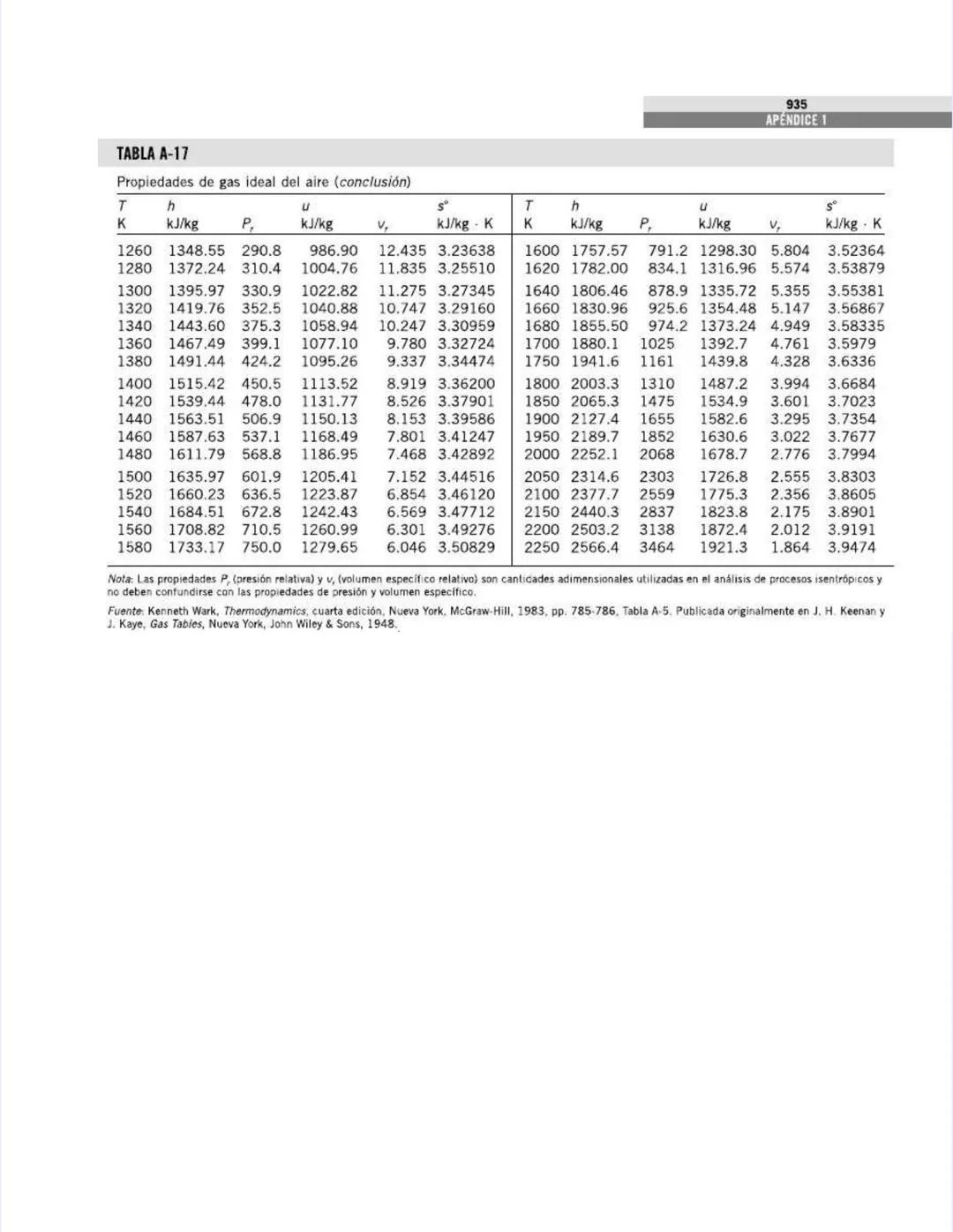
La tabla también muestra cómo los calores específicos aumentan con la temperatura. Por ejemplo, para el aire:
En la tercera parte de la tabla, encontrarás ecuaciones polinómicas para calcular Cp a diferentes temperaturas, expresadas como: cp = a + bT + cT² + dT³. Estas ecuaciones son extremadamente útiles para análisis de combustión y cálculos de ciclos de potencia a altas temperaturas.
💡 Recuerda siempre que la diferencia entre Cp y Cv para un gas ideal es simplemente la constante del gas: Cp - Cv = R
Utiliza estos valores cuando calcules trabajo, calor, cambios de entropía y eficiencias en ciclos termodinámicos.
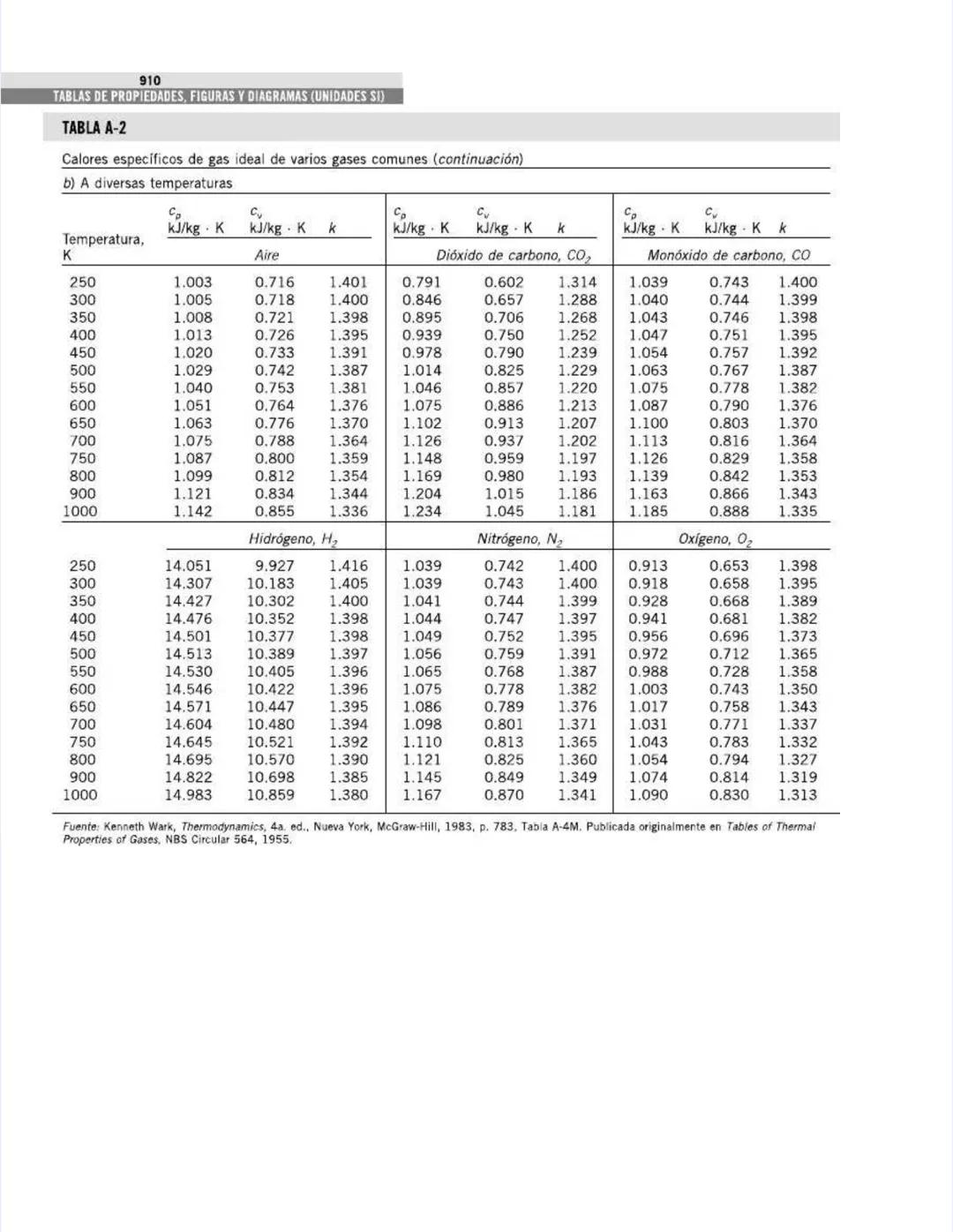
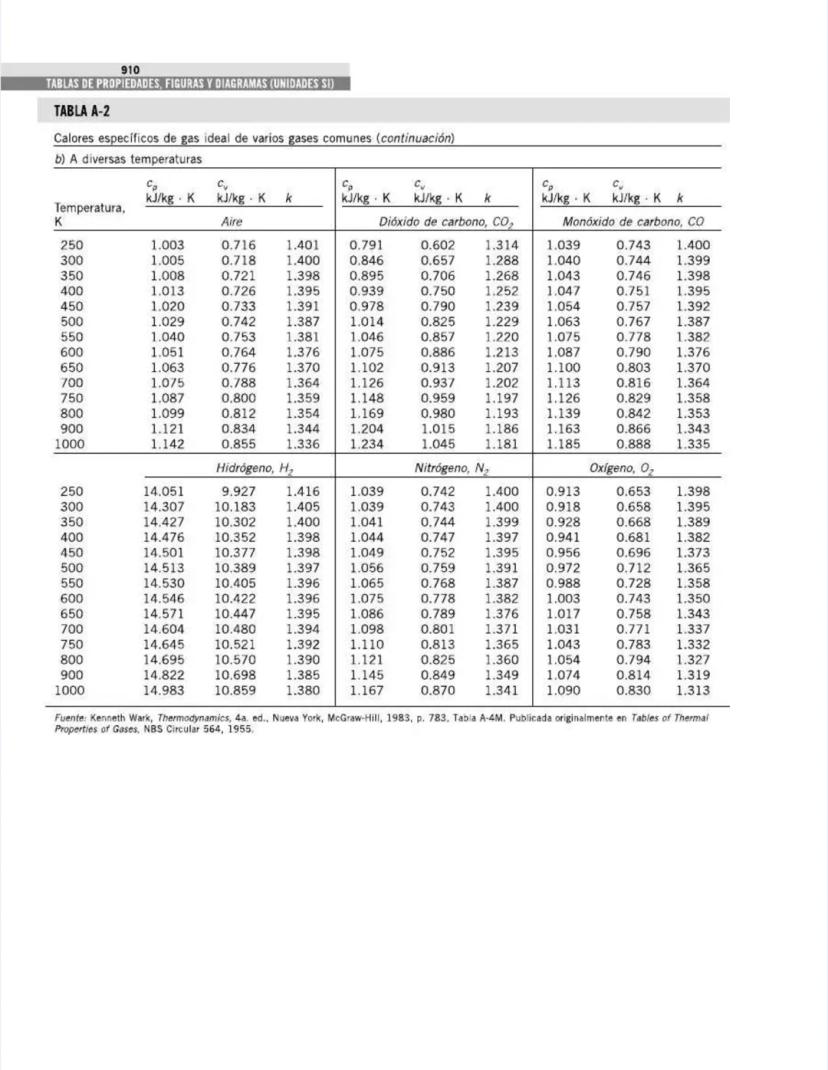
Esta tabla amplía la información anterior, mostrando cómo varían los calores específicos con la temperatura para gases comunes.
Para el aire, observa cómo Cp aumenta gradualmente:
Esta variación es crucial para cálculos precisos en sistemas que operan con grandes diferencias de temperatura, como turbinas de gas o motores de combustión interna.
El dióxido de carbono (CO₂) muestra una variación aún más significativa con la temperatura, lo que explica su comportamiento único en procesos térmicos:
También notarás que la relación k disminuye con la temperatura para la mayoría de los gases. Para el aire:
Estos cambios pueden parecer pequeños, pero tienen un impacto significativo en el cálculo de:
💡 Cuando realices análisis de ciclos termodinámicos que operen en amplios rangos de temperatura (como ciclos Brayton), considera usar valores de calor específico adecuados para cada nivel de temperatura o utiliza valores promedio para mayor precisión.
Usar valores incorrectos de calores específicos puede llevar a errores significativos en tus cálculos de eficiencia y rendimiento energético.
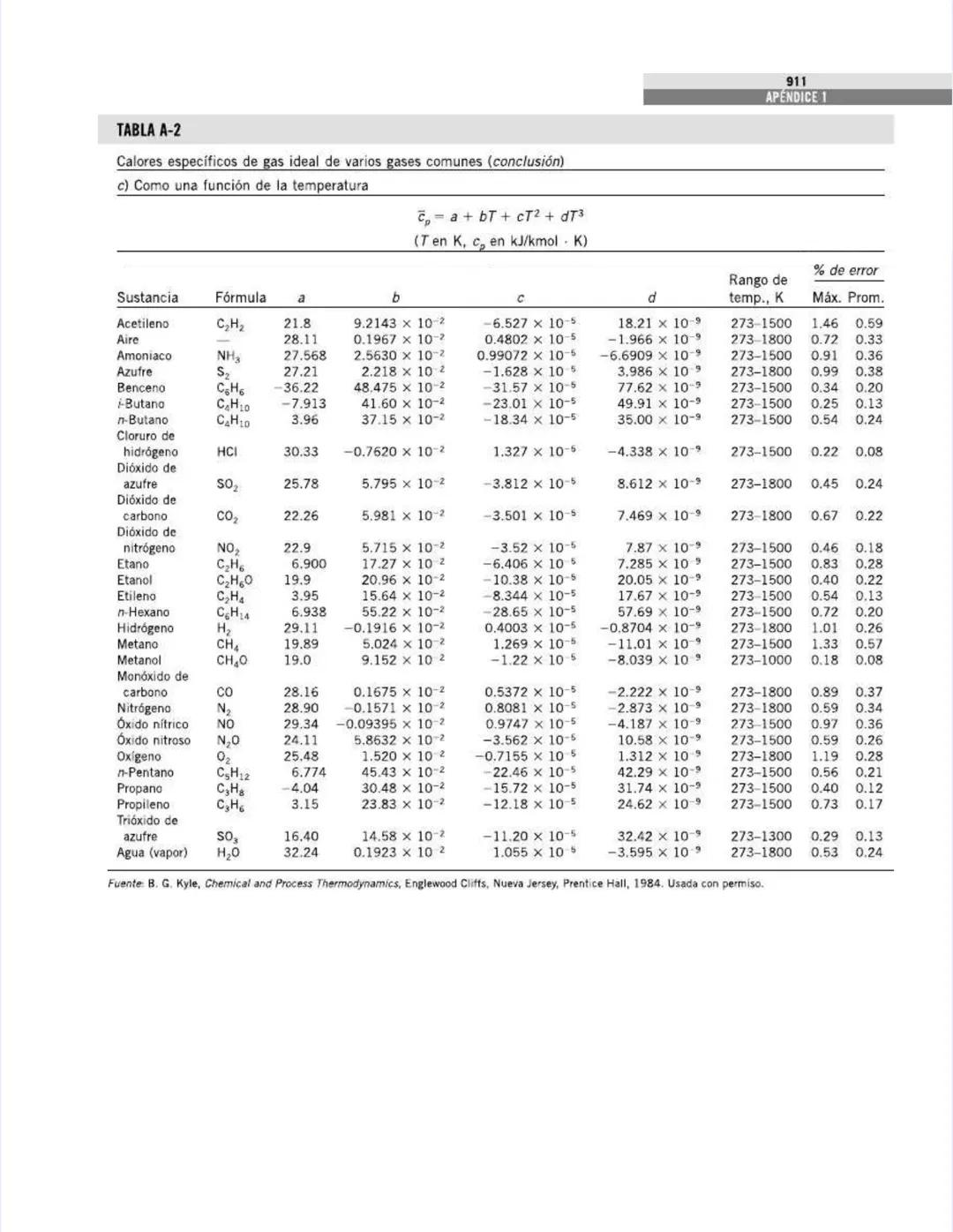
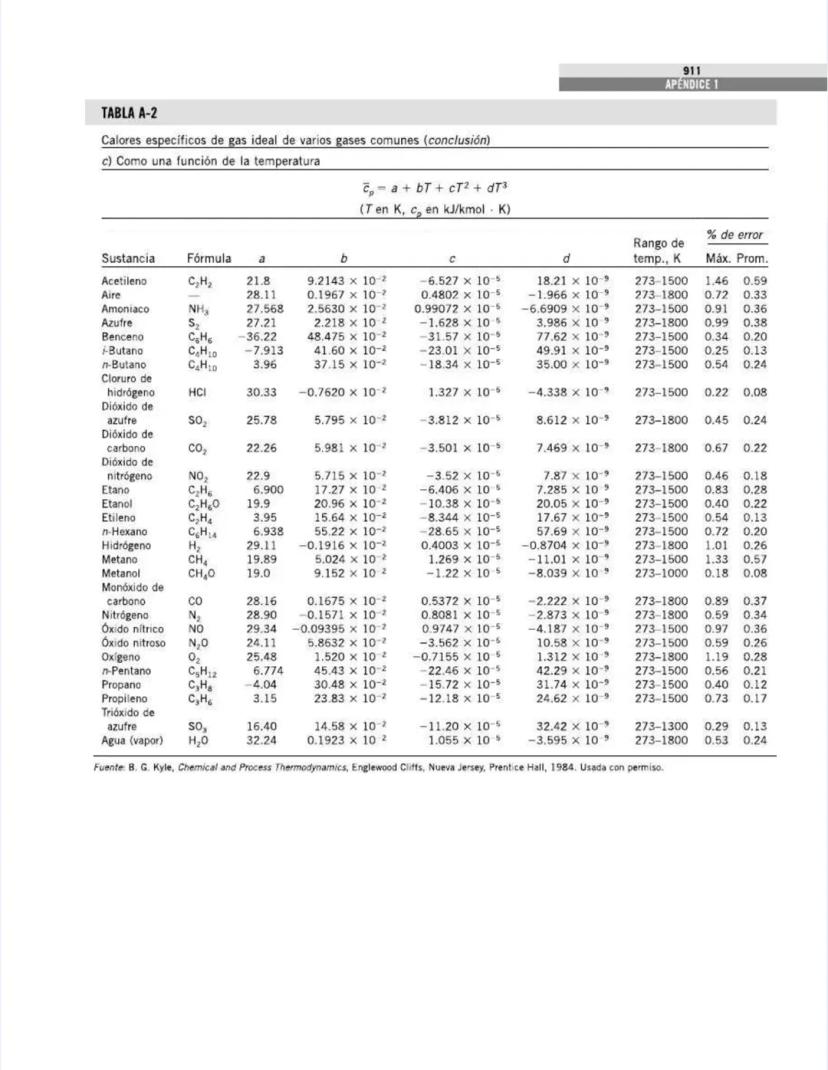
Esta tabla proporciona ecuaciones polinómicas para calcular calores específicos con mayor precisión. La fórmula general es:
cp = a + bT + cT² + dT³
donde T está en Kelvin y cp en kJ/kmol·K (¡nota que es por kmol, no por kg!).
Para sustancias como el metano (CH₄), los coeficientes son:
Estas ecuaciones son extremadamente valiosas para:
La tabla también muestra el rango de temperatura donde estas ecuaciones son válidas, generalmente entre 273-1500 K o 273-1800 K, así como el porcentaje de error máximo y promedio.
El agua (vapor) tiene un comportamiento bastante complejo, con coeficientes:
💡 Para convertir los calores específicos de base molar a base másica , simplemente divide por la masa molar de la sustancia. Por ejemplo, para el CO₂ con masa molar de 44.01 kg/kmol, divide los valores calculados por 44.01.
Estas relaciones permiten programar modelos termodinámicos precisos y resolver problemas complejos que requieren integración de cp en amplios rangos de temperatura.
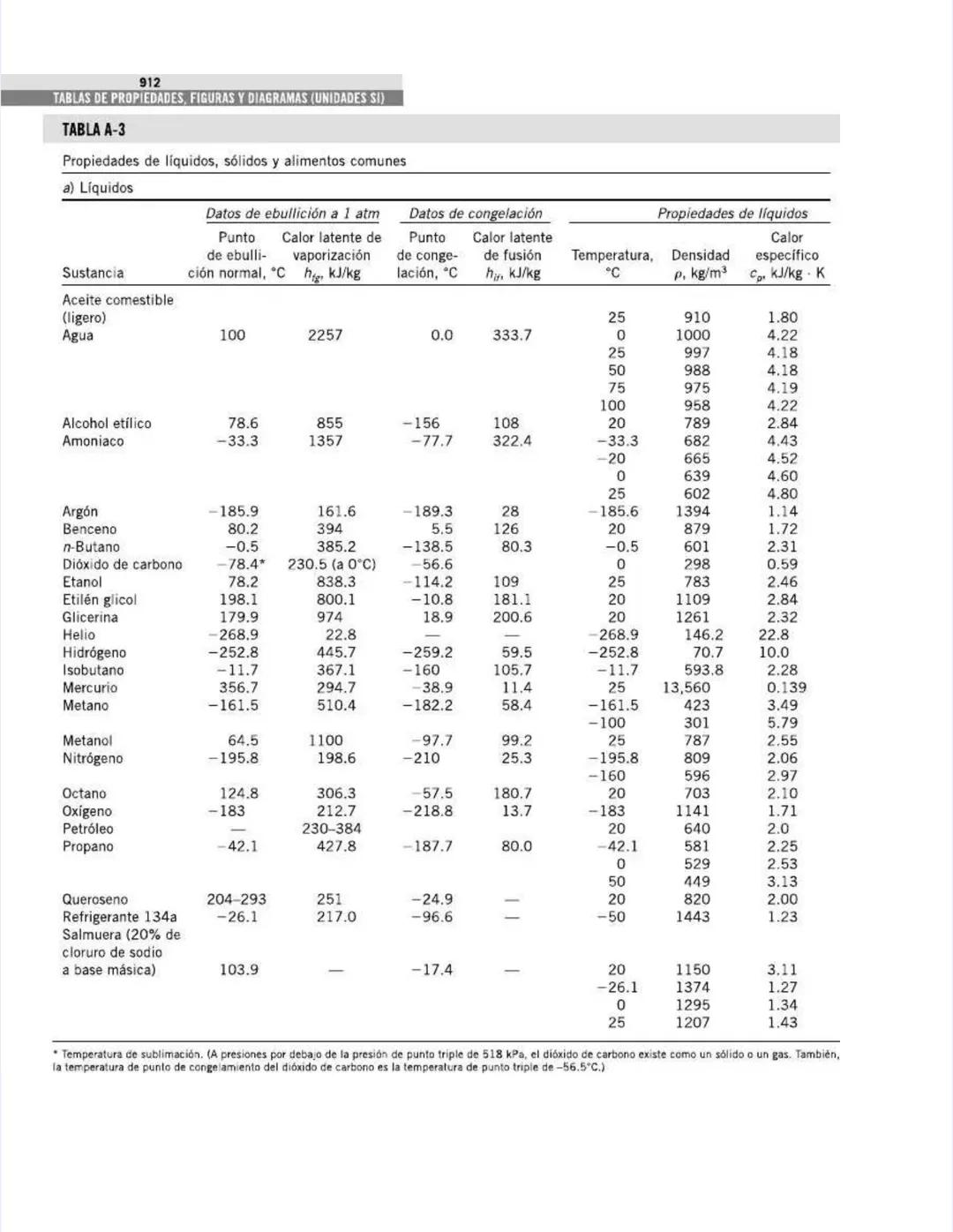
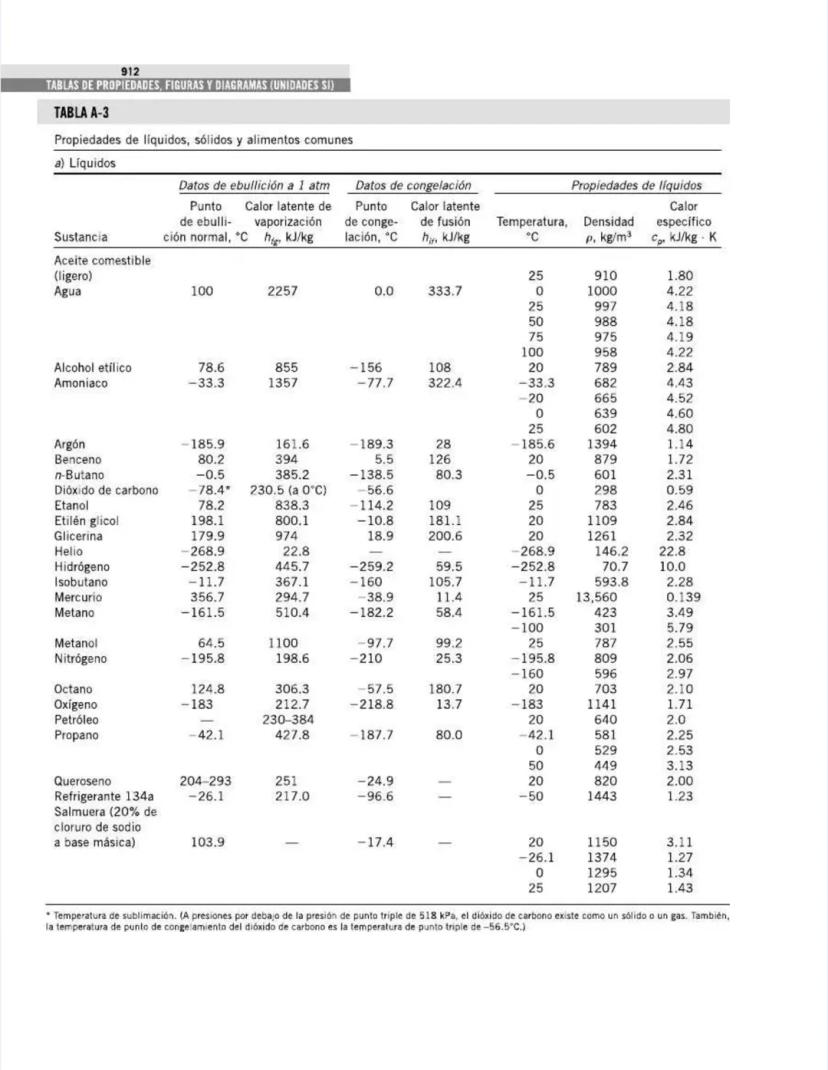
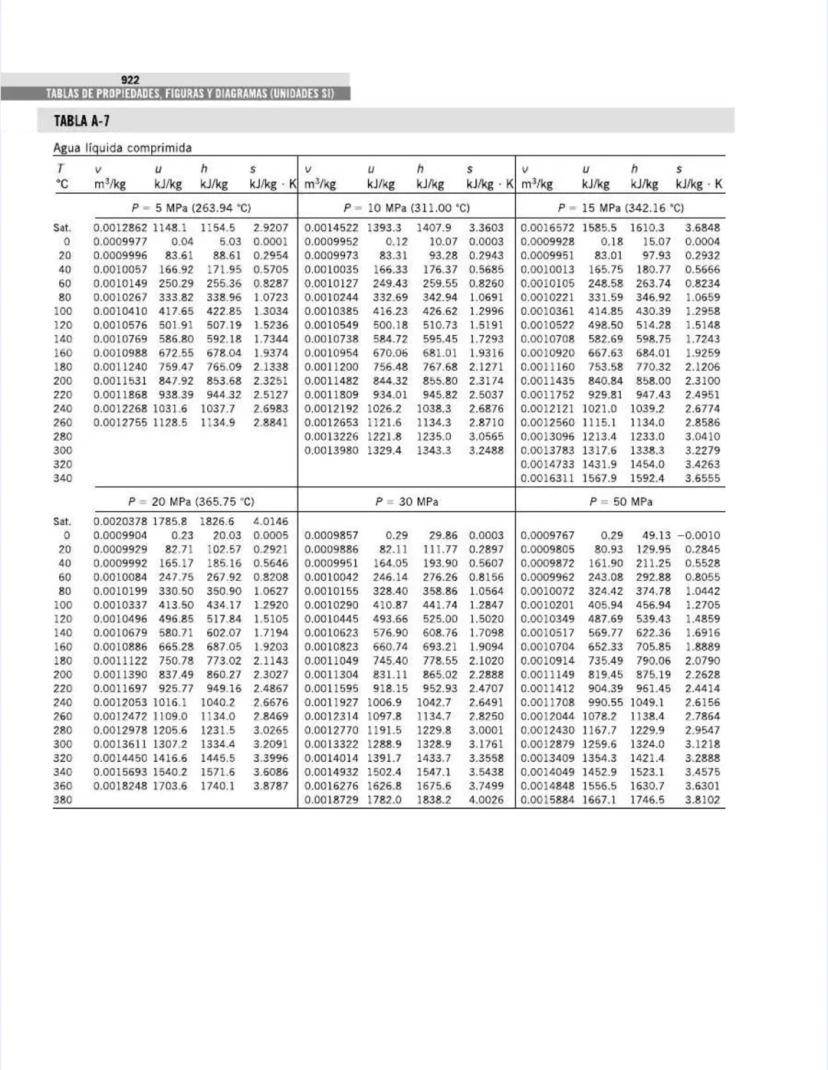
Esta tabla es un recurso invaluable para aplicaciones prácticas de ingeniería. Contiene propiedades físicas de sustancias en estados diferentes al gaseoso.
Para los líquidos, encuentras datos esenciales como:
Por ejemplo, el agua a 25°C tiene una densidad de 997 kg/m³ y un calor específico de 4.18 kJ/kg·K, mientras que el mercurio tiene una densidad mucho mayor pero un calor específico mucho menor .
Para refrigerantes como el amoniaco, puedes encontrar que tiene un calor latente de vaporización de 1357 kJ/kg a -33.3°C, un dato crucial para diseño de sistemas de refrigeración.
Observa cómo la densidad de la mayoría de los líquidos disminuye con la temperatura. Por ejemplo, el agua:
Esta información es esencial para calcular:
💡 El calor latente de vaporización disminuye a medida que aumenta la temperatura, llegando a cero en el punto crítico. Esta es una consideración importante en ciclos de potencia y refrigeración que operan cerca de condiciones críticas.
La tabla incluye también datos para petróleo, queroseno y salmuera, que son fluidos ampliamente utilizados en aplicaciones industriales.
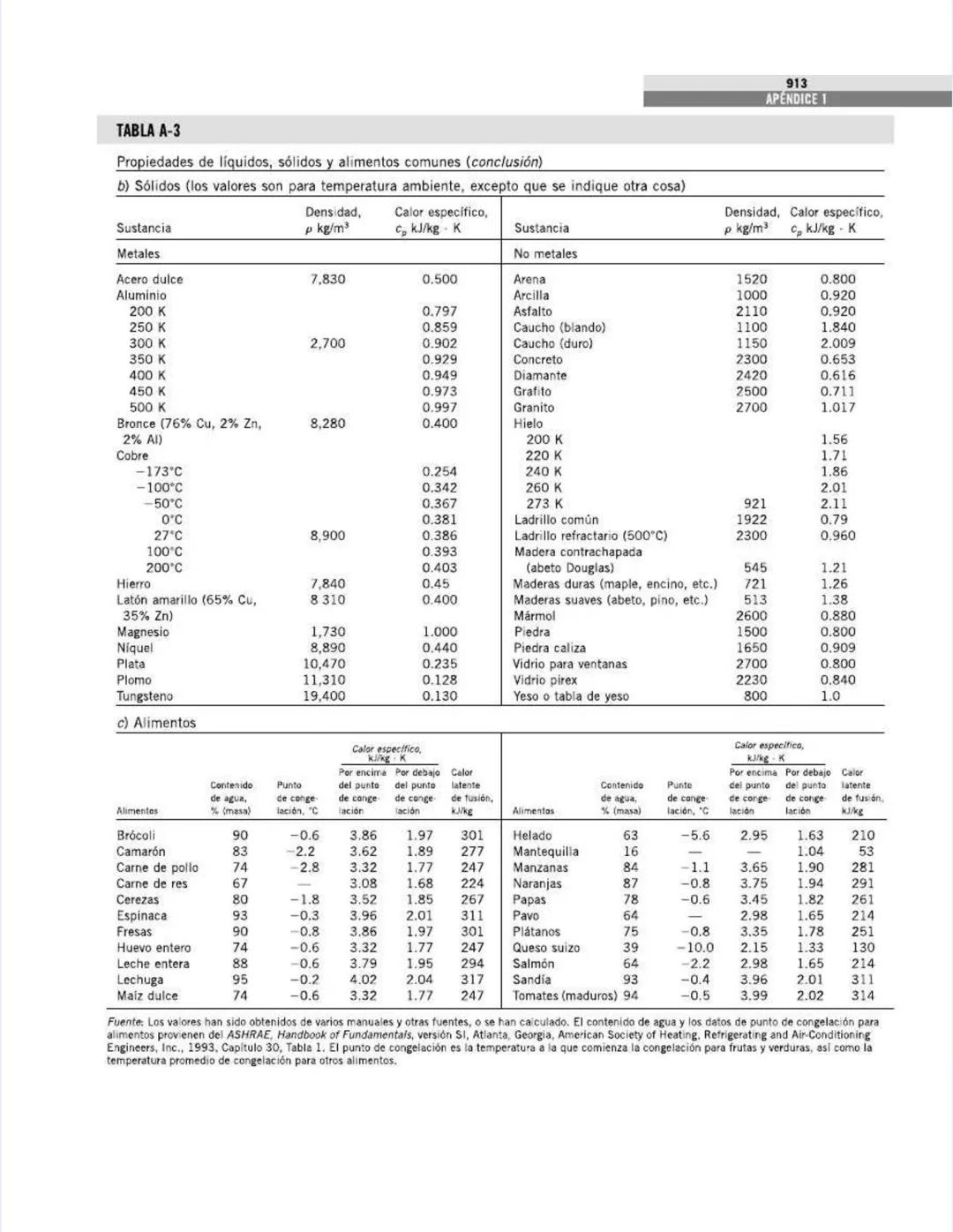
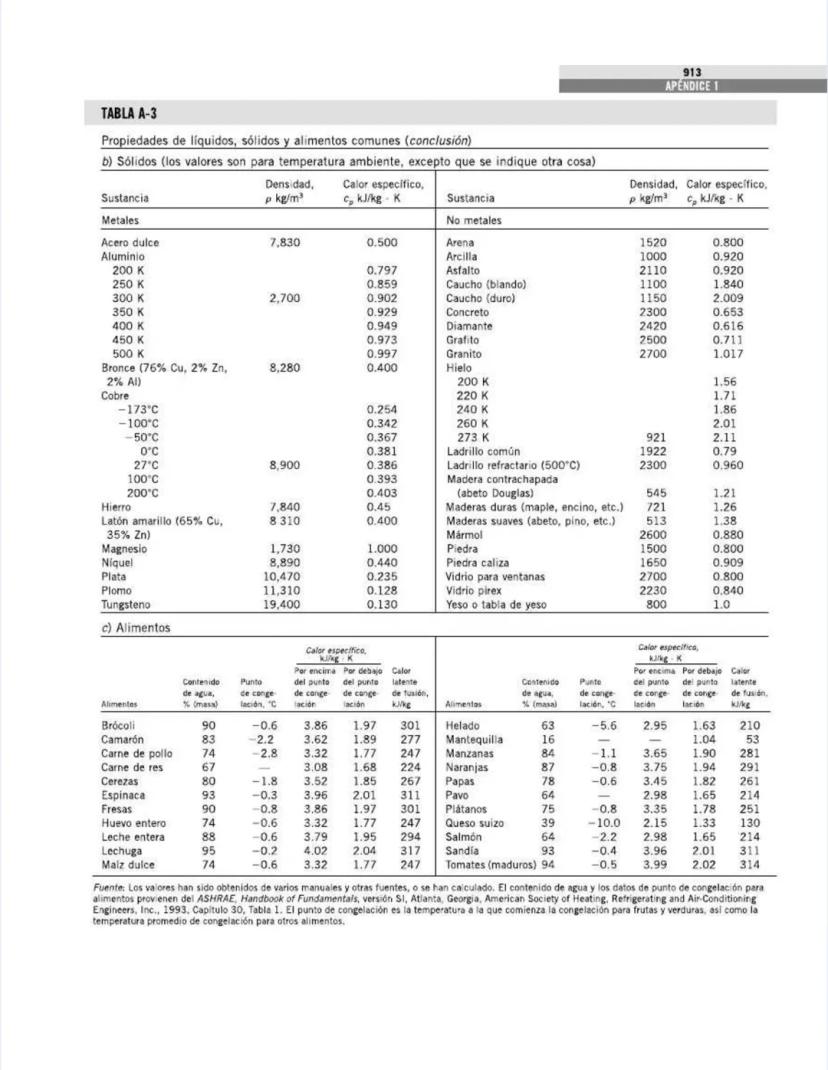
Esta tabla continúa ofreciendo datos valiosos, ahora para sólidos y alimentos, información crucial para aplicaciones de transferencia de calor e ingeniería alimentaria.
Para los sólidos, la tabla muestra:
Comparando metales:
Los materiales de construcción muestran propiedades interesantes:
Para los alimentos, la tabla proporciona:
Las frutas y verduras tienen alto contenido de agua:
El contenido de agua afecta directamente el calor específico y el calor latente. Por ejemplo:
💡 Estos datos son fundamentales para el diseño de procesos de congelación, almacenamiento y cocción de alimentos. La gran diferencia entre calores específicos de alimentos congelados y no congelados explica por qué los tiempos de descongelación son mucho mayores que los de congelación.
Utiliza esta información para cálculos de refrigeración, procesamiento térmico y diseño de sistemas de almacenamiento.
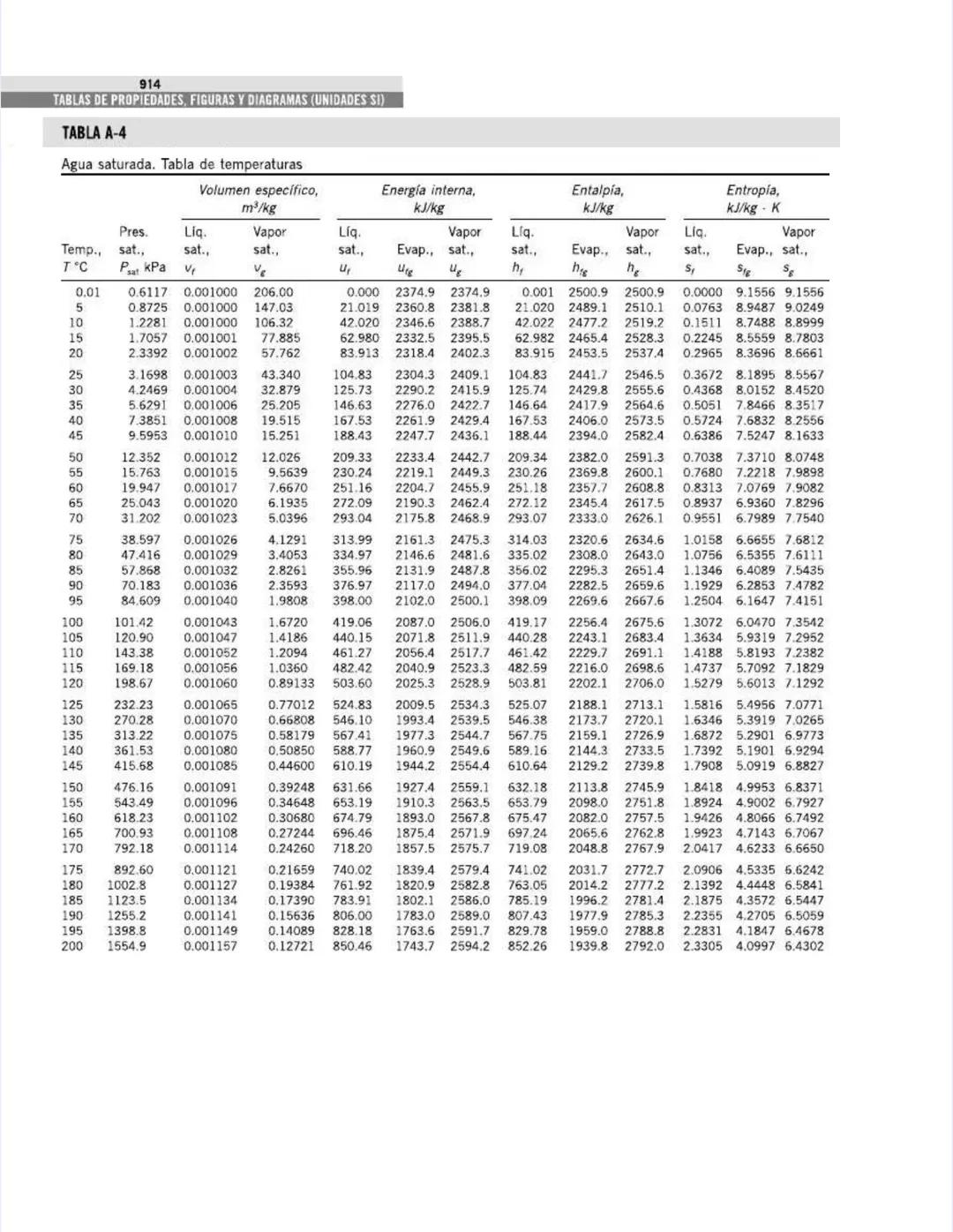
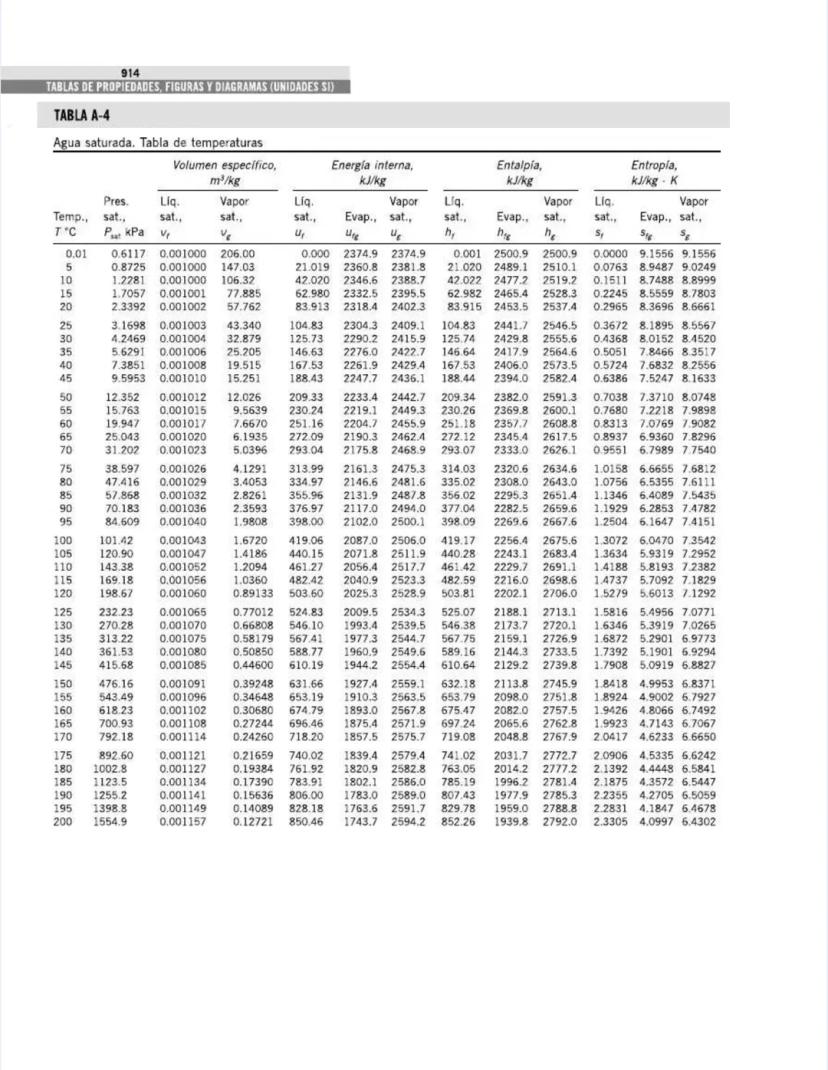
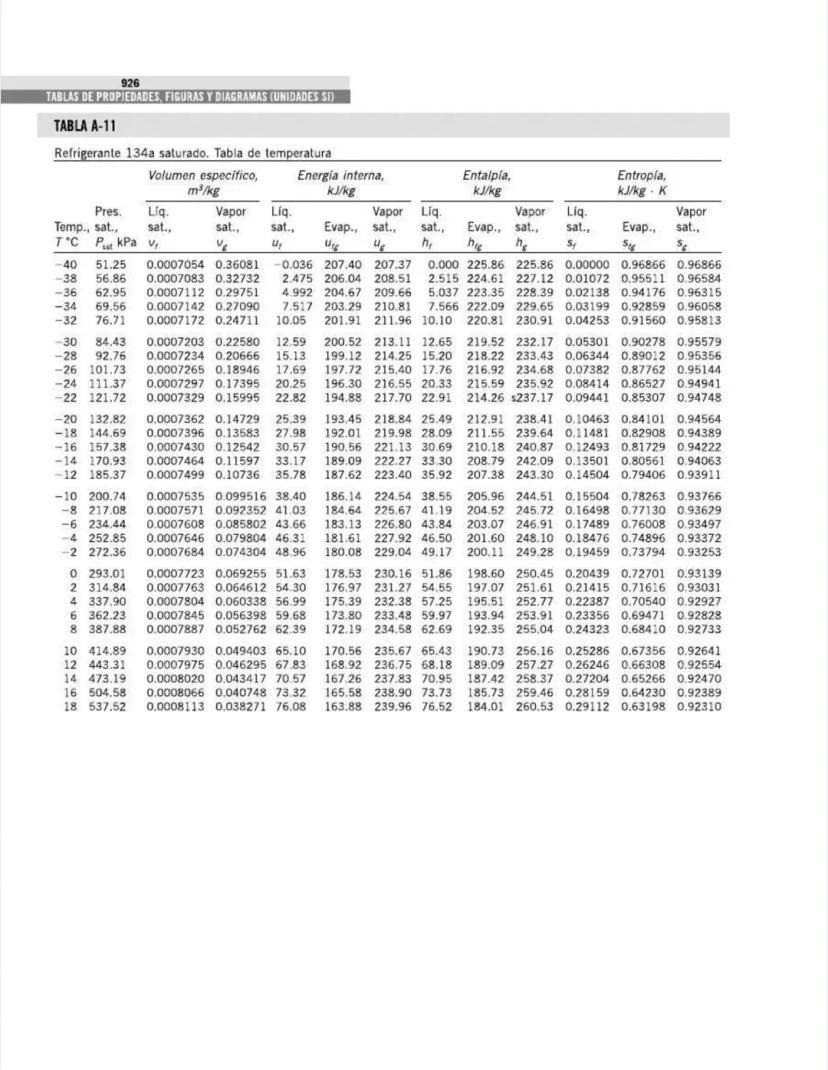
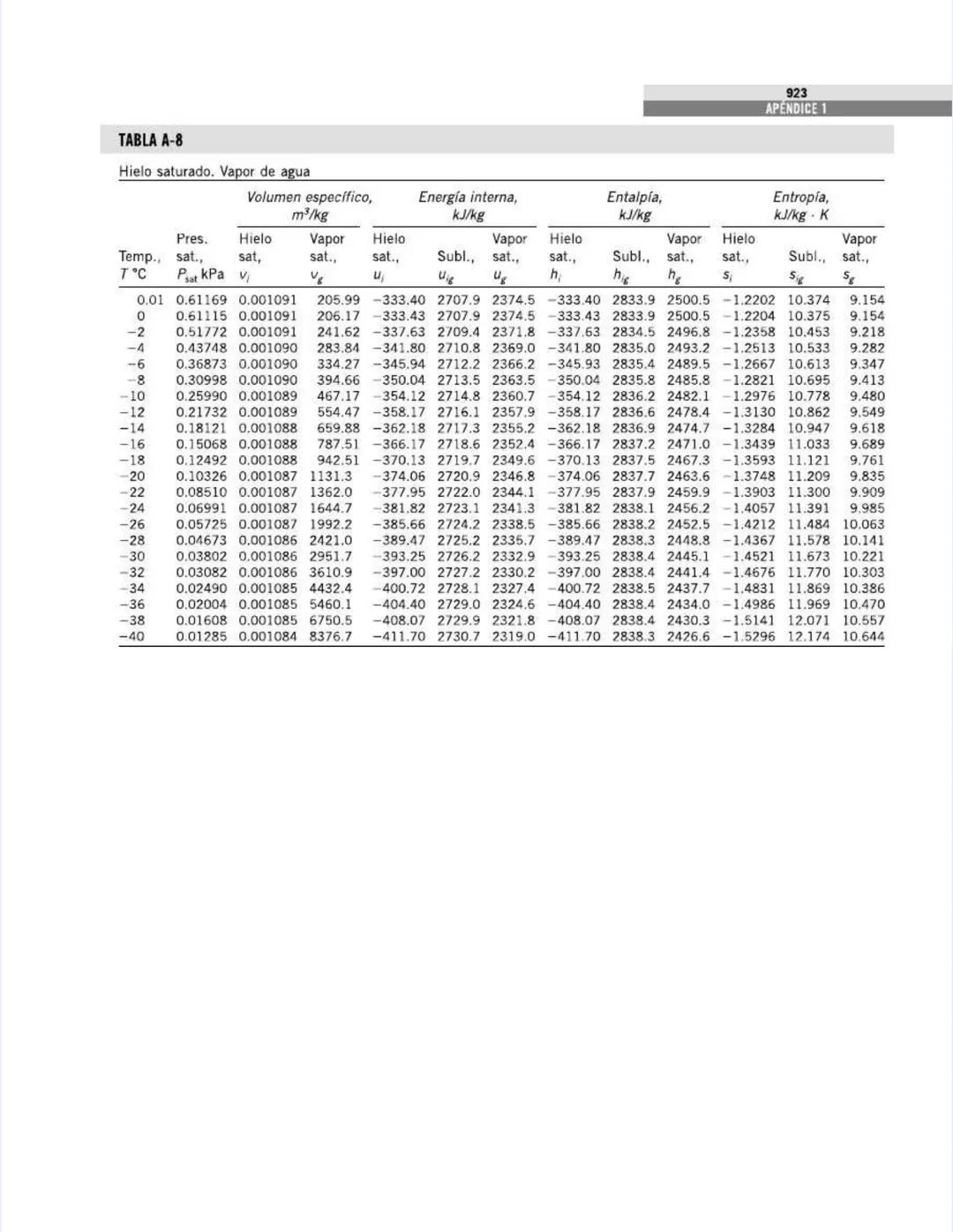
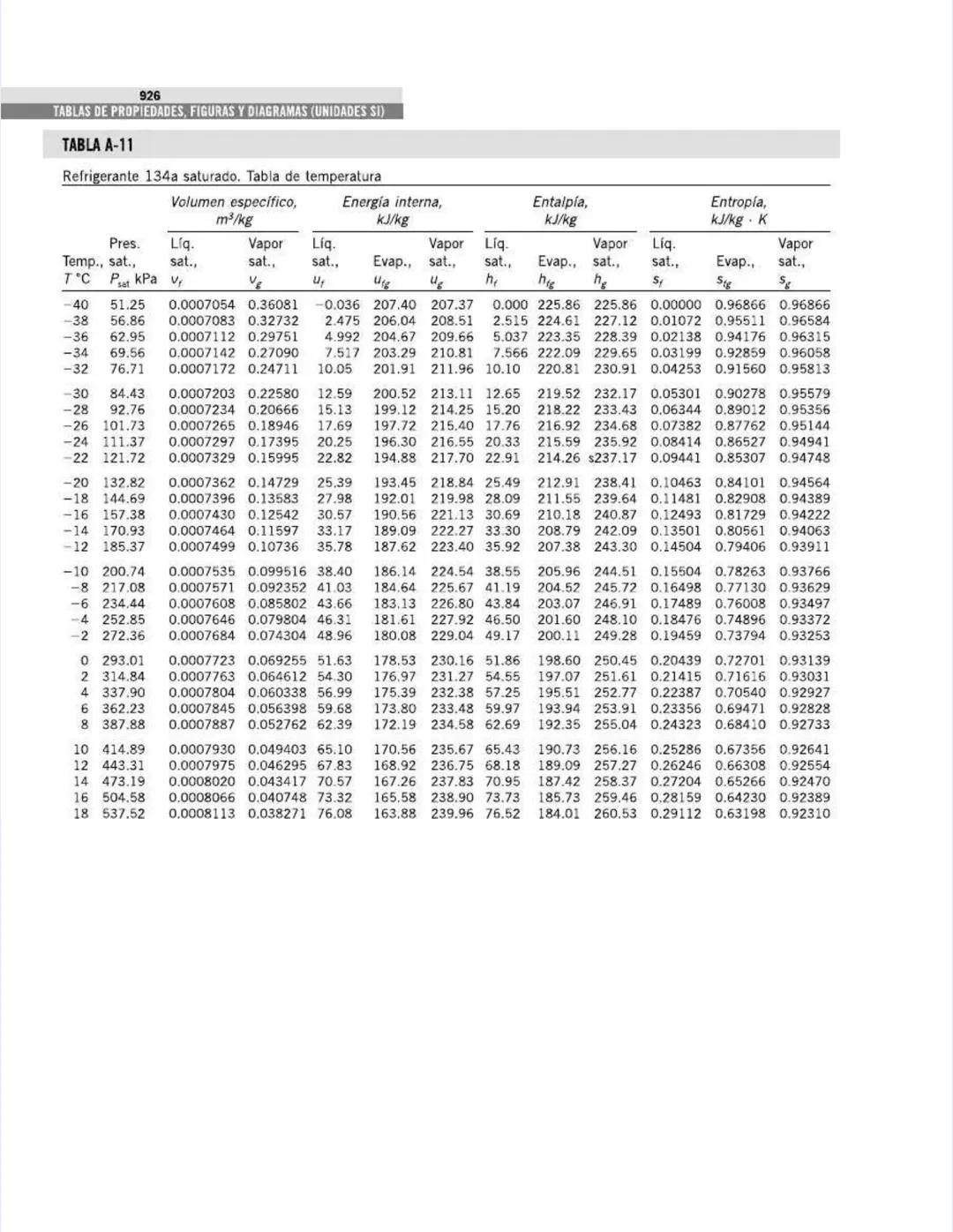
Esta tabla es una de las más utilizadas en termodinámica. Proporciona las propiedades del agua saturada a diferentes temperaturas, permitiéndote encontrar rápidamente valores fundamentales para análisis de ciclos de potencia, refrigeración y sistemas térmicos.
La tabla está organizada por temperatura y muestra:
Por ejemplo, a 20°C:
Observa cómo estas propiedades cambian con la temperatura:
💡 En el punto crítico (374°C), el calor latente se vuelve cero y las propiedades del líquido y vapor son idénticas. Este comportamiento es fundamental para entender ciclos supercríticos en centrales eléctricas modernas.
Esta tabla será tu referencia constante para resolver problemas de transferencia de calor, ciclos de Rankine y procesos de evaporación o condensación.
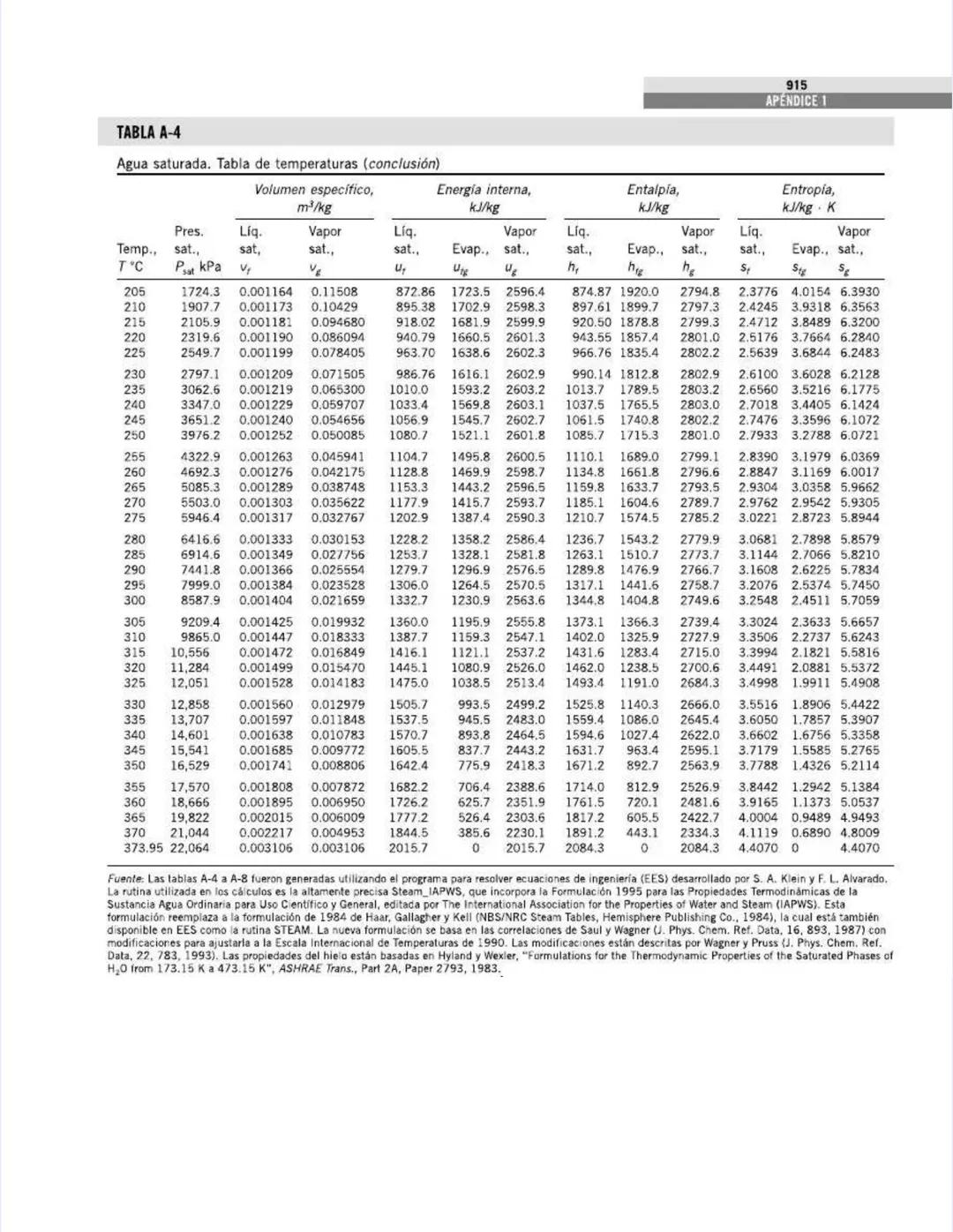
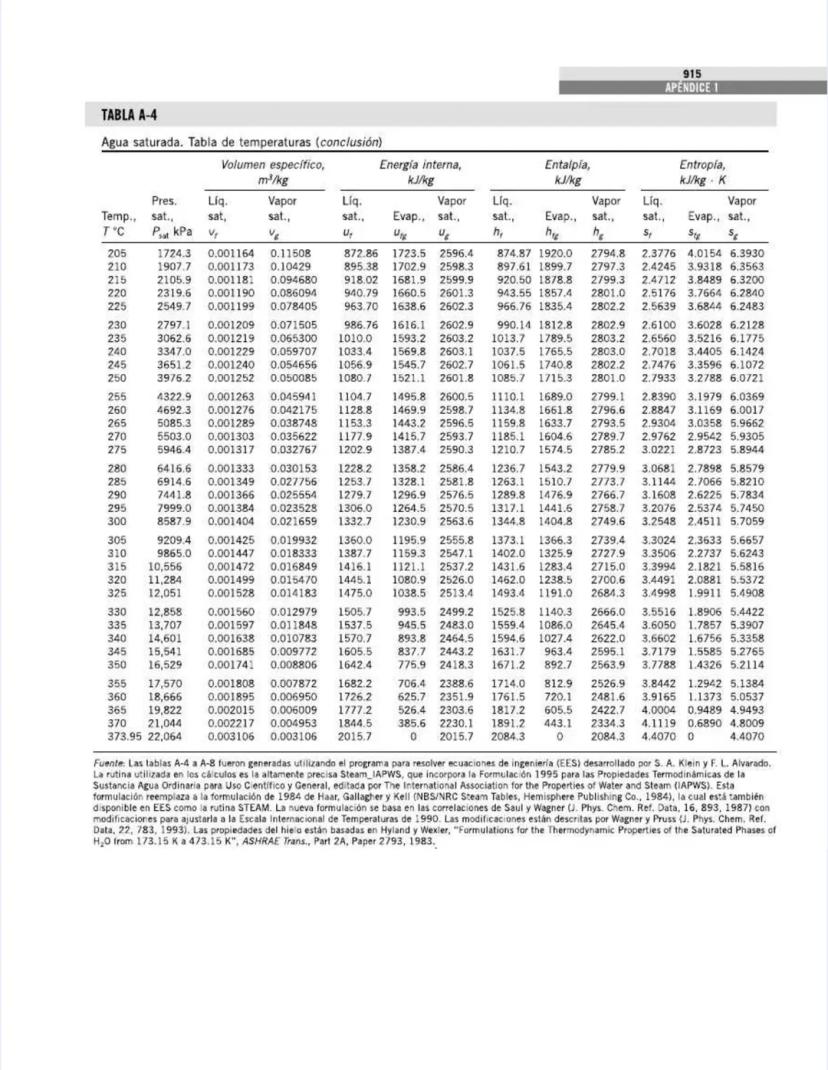
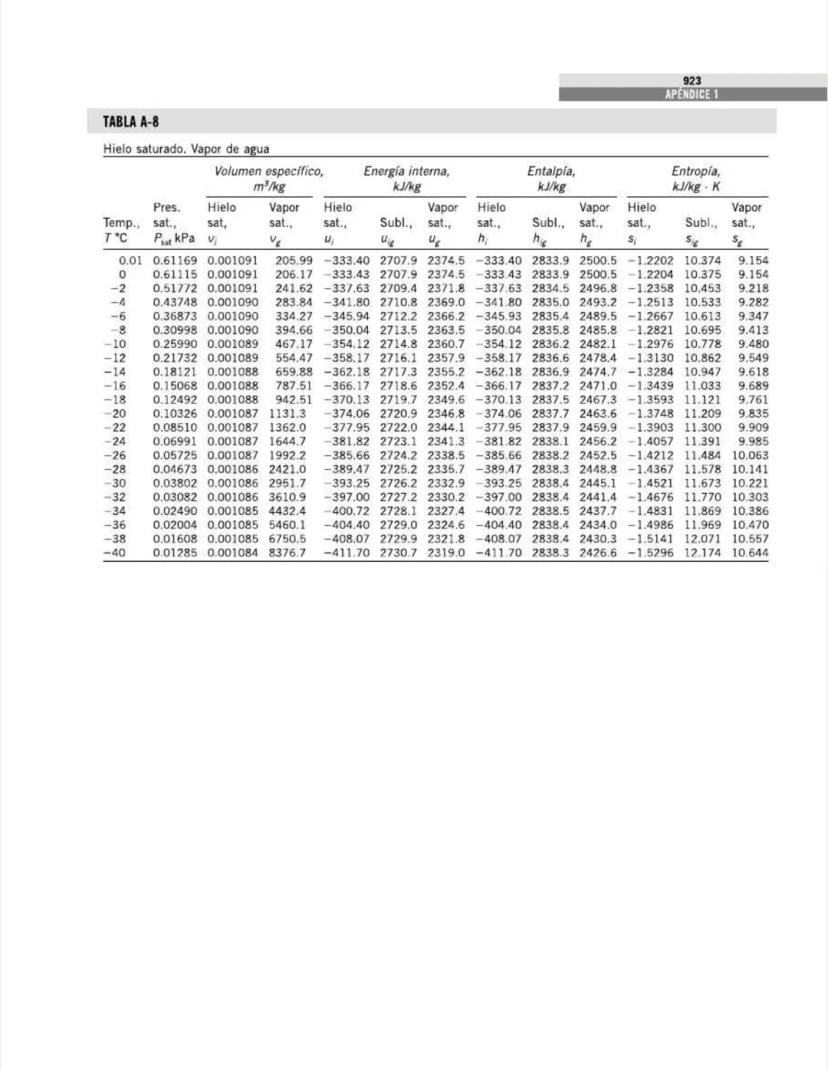
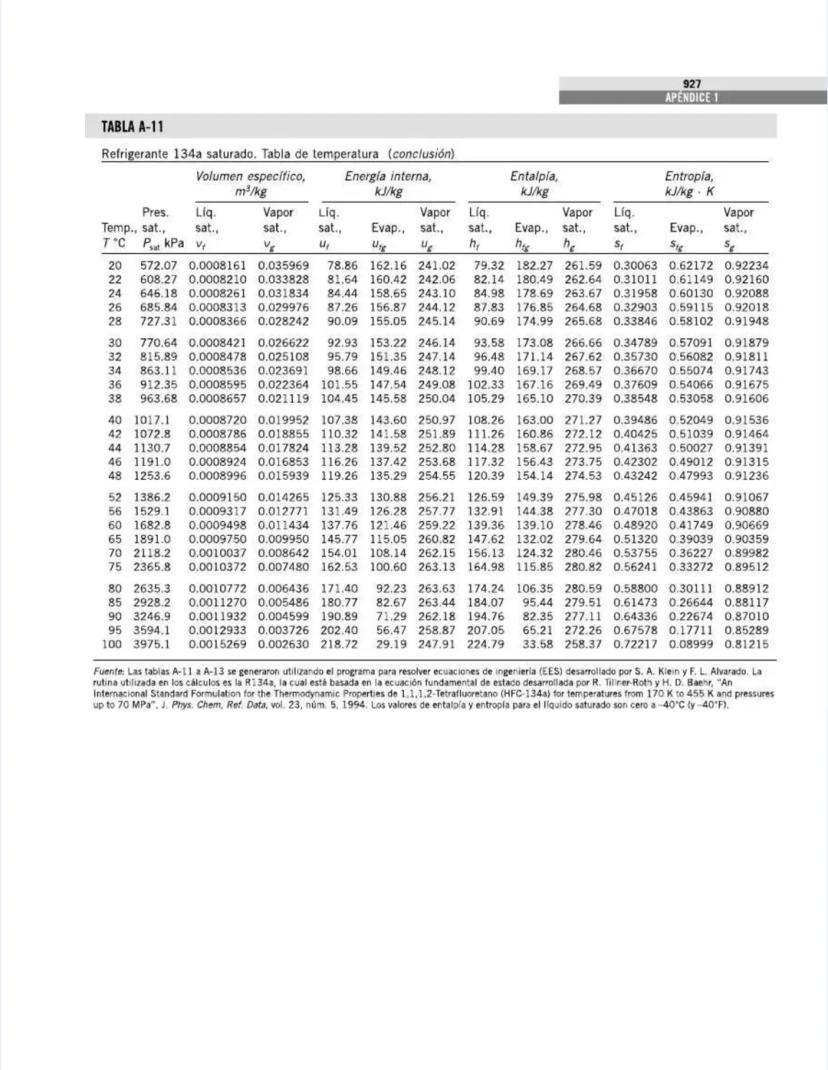
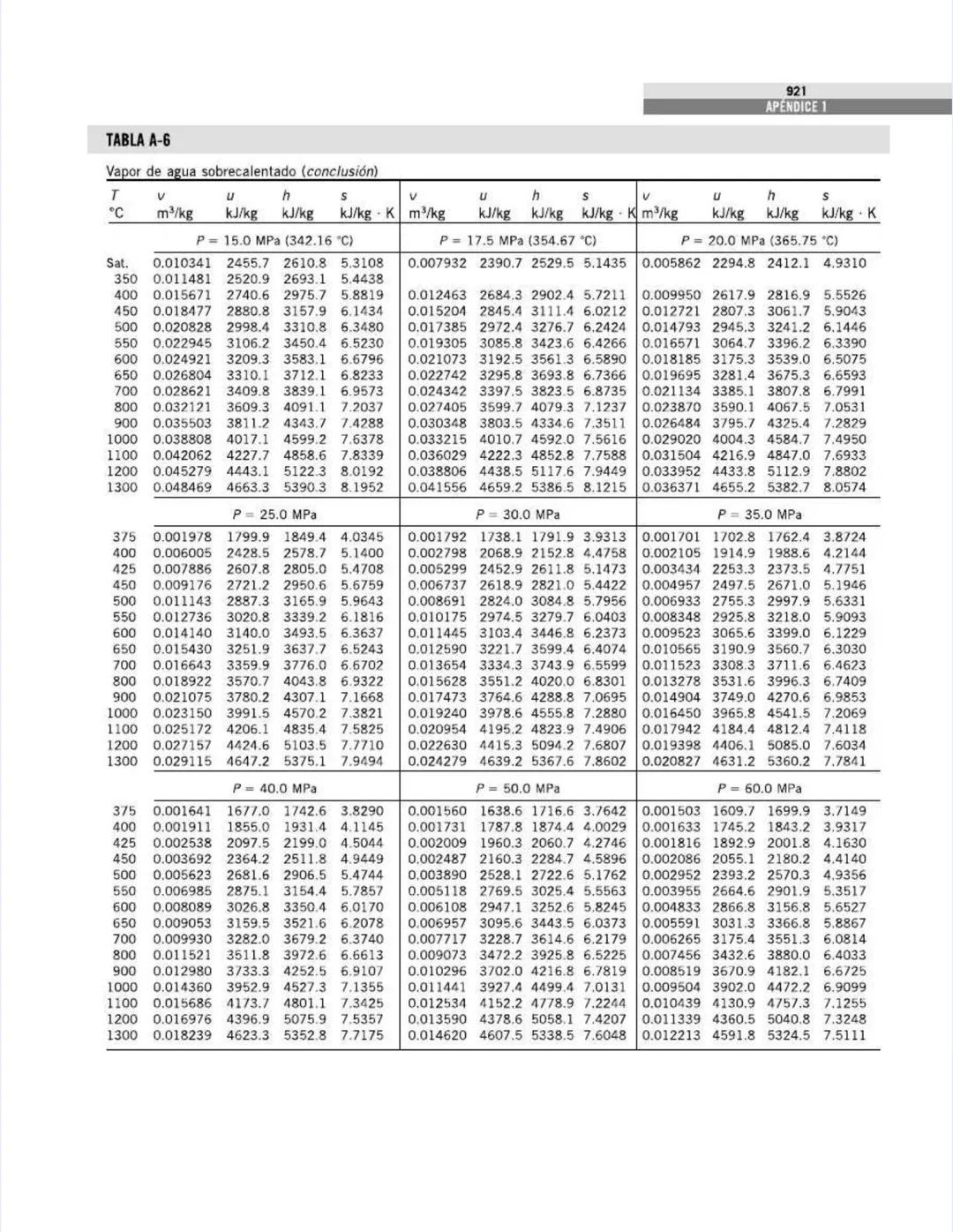
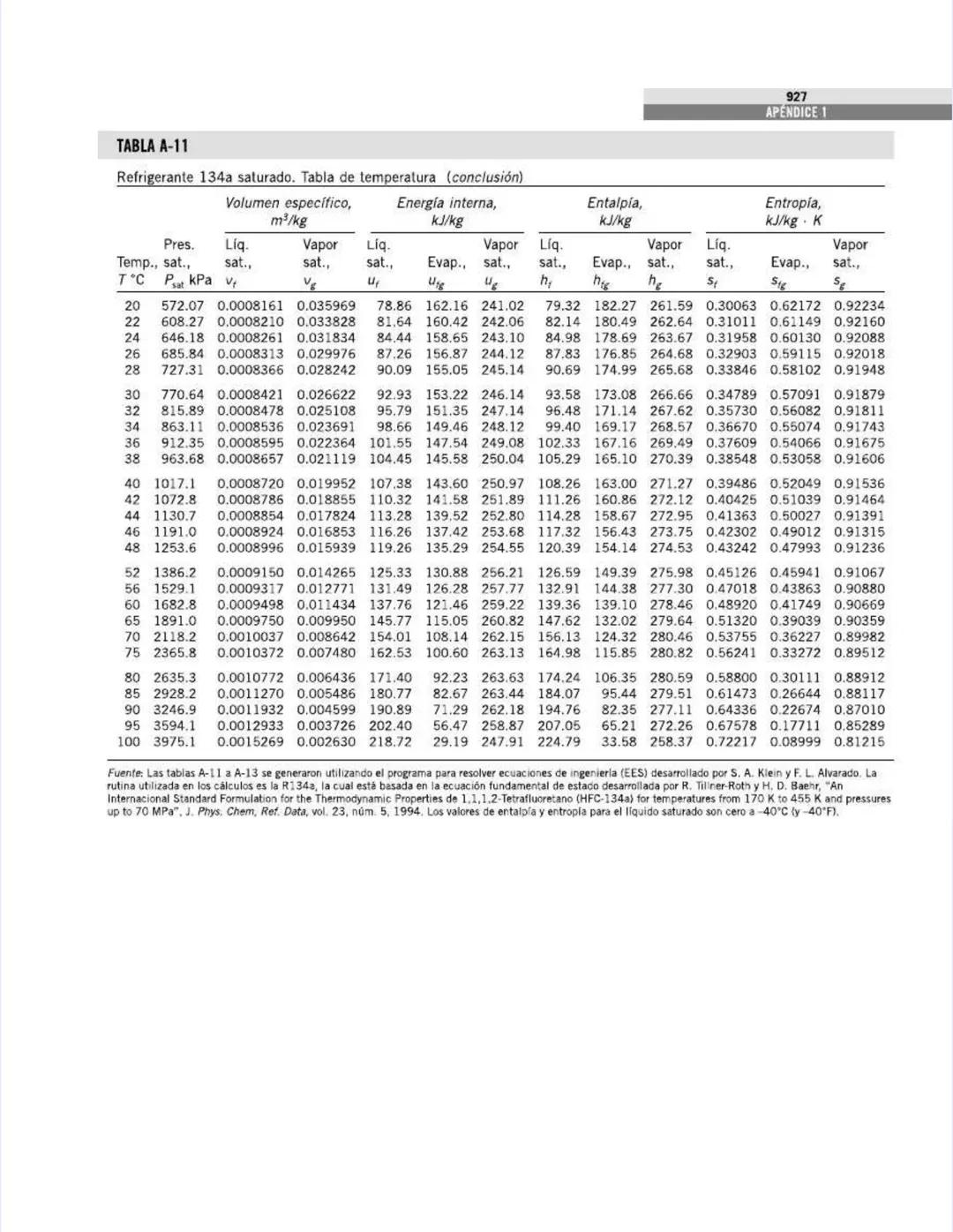
La tabla continúa mostrando las propiedades del agua saturada, ahora para temperaturas más altas (205°C a 373.95°C).
A medida que la temperatura se acerca al punto crítico (373.95°C), observa estas tendencias importantes:
La presión de saturación aumenta exponencialmente:
El volumen específico del líquido aumenta mientras el del vapor disminuye:
El calor latente disminuye hasta llegar a cero:
La diferencia de entropía entre líquido y vapor también disminuye:
💡 Estas tendencias son cruciales para entender el comportamiento de ciclos de potencia y refrigeración. En centrales termoeléctricas supercríticas, el agua no experimenta un cambio de fase distinto, lo que mejora la eficiencia térmica.
La tabla fue generada con ecuaciones de estado de alta precisión , que representa una mejora respecto a formulaciones anteriores y garantiza valores precisos para tus cálculos de ingeniería.
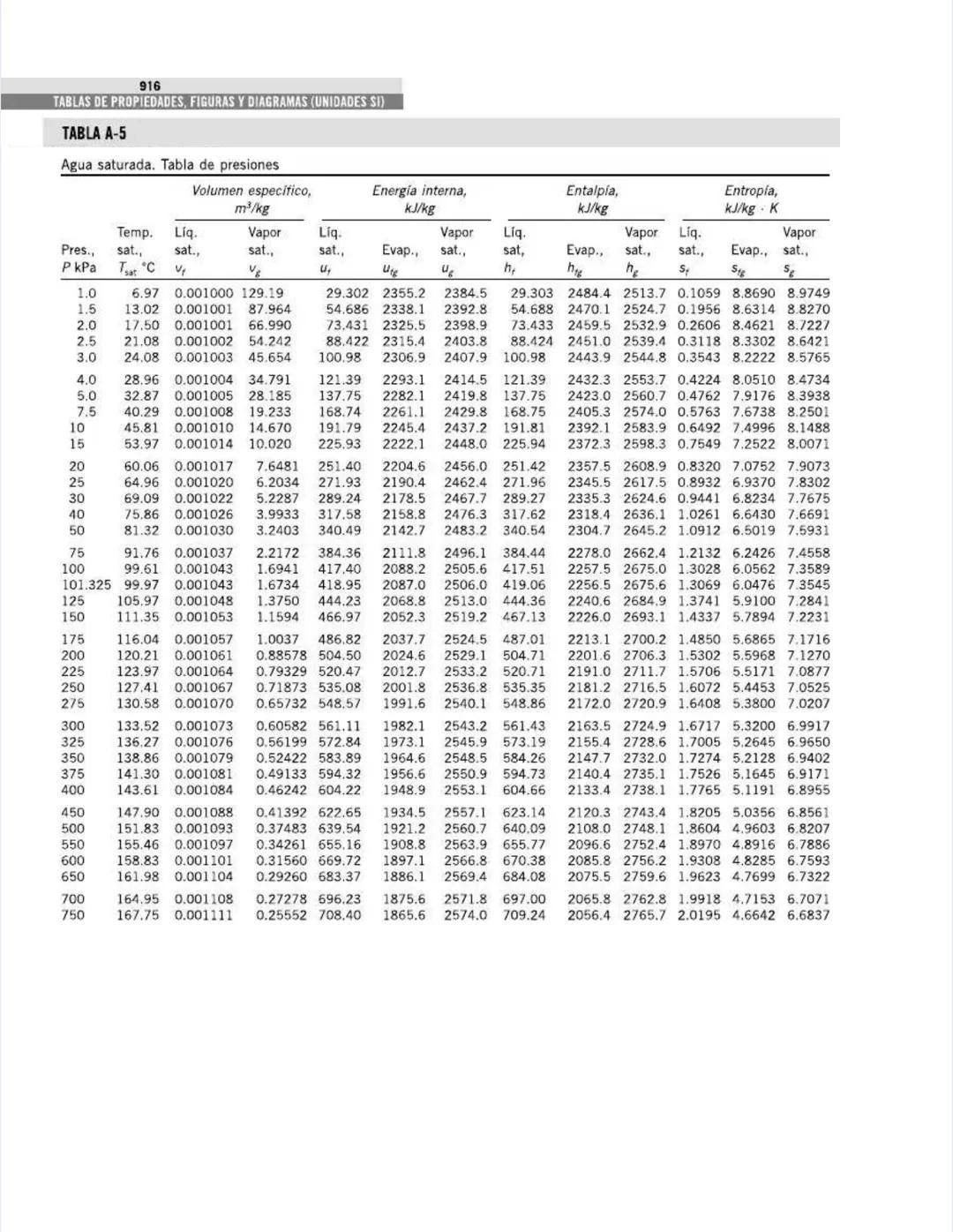
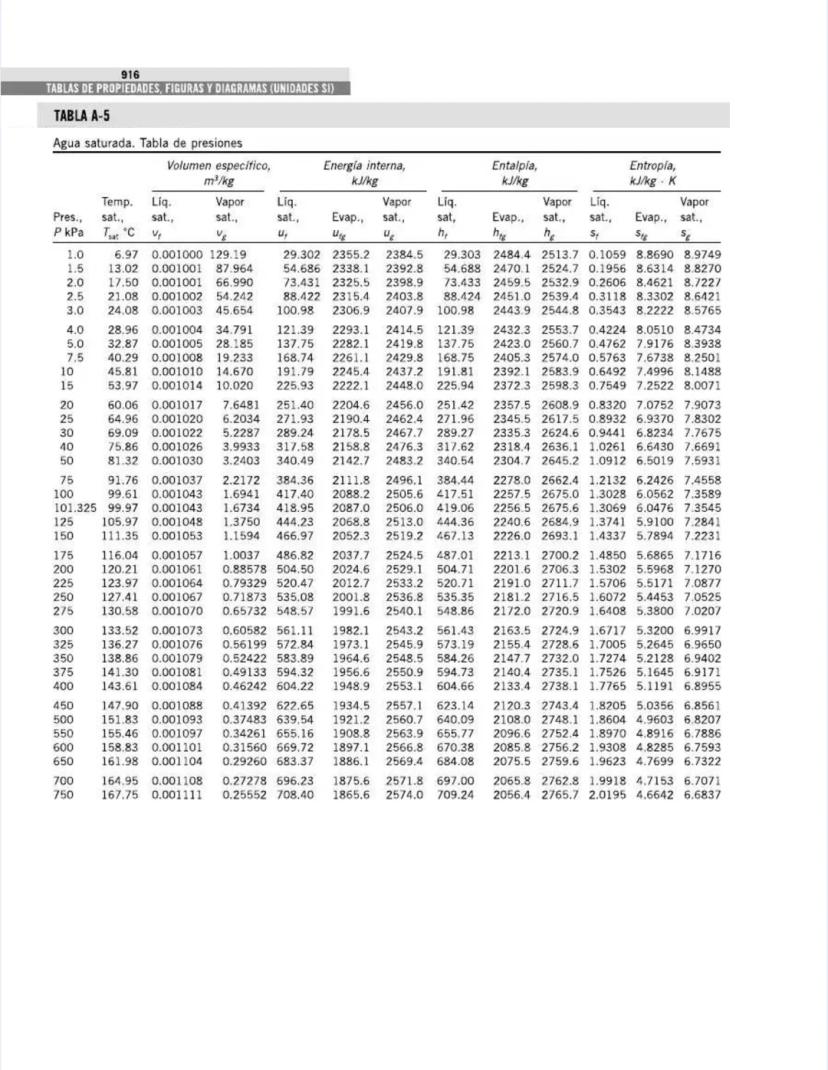
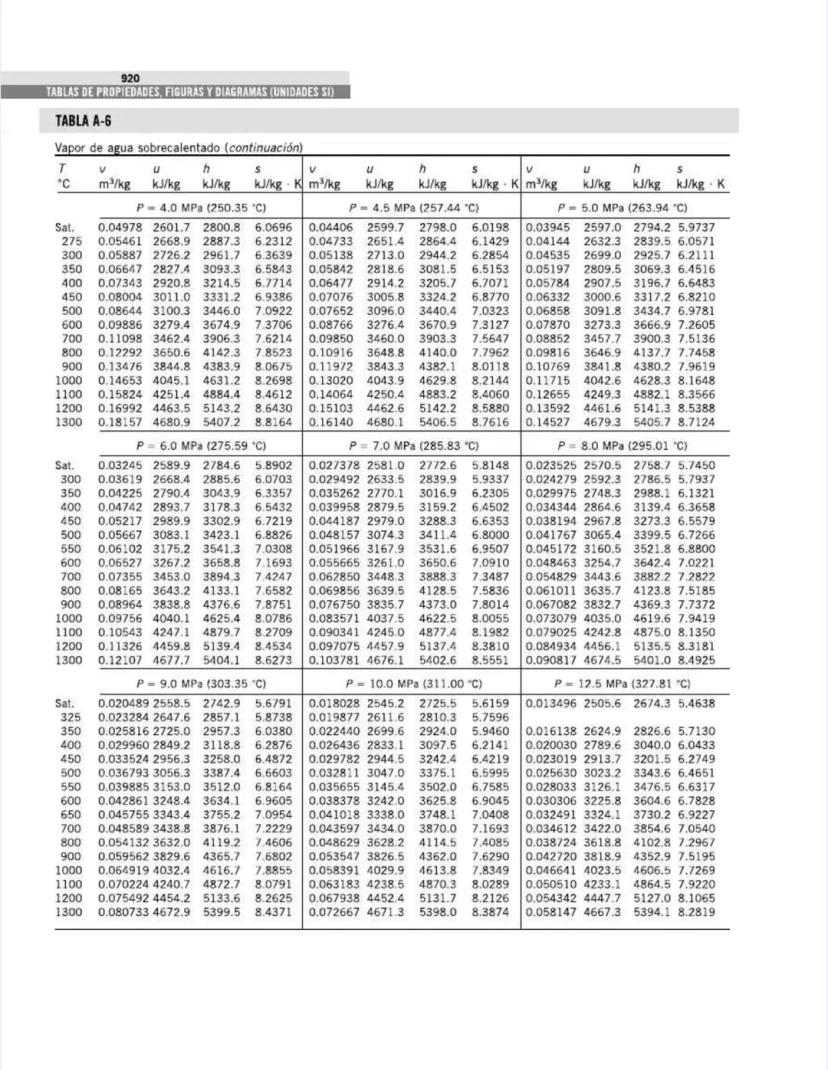
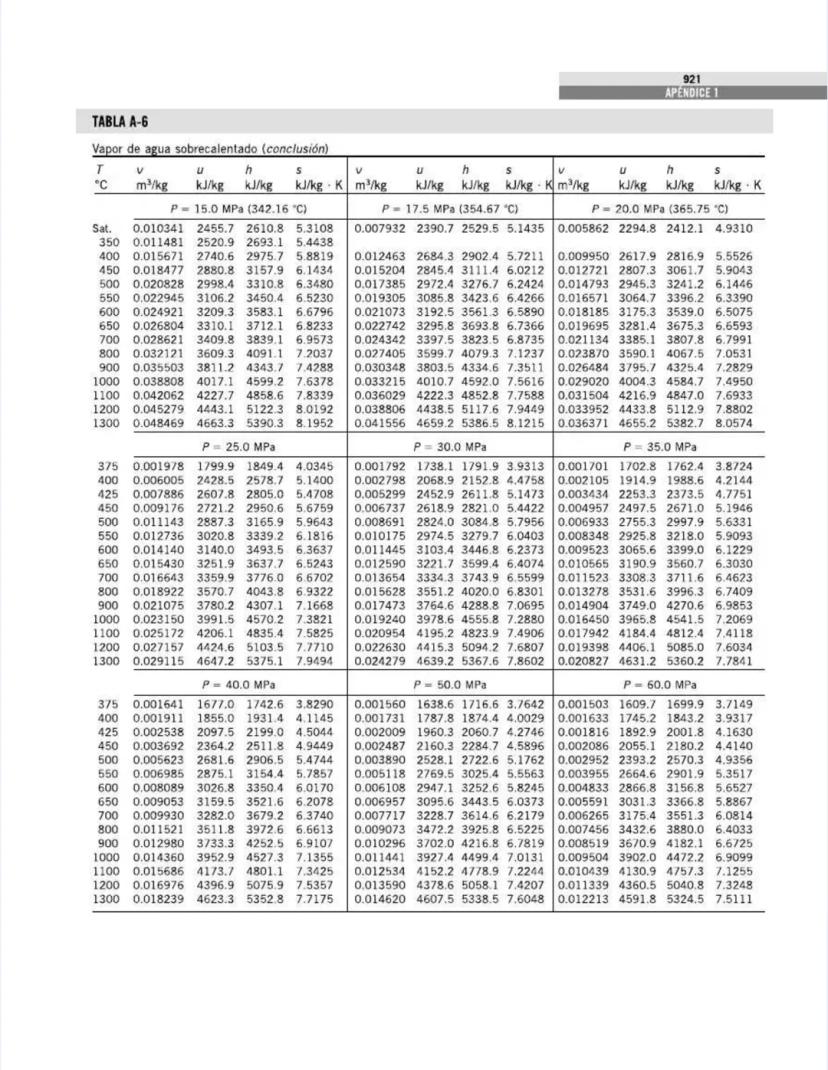
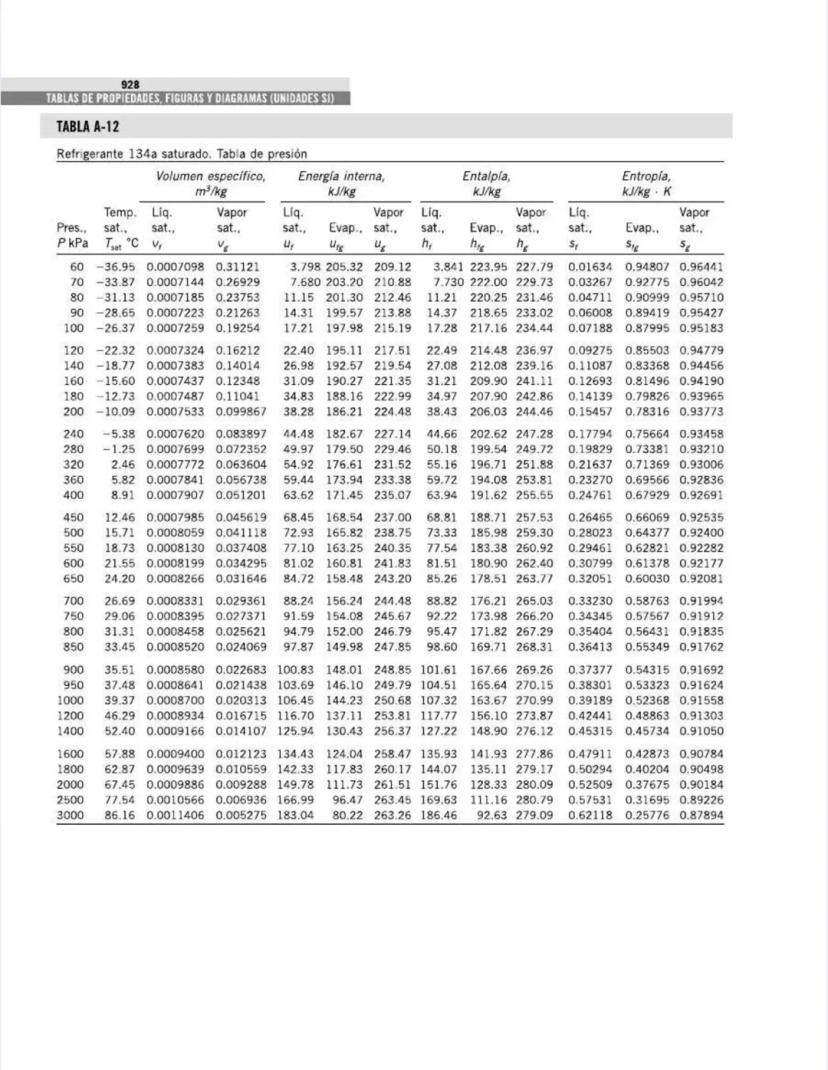
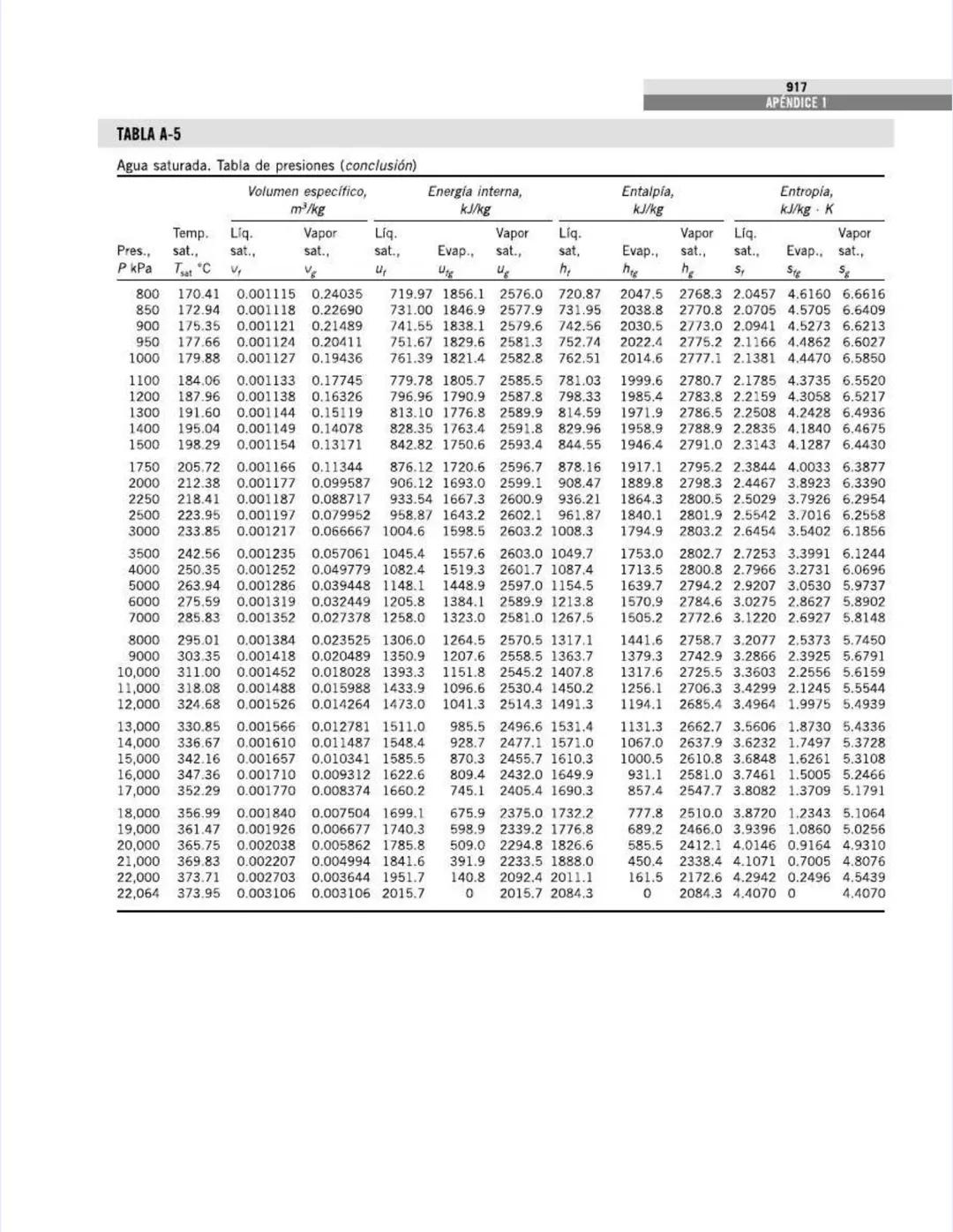
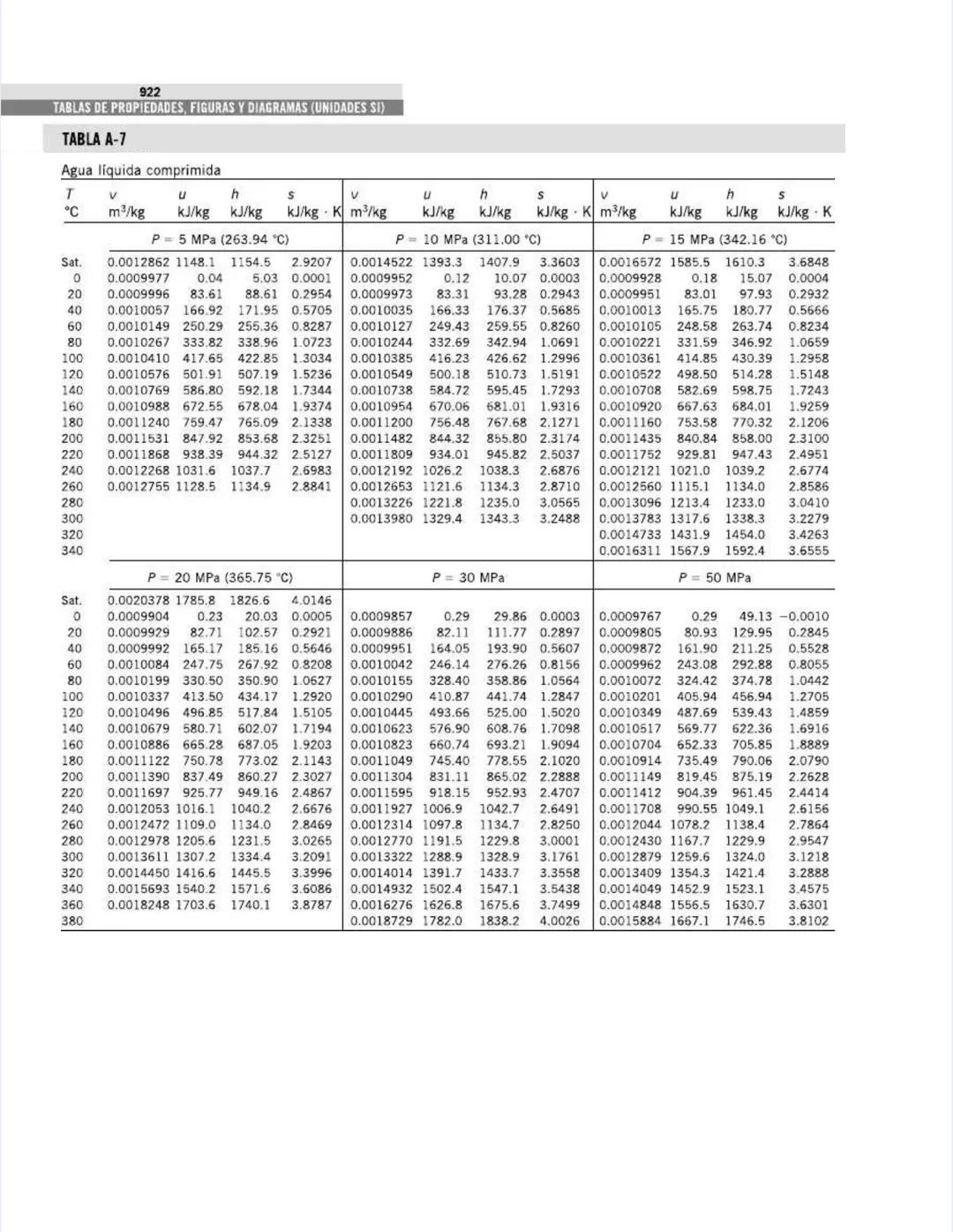
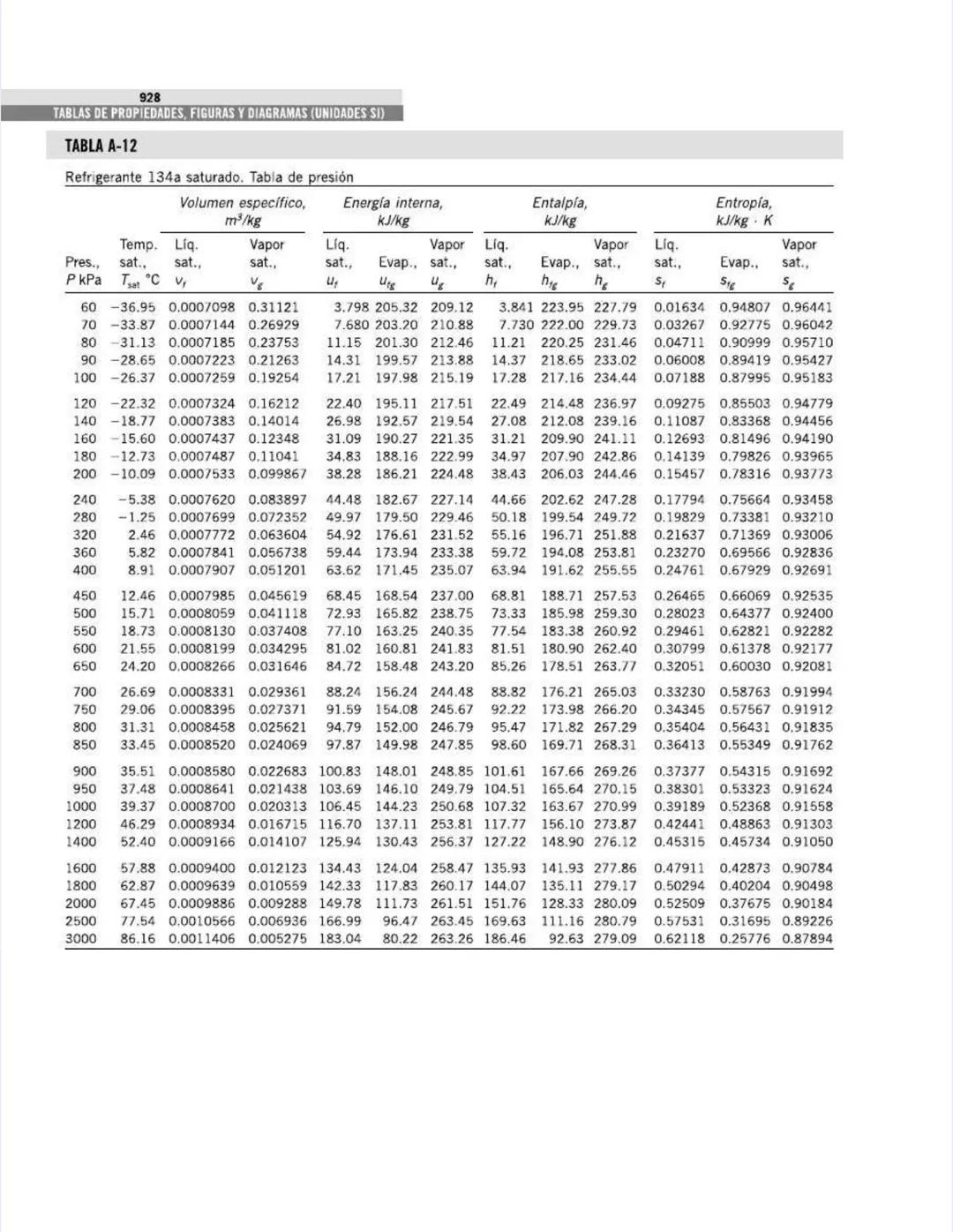
Esta tabla complementa la anterior, pero ahora está organizada por presiones en lugar de temperaturas. Es particularmente útil para análisis de ciclos de potencia y sistemas que operan a presiones específicas.
Para cada presión, puedes encontrar:
Por ejemplo, a presión atmosférica (101.325 kPa):
Para análisis de ciclos de Rankine, observa los valores a presiones típicas:
La tabla cubre un amplio rango de presiones, desde vacío parcial (1 kPa) hasta presiones supercríticas (22,064 kPa), permitiéndote analizar desde condensadores de baja presión hasta calderas de alta presión.
💡 La presión crítica del agua es 22.06 MPa, donde el calor latente se vuelve cero. En sistemas supercríticos, no hay una distinción clara entre líquido y vapor, lo que permite ciclos más eficientes al eliminar la necesidad de calor latente durante el cambio de fase.
Esta tabla es fundamental para dimensionar equipos térmicos como calderas, condensadores, y turbinas de vapor.


Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
Danna Contreras
@dannacont_qqt8s
Las tablas de propiedades termodinámicas son herramientas esenciales para resolver problemas de ingeniería. Estas tablas contienen información detallada sobre el comportamiento de diversas sustancias bajo diferentes condiciones, lo que te permitirá realizar cálculos precisos en tus cursos de termodinámica y... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
¡Tienes en tus manos un tesoro para ingenieros! Esta página nos presenta el contenido de las tablas y figuras que usarás constantemente en tus clases de termodinámica.
Las tablas están organizadas por tipo de sustancia y propiedades. En la Tabla A-1 encontrarás información fundamental como la masa molar y las constantes de gas para diversas sustancias, desde el agua hasta gases nobles como el helio. Estas propiedades son la base para muchos cálculos termodinámicos.
Las tablas incluyen datos de propiedades críticas (temperatura, presión y volumen) que son cruciales para entender el comportamiento de las sustancias cerca de sus puntos críticos, donde las fases líquida y gaseosa se vuelven indistinguibles.
También encontrarás tablas específicas para sustancias comunes como agua, refrigerantes, y gases como nitrógeno, oxígeno y dióxido de carbono. Estas tablas te permitirán determinar propiedades como entalpía, entropía y energía interna a diferentes temperaturas y presiones.
💡 No memorices estos datos, pero familiarízate con la organización de las tablas. Saber dónde encontrar cada propiedad te ahorrará tiempo valioso durante exámenes y proyectos.
Las figuras y diagramas incluyen herramientas visuales importantes como el diagrama T-s y el diagrama de Mollier para el agua, que te ayudarán a analizar ciclos termodinámicos de manera eficiente.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Esta tabla es una mina de oro para tus cálculos termodinámicos. Contiene la masa molar, la constante de gas y las propiedades del punto crítico para diversas sustancias.
La masa molar (M) se expresa en kg/kmol y es fundamental para convertir entre unidades molares y másicas. Por ejemplo, el agua (H₂O) tiene una masa molar de 18.015 kg/kmol, mientras que el aire tiene 28.97 kg/kmol.
La constante específica de gas (R) varía para cada sustancia y es crucial para la ecuación de estado de gases ideales . Para el agua es 0.4615 kJ/kg·K, mientras que para el hidrógeno es 4.1240 kJ/kg·K, ¡casi diez veces mayor!
Las propiedades críticas son valores límite donde el comportamiento de las sustancias cambia drásticamente:
Estas propiedades críticas son esenciales cuando trabajas con ciclos de refrigeración, procesos de extracción supercrítica o sistemas de generación de energía.
💡 La relación entre la constante universal de gases R₀ = 8.31447 kJ/kmol·K y la constante específica R para cualquier sustancia es: R = R₀/M, donde M es la masa molar de la sustancia.
Esta tabla será tu referencia para numerosos problemas que involucren ecuaciones de estado y cálculos de propiedades de gases.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Esta tabla es fundamental para tus cálculos de energía térmica. Los calores específicos representan la cantidad de energía necesaria para cambiar la temperatura de una sustancia y son propiedades esenciales en termodinámica.
A 300 K (temperatura ambiente), observa las diferencias significativas entre gases:
La relación entre calores específicos es crucial para calcular procesos isentrópicos:
La tabla también muestra cómo los calores específicos aumentan con la temperatura. Por ejemplo, para el aire:
En la tercera parte de la tabla, encontrarás ecuaciones polinómicas para calcular Cp a diferentes temperaturas, expresadas como: cp = a + bT + cT² + dT³. Estas ecuaciones son extremadamente útiles para análisis de combustión y cálculos de ciclos de potencia a altas temperaturas.
💡 Recuerda siempre que la diferencia entre Cp y Cv para un gas ideal es simplemente la constante del gas: Cp - Cv = R
Utiliza estos valores cuando calcules trabajo, calor, cambios de entropía y eficiencias en ciclos termodinámicos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
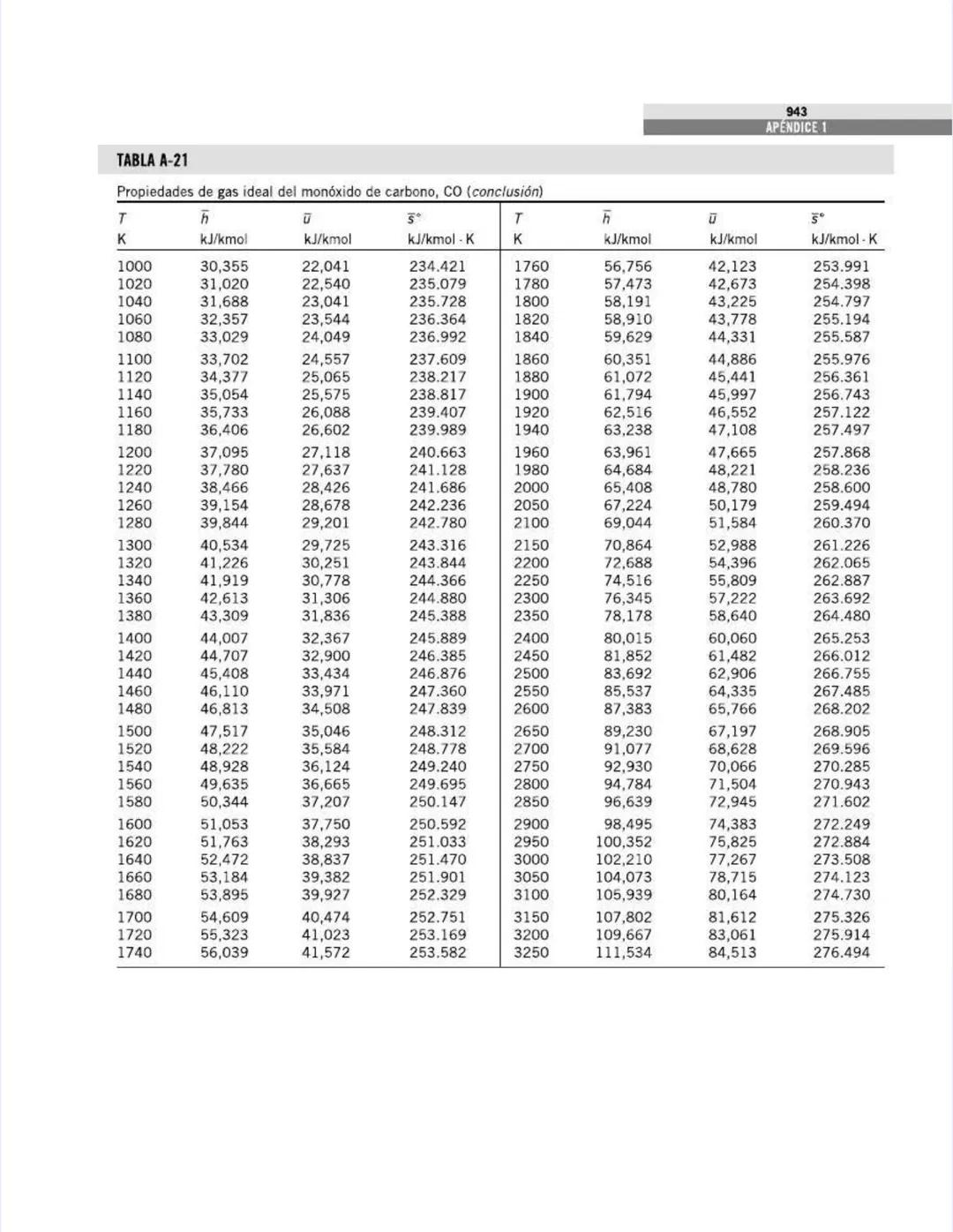
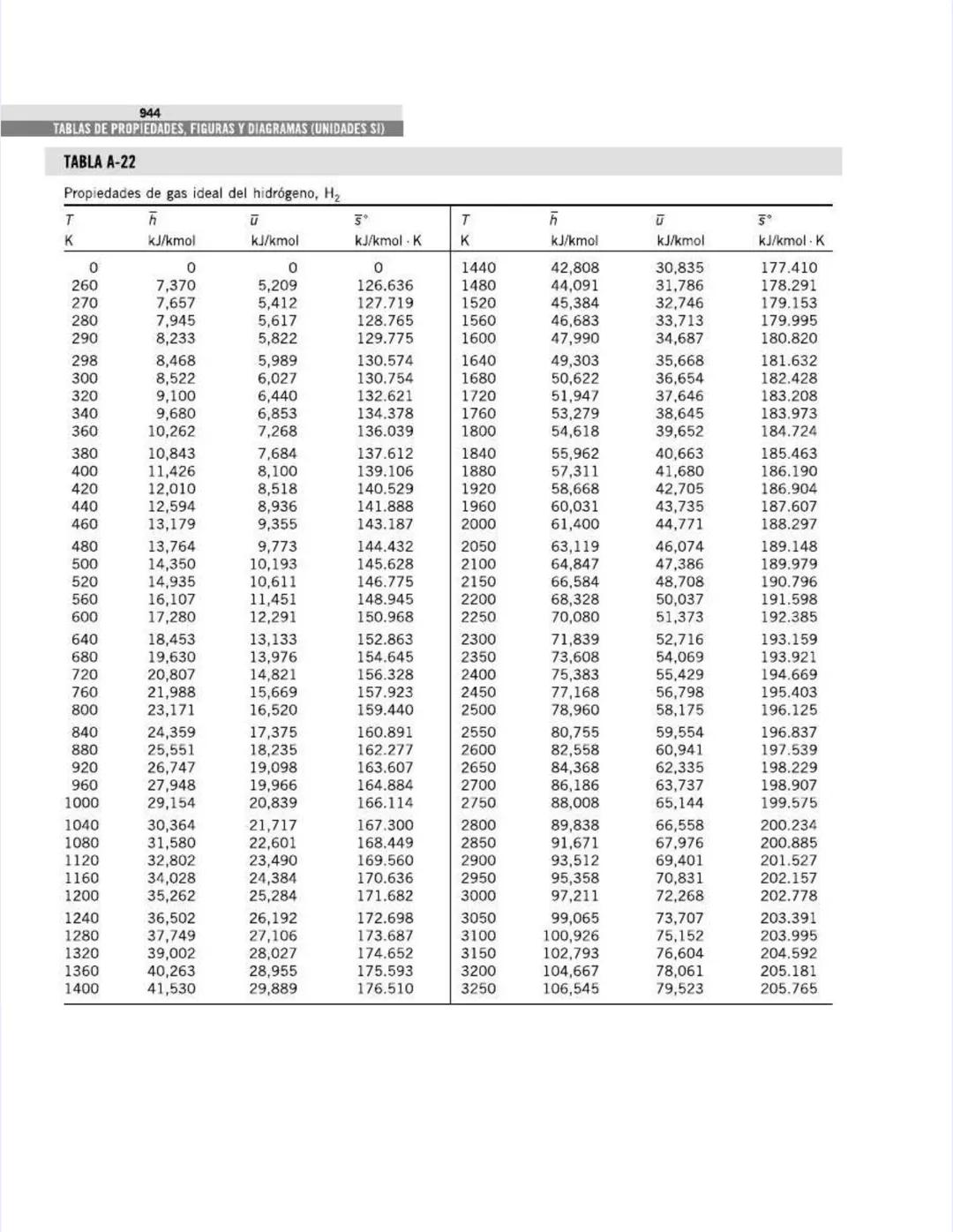
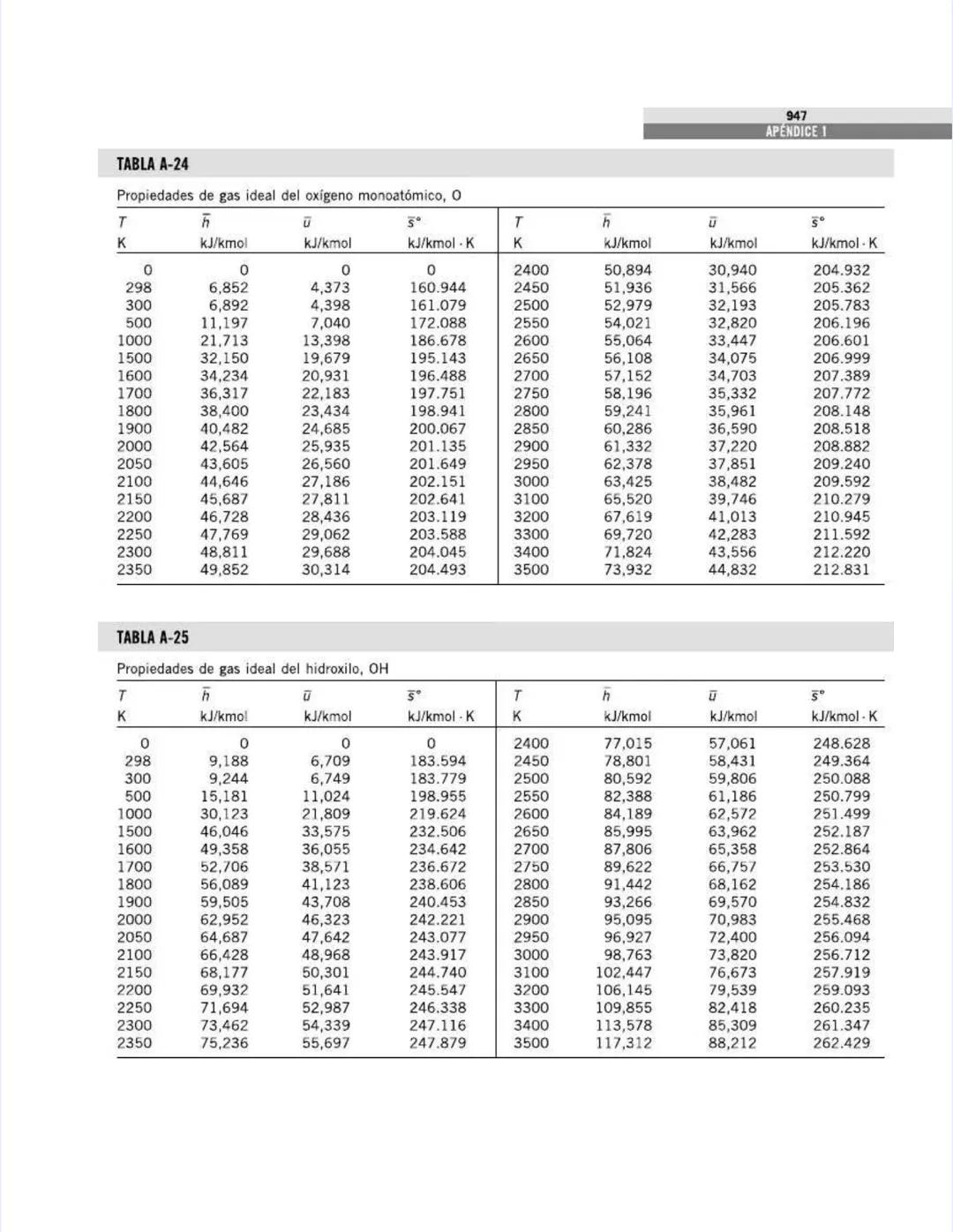
Esta tabla amplía la información anterior, mostrando cómo varían los calores específicos con la temperatura para gases comunes.
Para el aire, observa cómo Cp aumenta gradualmente:
Esta variación es crucial para cálculos precisos en sistemas que operan con grandes diferencias de temperatura, como turbinas de gas o motores de combustión interna.
El dióxido de carbono (CO₂) muestra una variación aún más significativa con la temperatura, lo que explica su comportamiento único en procesos térmicos:
También notarás que la relación k disminuye con la temperatura para la mayoría de los gases. Para el aire:
Estos cambios pueden parecer pequeños, pero tienen un impacto significativo en el cálculo de:
💡 Cuando realices análisis de ciclos termodinámicos que operen en amplios rangos de temperatura (como ciclos Brayton), considera usar valores de calor específico adecuados para cada nivel de temperatura o utiliza valores promedio para mayor precisión.
Usar valores incorrectos de calores específicos puede llevar a errores significativos en tus cálculos de eficiencia y rendimiento energético.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
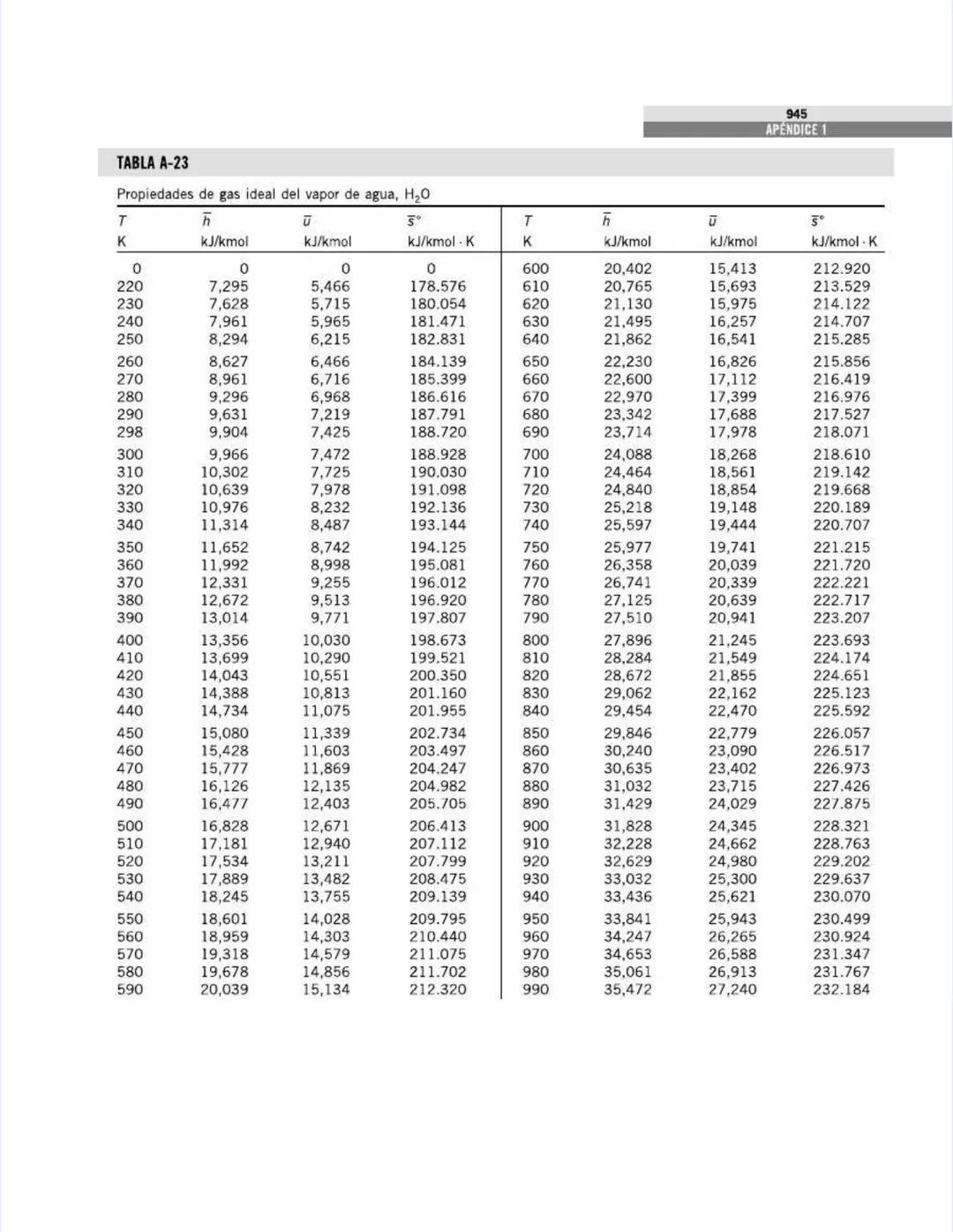
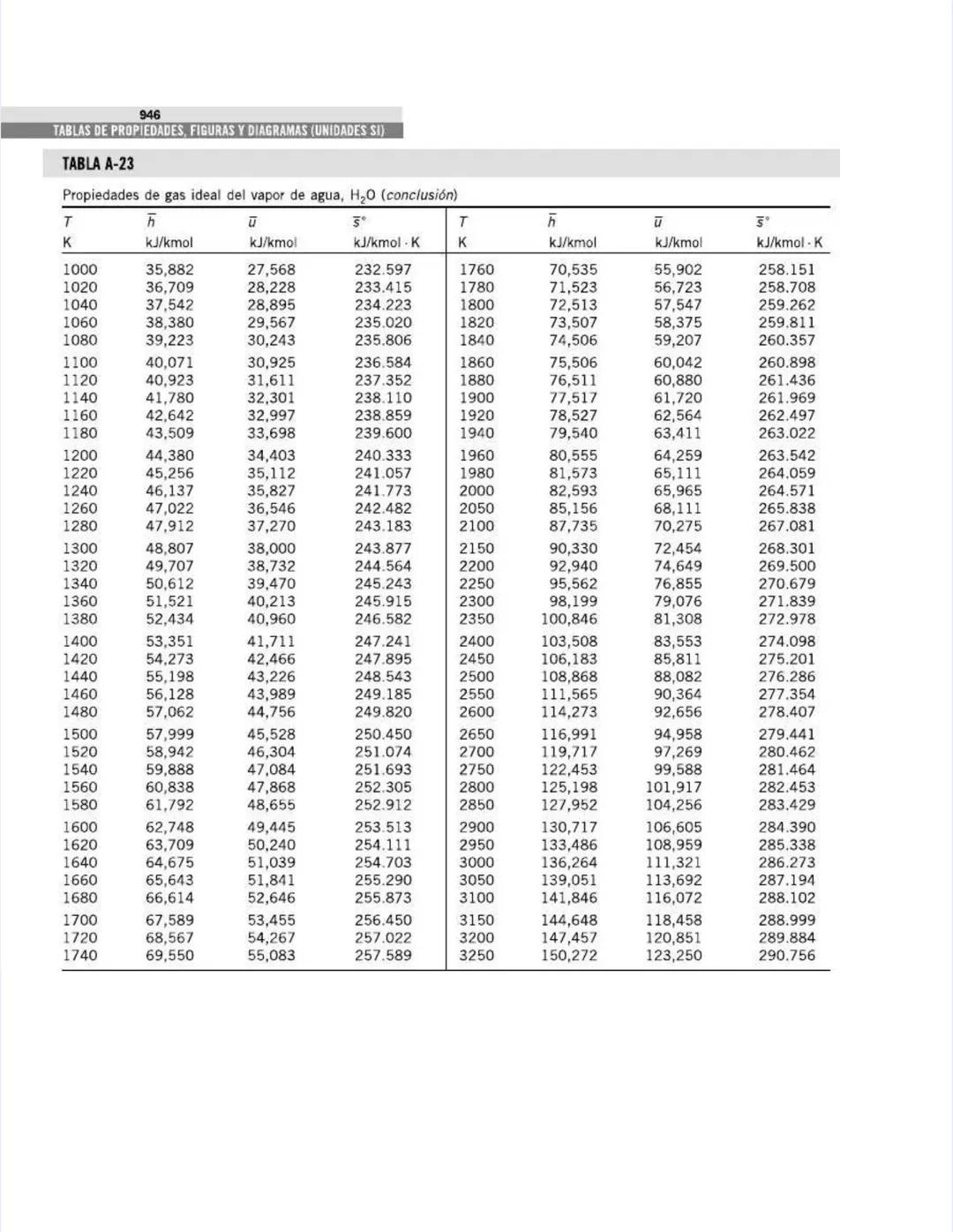
Esta tabla proporciona ecuaciones polinómicas para calcular calores específicos con mayor precisión. La fórmula general es:
cp = a + bT + cT² + dT³
donde T está en Kelvin y cp en kJ/kmol·K (¡nota que es por kmol, no por kg!).
Para sustancias como el metano (CH₄), los coeficientes son:
Estas ecuaciones son extremadamente valiosas para:
La tabla también muestra el rango de temperatura donde estas ecuaciones son válidas, generalmente entre 273-1500 K o 273-1800 K, así como el porcentaje de error máximo y promedio.
El agua (vapor) tiene un comportamiento bastante complejo, con coeficientes:
💡 Para convertir los calores específicos de base molar a base másica , simplemente divide por la masa molar de la sustancia. Por ejemplo, para el CO₂ con masa molar de 44.01 kg/kmol, divide los valores calculados por 44.01.
Estas relaciones permiten programar modelos termodinámicos precisos y resolver problemas complejos que requieren integración de cp en amplios rangos de temperatura.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
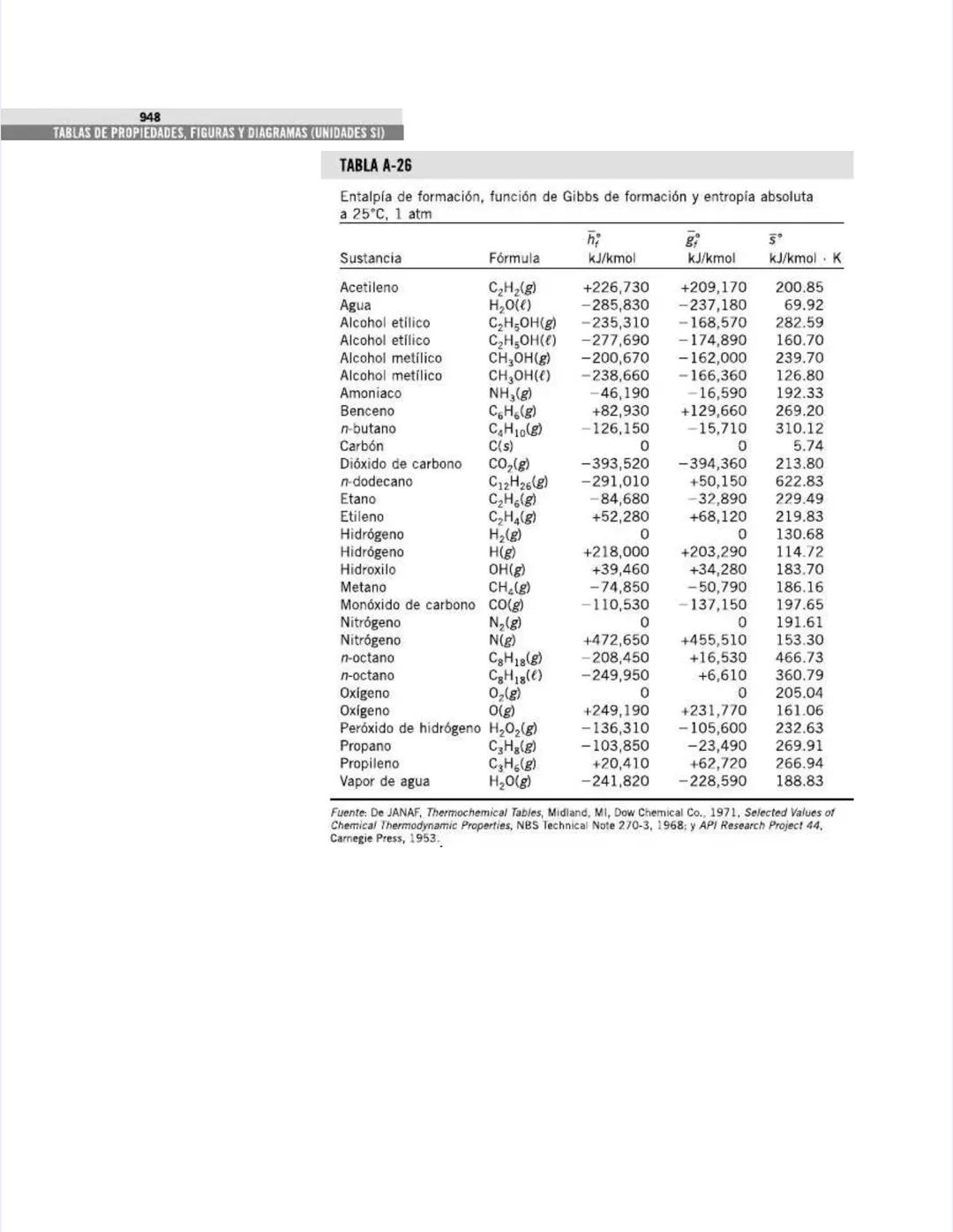
Esta tabla es un recurso invaluable para aplicaciones prácticas de ingeniería. Contiene propiedades físicas de sustancias en estados diferentes al gaseoso.
Para los líquidos, encuentras datos esenciales como:
Por ejemplo, el agua a 25°C tiene una densidad de 997 kg/m³ y un calor específico de 4.18 kJ/kg·K, mientras que el mercurio tiene una densidad mucho mayor pero un calor específico mucho menor .
Para refrigerantes como el amoniaco, puedes encontrar que tiene un calor latente de vaporización de 1357 kJ/kg a -33.3°C, un dato crucial para diseño de sistemas de refrigeración.
Observa cómo la densidad de la mayoría de los líquidos disminuye con la temperatura. Por ejemplo, el agua:
Esta información es esencial para calcular:
💡 El calor latente de vaporización disminuye a medida que aumenta la temperatura, llegando a cero en el punto crítico. Esta es una consideración importante en ciclos de potencia y refrigeración que operan cerca de condiciones críticas.
La tabla incluye también datos para petróleo, queroseno y salmuera, que son fluidos ampliamente utilizados en aplicaciones industriales.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
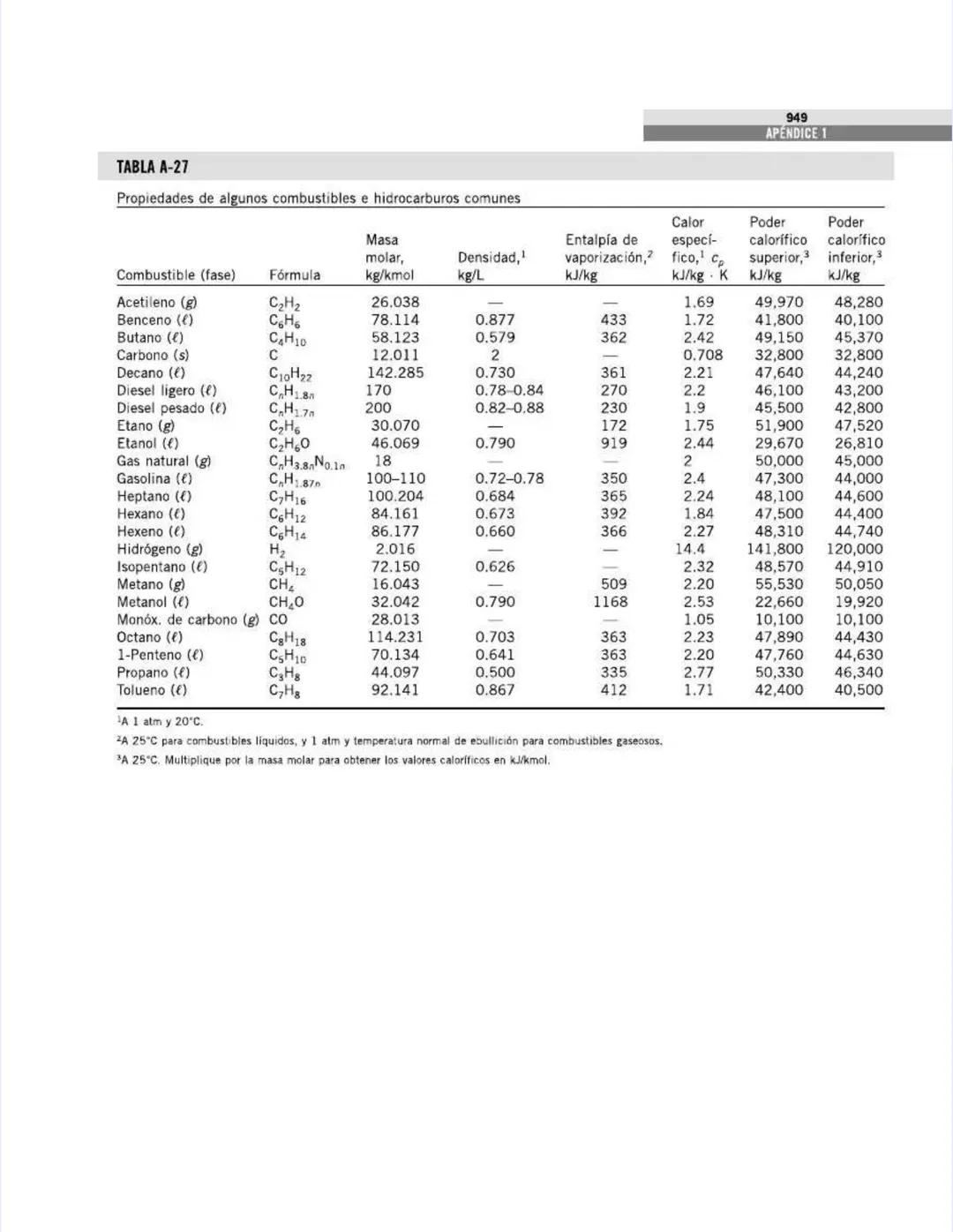
Esta tabla continúa ofreciendo datos valiosos, ahora para sólidos y alimentos, información crucial para aplicaciones de transferencia de calor e ingeniería alimentaria.
Para los sólidos, la tabla muestra:
Comparando metales:
Los materiales de construcción muestran propiedades interesantes:
Para los alimentos, la tabla proporciona:
Las frutas y verduras tienen alto contenido de agua:
El contenido de agua afecta directamente el calor específico y el calor latente. Por ejemplo:
💡 Estos datos son fundamentales para el diseño de procesos de congelación, almacenamiento y cocción de alimentos. La gran diferencia entre calores específicos de alimentos congelados y no congelados explica por qué los tiempos de descongelación son mucho mayores que los de congelación.
Utiliza esta información para cálculos de refrigeración, procesamiento térmico y diseño de sistemas de almacenamiento.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Esta tabla es una de las más utilizadas en termodinámica. Proporciona las propiedades del agua saturada a diferentes temperaturas, permitiéndote encontrar rápidamente valores fundamentales para análisis de ciclos de potencia, refrigeración y sistemas térmicos.
La tabla está organizada por temperatura y muestra:
Por ejemplo, a 20°C:
Observa cómo estas propiedades cambian con la temperatura:
💡 En el punto crítico (374°C), el calor latente se vuelve cero y las propiedades del líquido y vapor son idénticas. Este comportamiento es fundamental para entender ciclos supercríticos en centrales eléctricas modernas.
Esta tabla será tu referencia constante para resolver problemas de transferencia de calor, ciclos de Rankine y procesos de evaporación o condensación.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
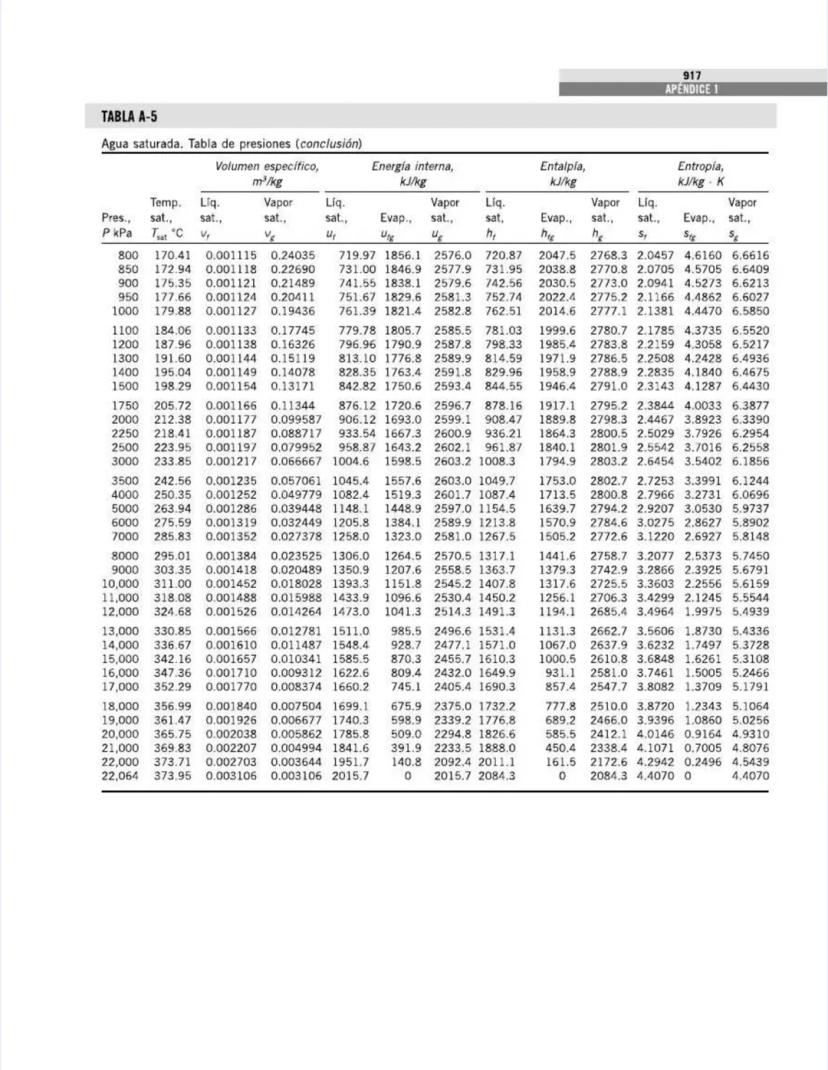
La tabla continúa mostrando las propiedades del agua saturada, ahora para temperaturas más altas (205°C a 373.95°C).
A medida que la temperatura se acerca al punto crítico (373.95°C), observa estas tendencias importantes:
La presión de saturación aumenta exponencialmente:
El volumen específico del líquido aumenta mientras el del vapor disminuye:
El calor latente disminuye hasta llegar a cero:
La diferencia de entropía entre líquido y vapor también disminuye:
💡 Estas tendencias son cruciales para entender el comportamiento de ciclos de potencia y refrigeración. En centrales termoeléctricas supercríticas, el agua no experimenta un cambio de fase distinto, lo que mejora la eficiencia térmica.
La tabla fue generada con ecuaciones de estado de alta precisión , que representa una mejora respecto a formulaciones anteriores y garantiza valores precisos para tus cálculos de ingeniería.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
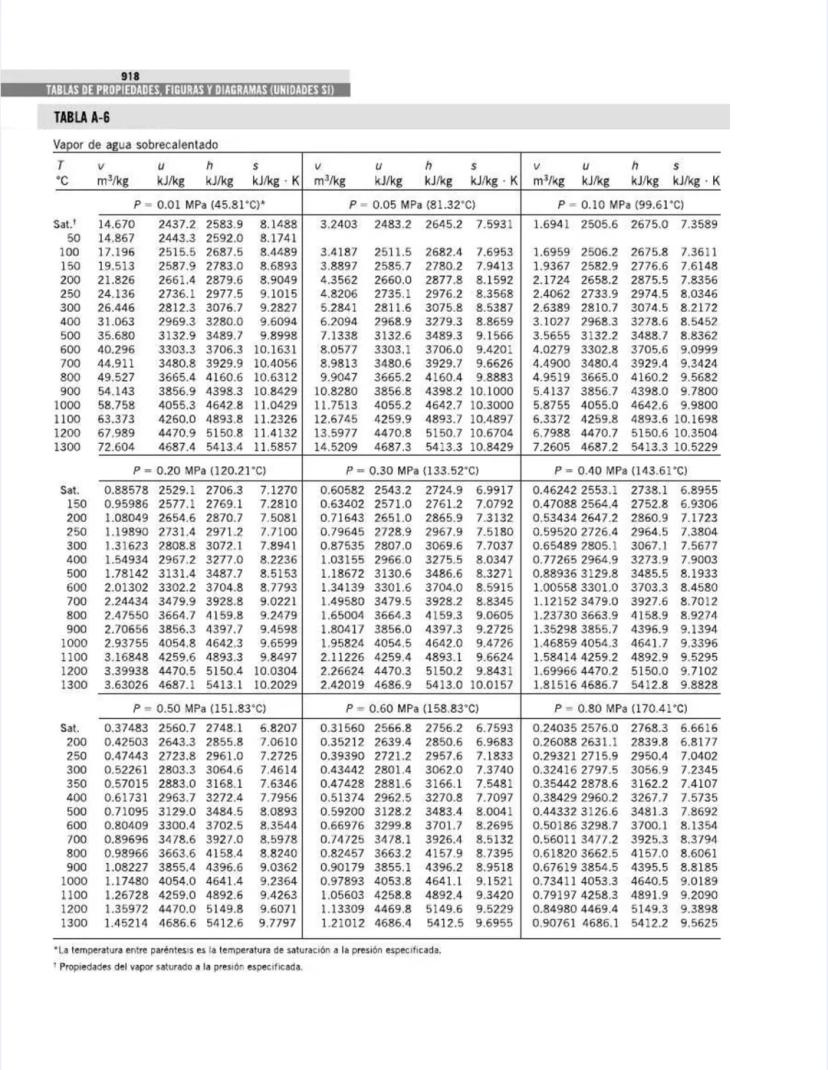
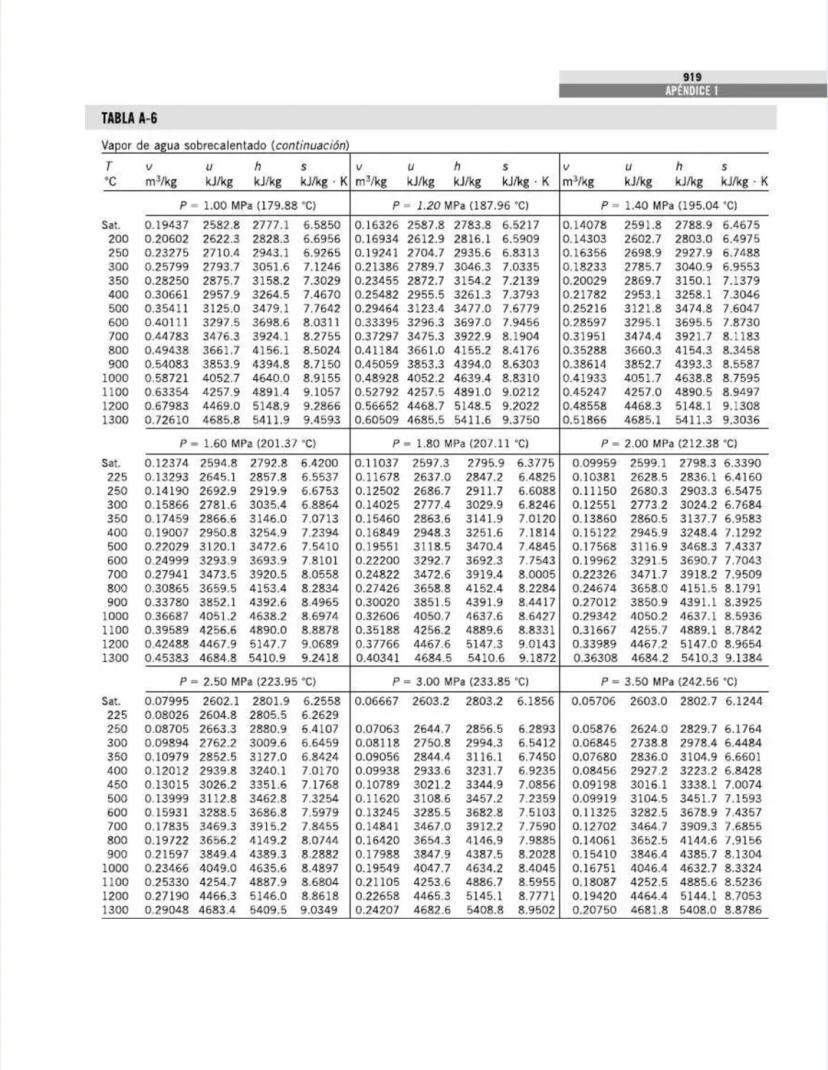
Esta tabla complementa la anterior, pero ahora está organizada por presiones en lugar de temperaturas. Es particularmente útil para análisis de ciclos de potencia y sistemas que operan a presiones específicas.
Para cada presión, puedes encontrar:
Por ejemplo, a presión atmosférica (101.325 kPa):
Para análisis de ciclos de Rankine, observa los valores a presiones típicas:
La tabla cubre un amplio rango de presiones, desde vacío parcial (1 kPa) hasta presiones supercríticas (22,064 kPa), permitiéndote analizar desde condensadores de baja presión hasta calderas de alta presión.
💡 La presión crítica del agua es 22.06 MPa, donde el calor latente se vuelve cero. En sistemas supercríticos, no hay una distinción clara entre líquido y vapor, lo que permite ciclos más eficientes al eliminar la necesidad de calor latente durante el cambio de fase.
Esta tabla es fundamental para dimensionar equipos térmicos como calderas, condensadores, y turbinas de vapor.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
1
Herramientas Inteligentes NUEVO
Transforma estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Fichas Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener problemas para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuaria de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser realmente difícil recopilar toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis apuntes y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuaria de Android
Estaba constantemente estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a gestionar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZ Y FLASHCARDS SON SÚPER ÚTILES Y ME ENCANTA Knowunity IA. ADEMÁS ES LITERALMENTE COMO CHATGPT PERO MÁS LISTO!! ME AYUDÓ TAMBIÉN CON MIS PROBLEMAS DE MÁSCARA!! Y CON MIS ASIGNATURAS DE VERDAD! OBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuaria de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros - me siento mucho más seguro al prepararme para los exámenes.
Paul T
usuario de iOS